Эпигенетическое редактирование снизило уровень холестерина у мышей
Итальянские исследователи создали белковые конструкции для целевого редактирования эпигенетических меток в организме млекопитающего без изменения нуклеотидной последовательности. Метилирование гена белка PCSK9 у мыши подавило его активность как минимум на 11 месяцев. Этот белок — мишень препаратов, снижающих уровень холестерина, и эпигенетическое выключение его гена может стать перспективным клиническим подходом.
В конце прошлого года была одобрена первая терапия на основе CRISPR-Cas9 — редактирование вне организма гемопоэтических стволовых клеток и клеток-предшественников эритроцитов, взятых у пациентов с серповидноклеточной анемией или бета-талассемией. В новой работе, результаты которой опубликованы в Nature, предложен иной подход — редактирование эпигенома непосредственно в организме.
Существуют технологии, которые не изменяют последовательность нуклеотидов в ДНК, но меняют эпигенетические метки, в частности, присоединяют к ДНК метильные группы, что подавляет активность гена. Однако было неясным, насколько они применимы в клинике.
Анджело Ломбардо, исследователь генной терапии из Научного института Сан-Раффаэле в Милане, и его коллеги использовали для нацеливания на мишень белки с цинковыми пальцами (ZFP), специфически взаимодействующие с определенными последовательностями ДНК. ZFP оказался более эффективным, чем неразрезающая dCas9 и белок TALE.
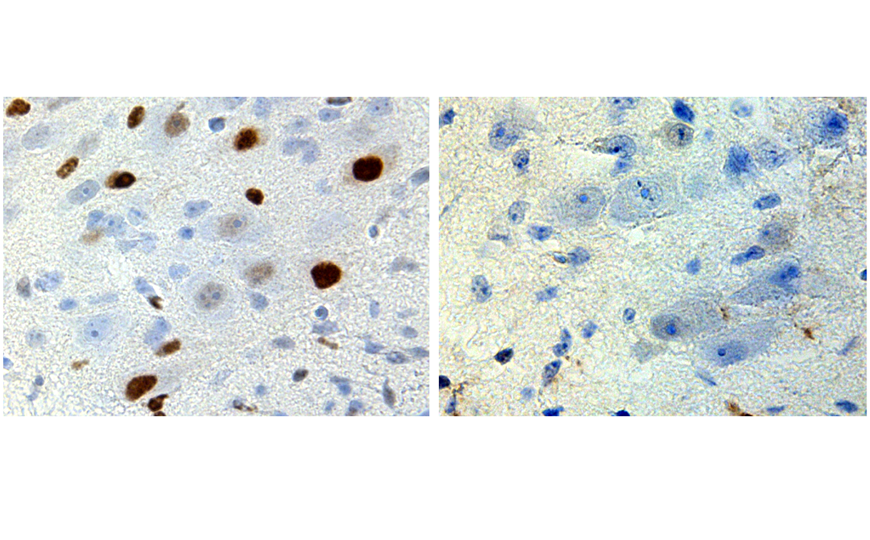
Команда разработала ZFP, который связывается с геном Pcsk9 — известной мишенью ряда препаратов, снижающих холестерин. К этому ZFP они присоединяли фрагменты белков, которые метилируют ДНК во время эмбрионального развития, чтобы избежать активации провирусов, встроенных в геном (KRAB, каталитический домен de novo ДНК-метилтрансферазы A и ее кофактор DNMT3L). Полученную конструкцию, включающую ZFP и метилирующие домены, они назвали EvoETR (evolved engineered transcriptional repressor).
Идея была в том, что использование естественных механизмов долгосрочного метилирования, обеспечит и долгосрочное выключение выбранного гена. В то же время не происходит нецелевого редактирования, характерное для CRISPR.
Взрослым мышам C57BL/6 однократно вводили в вену мРНК белка-редактора в липидных наночастицах, обеспечивающих доставку в клетки печени. У животных, которые получили экспериментальный препарат, общий холестерин и холестерин, связанный с липопротеинами низкой плотности, снизились в течение месяца. Уровни белка PCSK9 у них оставались низкими на протяжении 330 дней.
Интересно, что сайленсинг гена Pcsk9 и сопутствующие эпигенетические репрессивные метки сохранялись в растущей печени мышей, когда ее часть удаляли хирургическим путем. Следовательно, делящиеся гепатоциты передавали метки дочерним клеткам.
Этот результат, вероятно, еще усилит интерес к эпигенетическому редактированию в клинике. Как отметила эпигенетик Марианна Ротс (Университетский медицинский центр Гронингена, Нидерланды), в комментарии для Nature, уже более десятка компаний занимаются разработкой методов эпигенетического редактирования. Есть сообщения о долгосрочном эффекте в опытах на обезьянах, но эти результаты пока не опубликованы в рецензируемых журналах. Компания Omega Therapeutics (Кембридж, Массачусетс), проводит клинические испытания эпигенетического редактора, деактивирующего ген MYC, активность которого повышена при многих видах рака.
Новые линии мышей для редактирования эпигенома на основе системы CRISPR-Cas9
Источник
Cappelluti, M.A., et al. Durable and efficient gene silencing in vivo by hit-and-run epigenome editing // Nature (2024). DOI: 10.1038/s41586-024-07087-8


 Меню
Меню





 Все темы
Все темы




 0
0