МД-2025: Молекулярно-генетические исследования в онкологии
Есть ли разница между мутациями в BRCA1 и BRCA2? Что уже сейчас может показать жидкостная биопсия? Какие молекулярно-генетические исследования рекомендованы при раке мочевого пузыря? Появление каких клеток в асцитической жидкости особо опасно при раке яичника? Как метилирование мРНК связано с опухолеобразованием? Таким вопросам была посвящена секция «Молекулярно-генетические исследования в онкологии».
Максим Леонидович Филипенко, д.б.н. ФГБУН ИХБФМ СО РАН, г. Новосибирск
Фото: Андрей Константинов
В начале секции Евгений Имянитов, чл.-корр. РАН, д.м.н., профессор ФГБУ «НМИЦ онкологии им. Н.Н. Петрова» Минздрава России, прочитал доклад на тему «BRCA1 versus BRCA2».
Гены BRCA1 и BRCA2 были открыты в 1994 и 1995 годах соответственно. С тех пор их часто употребляют скороговоркой как синонимы. Что общего у этих генов? Они оба предрасполагают к раку молочной железы и яичника. Но тут тоже есть определенные нюансы. BRCA1 — это скорее рак молочной железы без гормональных рецепторов. Рак яичников — это тоже скорее BRCA1, а не BRCA2. А BRCA2 ассоциирован еще с раком простаты и поджелудочной железы, что часто игнорируется.
У представителей славянской национальности наибольшая часть мутаций приходится на ген BRCA1, на ген BRCA2 — значительно меньше. Соответственно, в России другая статистика по наследственному раку простаты или раку поджелудочной железы, если сравнивать с Великобританией или США, где мутации в BRCA2 встречаются чаще.
Все это начало вызывать интерес, когда оказалось, что эти опухоли надо иначе лечить. Здесь уникальный механизм. Как правило, опухоль потому и возникает, что инактивируется оставшаяся копия гена BRCA1/2. То есть одна мутация унаследована, а вторая мутация — соматическая. Возникает дефицит белка BRCA1 или BRCA2. Оба эти белка восстанавливают ДНК после двунитевых разрывов. Достаточно дать препарат, который вызывает двунитевые разрывы, и опухолевая клетка погибнет.
Этот механизм является более или менее универсальным. Но если мы берем опухоли молочной железы, то в случае BRCA2 половина опухолей не имеет BRCA-дефицита, утраты оставшейся копии гена и мишени для терапии. В то время как для BRCA1 эта цифра намного меньше, ею фактически можно пренебречь.
При лечении рака яичника сегодня для всех случаев одна стандартная схема — это платина плюс таксаны. BRCA2-ассоциированные опухоли демонстрируют отличный эффект, а для BRCA1 этот эффект заметно меньше. С чем это связано?
По-видимому, если опухоль ассоциирована с геном BRCA1, и в клетке есть инактивация BRCA1, то такие клетки резистентны к таксанам. А вот если присутствует инактивация BRCA2, то таксаны прекрасно действуют независимо от статуса BRCA. Сейчас ведутся проспективные клинические испытания, в рамках которых BRCA1-ассоциированные опухоли лечат с цисплатином и митомицином.
Совершенно противоположная ситуация при раке молочной железы. Дело в том, что BRCA2-ассоциированные опухоли, в отличие от BRCA1-ассоциированных опухолей, очень часто имеют гормон-рецептор-позитивный статус. То есть они чувствительны к эндокринной терапии. И, по-видимому, они просто не имеют утраты оставшейся копии гена.
То есть, несмотря на то что на сегодняшний день для BRCA-ассоциированных опухолей считается стандартным лечение производной платины или PARP-ингибиторы, по-видимому, половина BRCA2-опухолей не будет к ним чувствительной.
В исследованиях предоперационной неоадъювантной терапии статус рецепторов имеет большее значение, чем наличие или отсутствие мутации BRCA1 или BRCA2.
Это принципиальная смена подхода к лечению рака молочной железы, потому что на сегодняшний день, если обнаружена BRCA-мутация, то таких пациенток предлагается лечить PARP-ингибиторами или более привычными препаратами, производными платины, и в какой-то степени игнорировать статус рецепторов. Но, по новым данным, в первую очередь надо учитывать статус рецепторов при планировании терапии, и уже только во вторую очередь BRCA-статус.
Лет 15 назад продемонстрировали, что BRCA-ассоциированные опухоли чувствительны к производным платины, и 6–7 лет назад стало принято при лечении трижды негативного рака добавлять карбоплатин к стандартной схеме терапии.
Группа докладчика показала, и это подтверждается другими данными в похожих исследованиях, что, если речь про опухоль без наследственных мутаций, при трижды негативном раке добавление платины имеет смысл. А вот если речь про BRCA-ассоциированные опухоли, то нет смысла добавлять платину к стандартной антрациклин-содержащей терапии. Потому что антрациклины и платина имеют на BRCA-ассоциированные клетки примерно одинаковое действие, и в данном случае только увеличивается токсичность терапии.
По-видимому, нужно по-разному лечить BRCA1 и BRCA2-ассоциированные раки молочной железы. Мало говорить про BRCA-статус, нужен еще анализ опухолевой клетки на предмет утраты оставшейся копии гена или статуса хромосомной нестабильности. А статус гормональных рецепторов — эстрогенов и протестеронов — более значимая характеристика, чем наличие BRCA-мутации.
При раке предстательной железы ключевое значение имеет назначение PARP-ингибиторов на основе так называемых мультигенных тестов — тестов HRR (от homologous recombination repair)+.
Есть HRR-панели для очень похожих препаратов, двух разных PARP-ингибиторов. В одном случае это панель на 15 генов, в другом — на 12, только 8 из них перекрываются. В какой-то степени те диагностические тесты, которые есть, носят произвольный характер. Только BRCA2-ассоциированные опухоли чувствительны к подобной таргетной терапии, для BRCA1 нет никакого эффекта.
Группа докладчика проанализировала больше тысячи случаев рака простаты. Сначала делали тест HRR на 34 гена. Там, где хватало ткани, после этого сканировали весь геном для того, чтобы выявить признаки дефицита гомологичной рекомбинации ДНК, дефицита восстановления ДНК после двунитевых разрывов, независимо от того, мутированы гены или нет.
На так называемый наследственный рак простаты приходится чуть больше 8% пациентов. Признаки чувствительности опухоли к PARP-ингибиторам или производным платины обнаруживлись примерно у 5% пациентов, у которых не выявлены никакие значимые мутации. Поэтому, если говорить о перспективе на ближайшие лет 5, то назначение препаратов должно основываться не на мутационных тестах, а на сканировании всего генома на предмет хромосомной нестабильности.
В BRCA2-ассоциированных опухолях в большинстве случаев был выраженный дефицит гомологичной рекомбинации ДНК. А в случае BRCA1 практически нет признаков хромосомной нестабильности и нет чувствительности к соответствующей препаратам. Это соответствует результатам клинических исследований.
Интересно, что PALB2, еще один ген, который очень похож на BRCA, демонстрирует примерно такое же значение для выбора терапии.
Таким образом, BRCA1 и BRCA2 разные по биологическим функциям, по спектрам и характеристикам ассоциированных опухолей, по частоте утраты оставшейся копии гена, по чувствительности к таксанам. Но современные клинические испытания и рутинная клиническая практика продолжают говорить скороговоркой BRCA1 и 2, даже используется термин BRCA без спецификации гена. Однако это клинически разные гены, и такие опухоли должны лечиться по-разному.
Доклад на тему «Новости “жидкостной биопсии”» Максим Филипенко, д.б.н. ФГБУН ИХБФМ СО РАН.
Жидкостная биопсия — это получение информации об опухоли с использованием ее компонентов, которые попадают в системную циркуляцию. Это могут быть белки, клетки, но наиболее часто все-таки говорят об анализе ДНК и начинают говорить об анализе РНК.
Основной вопрос — какова клинико-диагностическая целесообразность этой процедуры.
Жидкостная биопсия для онкологических заболеваний сегодня внесена в различного рода рекомендации. NCCN предлагает выполнять жидкостную биопсию для поиска таргетируемых мутаций в тех случаях, когда ДНК мало или нельзя достать ткани.
Есть две локализации – это немелкоклеточный рак легкого и рак молочной железы, где есть уже конкретные гены и аппликации, например, выявление мутации Т790M в гене EGFR для мониторинга возникающей резистентности к TK1-первого поколения.
Также расширились показания для рака молочной железы. Здесь появился интересный ген ESR1, точнее, его соматические мутации. Мутации в гене ESR1 являются частой причиной возникающей эндокринной резистентности.
При терапии гормонпозитивного рака молочной железы мутации возникают в той части гена, которая кодирует эстроген-связывающий домен, в результате чего происходит изменение структуры белка. Белок фосфорилируется, димеризуется, транслоцируется в ядро и запускает пролиферативную программу. То есть эти мутации являются классическими соматическими активирующими мутациями.
Когда говорят про метастатическое заболевание, то, беря биопсию из одного места, теряют другие. Жидкостная биопсия интегрирует первичный очаг и все метастазы. И с какого-то момента основной пулы исследований по соматическим мутациям гена ESR1 был перенесен в жидкостную биопсию. В результате было показано, что частота возникновения таких мутаций пропорциональна длительности эндокринной терапии и количеству линий эндокринной терапии. Эти мутации появляются в системной циркуляции намного раньше признаков радиологической прогрессии.
Это инициировало ряд клинических исследований, например, PADA-1. Брали пациентов, которые проходили терапию ингибиторами ароматазы плюс ингибиторами CDK4/6, соматические мутации ESR1 мониторировались динамически во времени раз в 2 или в 3 месяца с помощью цифровой ПЦР. В том случае, если такие мутации находились, и следующий тест показывал увеличение их концентрации, то часть пациентов переключали на другую схему, то есть фактически уходили от ингибиторов ароматазы. Это давало выигрыш во времени до прогрессирования.
То есть смена терапии на основе мониторирования возникающей мутации с помощью жидкостной биопсии дает возможность продлить безрецидивную выживаемость пациента.
В исследовании SERENA-6, результаты которого были доложены в этом году, также брались пациенты, которые проходили терапию ингибиторами ароматазы плюс CDK4/6, но они постоянно мониторировались на предмет наличия соматических мутаций ESR1 в плазме.
Как только эти мутации возникали, не дожидаясь клинического прогрессирования, пациентов стратифицировали в две группы, в одной продолжали старую терапию, в другой назначали иную терапию. Смена терапии на основании этого теста тоже вела к выигрышу времени до прогрессии.
Таким образом, можно на основе молекулярного теста принимать решение о смене терапии, о наличии возникающей резистентности и получать выигрыш для пациента.
Это все попало в клинические рекомендации ASCO, ESMO, NCCN. Но впервые для жидкостной биопсии все практически регуляторные органы говорят о том, что жидкостную биопсию нужно делать, и что она предпочтительнее тканевой, то есть она имеет лучшую чувствительность и информативность.
Другая очень важная история — это молекулярная резидуальная болезнь для модификации адъювантной терапии. В 2016 году показали, что можно мониторировать послеоперационную циркулирующую опухолевую ДНК у пациентов с колоректальным раком. И наличие этой ДНК — это мощный прогностический фактор для рецидива.
Но не очень понятно, можно ли скалировать эту адъювантную терапию, чтобы помочь пациенту. Сегодня существует две стратегии выполнения такого рода тестов.
Первая подразумевает то, что сначала опухоль изучают, секвинируют, выявляют мутации, а для них уже делают либо маленькую таргетную NGS-панель, либо используют чувствительную цифровую ПЦР.
И второй, агностический подход, когда сразу секвинируют циркулирующую опухолевую ДНК, и потом с помощью различных биоинформационных или других подходов пытаются выделить процент фракции опухолевой ДНК из этого суммарного препарата.
Были публикации, но в классических плацебо-контролируемых двойных слепых клинических исследований, чтобы посмотреть, можно ли повлиять на терапию, было мало.
Но в этом году FDA дал статус Breakthrough Device Designation для набора Haystack test от Quest Diagnostics, который как раз и осуществляет детекцию постоперационной циркулирующей опухолевой ДНК для принятия решения для пациентов с колоректальным раком 2 стадии.
Для пациентов, у которых статус отрицательный, можно исключить платину и таким образом снизить токсический эффект. Но выигрыша от эскалации терапии, по крайней мере, той, которую использовали в данном клиническом исследовании, статистически значимо не удалось получить. Но FDA этого все равно хватило для регистрации.
Другое направление — это то, что называется ранняя диагностика опухоли, или скрининговые тесты на основе детекции циркулирующей опухолевой ДНК.
Здесь тоже произошло в прошлом году очень важное событие, FDA зарегистрировало платформу SHIELD от компании Guardant Health, которая предназначена для раннего скрининга колоректального рака. Было проведено клиническое исследование, которое показало не очень хорошие характеристики: чувствительность в районе 80%, специфичность 90%. Для скринингового теста это не так много. А способность оценивать предраковые очаги у этого теста еще хуже, чем у классического теста на скрытую кровь. Но это создало некоторый прецедент.
Пока неясно, снизит ли тест количество смертей от колоректального рака. Будет ли он вообще экономически и логистически эффективным. Есть ряд публикаций в Lancet, которые говорят о том, что сегодняшние подходы для скрининга на основе жидкостной биопсии фактически экономически не имеют смысла. Требуются повышение специфичности. FDA рекомендует авторам пострегистрационные когортные наблюдения.
Основная проблема жидкостной биопсии сегодня — это чувствительность. Потому что мало опухолевой ДНК циркулирует в крови. Расти можно в сторону попыток увеличить количество ДНК, которую можно извлечь из пациента для анализа, и такие попытки предпринимались.
Так, в прошлом году в Science была опубликована работа, где авторы взяли липидные наночастицы, чтобы «загрузить» печень, чтобы она работала с этими наночастицами и не выводила циркулирующую опухолевую ДНК. Добавили еще антитела, которые могут защищать ее, и почти в 10 раз увеличили выход циркулирующей опухолевой ДНК у мышей.

Чтобы тесты нормально работали, нужны контрольные материалы. Контрольные материалы для жидкостной биопсии — это сложная история. Наверное, самое главное требование — чтобы это была либо человеческая реальная плазма с человеческой циркулирующей опухолевой ДНК, либо что-то, что ее моделирует максимально близко. Ну и количество должно быть немаленькое. Сегодня рекомендуют 4 мл плазмы на тест.
Последние два года группа докладчика занималась тем, что искала другой способ, и вот такой способ нашелся. Хороший источник плазмы — это лошадь, потому что много плазмы можно отобрать за раз, а плазма похожа на человеческую. Смешение компонентов стабилизации плазмы, нуклеосом и еще некоторых компонентов позволяет получить достаточно стабильный препарат, который может храниться при 8 градусах, не терять концентрации и представлять собой вот этот самый контроль, который можно получать, в общем-то, препаративных количествах.
«Мы очень надеемся, что в следующем году мы попытаемся провести какой-нибудь раунд для заинтересованных лабораторий», — добавил докладчик.
Ирина Демидова, к.м.н. ГБУЗ «МГОБ № 62 ДЗМ» г. Москвы, выступила с докладом на тему «Вопросы рационального применения высокопроизводительного секвенирования в онкологии».
С чем сталкивается даже самая лучшая генетическая лаборатория, которая работает в онкологическом учреждении? Что она работает не в каком-то безвоздушном пространстве, а рядом с реальными службами, которые тоже влияют на результаты генетического исследования. Это работа с патоморфологом, потому что материал должен быть правильно оценен. Зачастую приходится применять целый комплекс методов для того, чтобы определить нарушения, которые вроде бы являются генетическими. И это работа с клиницистами, которые являются конечными потребителями информации. Они должны понимать, что написано в заключении, а также каким-то образом контактировать для того, чтобы сложные случаи, которые сейчас встречаются все чаще и чаще, обсуждать.
NCCN пишет, что на самом деле большая часть методов придумана для образцов, которые фиксированы в формалине и залиты в парафин. К такой опции, как цитоблоки, NCCN относится довольно критически и не включает в основное тело рекомендации, тем не менее, упоминает об их важности.
Как взаимодействовать с патоморфологами? К сожалению, иногда приходят такие образцы, когда с одного блока, это был микробиоптат рака легкого, полученный с большим трудом, сделано 28 срезов. Зачем? Тайна, покрытая мраком. Но образец был полностью уничтожен в результате такого нерационального подхода. Сейчас в большинстве патоанатомических лабораторий, работающих с образцами, которые должны в дальнейшем пойти на генетическое тестирование, принята методика разумного использования материала. То есть крайне ограниченное количество срезов, причем для молекулярного тестирования срезы делаются одновременно с теми же срезами на ИГХ. Это делается для того, чтобы не допускать дальнейшего подравнивания, поскольку каждое подравнивание — это потеря материала.
При раке легкого подавляющее большинство образцов — это мелкие биопсии, содержание опухолевой ткани в которых зачастую очень невелико. Как правило, опираются на количество клеток, которые патоморфолог видит в образце, и в зависимости от этого образец берется на секвенирование. Формально клеток должна быть хотя бы тысяча. В такой ситуации секвенирование, как правило, удается.
Цитологический препарат идет исключительно на стандартные методы, на самые простые — ПЦР, FISH, если остается материал, что тоже в ряде случаев дает информацию.
На примере около 15% биоптата представляют собой опухолевую ткань. Так и получается, что при секвенировании была выявлена примерно 15%-ная фракция мутантного аллеля гена KRAS. Секвенирование удалось провести.
Еще один крайне сложный и неприятный случай — это когда в материале значительное количество некроза. Он не годится для секвенирования, поскольку некротическая ткань с обломками ДНК секвенируется и возникают артефакты.
Если результаты исследования вызывают сомнения, необходимо использовать полный арсенал методов, потому что от этого зависит жизнь пациента и его успешное лечение.
В настоящий момент уже очевидно, что секвенирование выявляет огромное количество соматических мутаций, которые требуют индивидуальной аннотации. Более того, даже в США только около 70% обнаруженных вариантов передаются в базы данных. Считается, что основные затраты, которые будут сопровождать высокопроизводительное секвенирование в будущем, пойдут уже не сам процесс секвенирования, не на приборы, а скорее на какую-то адекватную биоинформатику.
Еще одна серьезная проблема: каким образом репортировать аннотированные варианты в условиях специфики национальных рекомендаций. В первую очередь они репортируются по степени таргетабельности. Но, например, обнаружена инсерция 20-го экзона гена EGFR, в этом случае в настоящий момент существует эффективная терапия, которая позволяет отнести эти мутации к таргетабельным, но эта терапия недоступна в Российской Федерации. Эти случаи все равно репортируются как IA, но для России это IIC.

Любое внедрение каких-то высокопроизводительных методик в реальную практику — это процесс сложный, занимающий достаточно много времени и требующий довольно больших усилий. Это и адекватное отношение к материалу со стороны всех служб, и возможность сочетания различных методик, если необходимо подтвердить каким-то образом наличие обнаруженного варианта.
Доклад «Ключевые диагностические точки при раке мочевого пузыря» прочитала Людмила Любченко, д.м.н. ФГБУ «НМИЦ Радиологии» МЗ РФ.
В канцерогенез рака мочевого пузыря, как и других злокачественных образований, вовлечена обширная сеть сигнальных путей. Выявлены 20 генов, которые показали клинико-генетические корреляции и которые на сегодняшний день активно используются для оценки эффективности химиолучевой, таргетной и иммунотерапии.
Мишени для таргетной терапии при раке мочевого пузыря на сегодняшний день хорошо изучены и используются в клинической практике.
Конечно же, и наследственная предрасположенность играет важную роль в развитии рака мочевого пузыря. Так, 50% пациентов с уротелиальной карциномой имеют онкологически отягощенный семейный анамнез: 4,5% больных имеют родственников, страдающих раком мочевого пузыря. Частота мутации генов BRCA при раке мочевого пузыря составляет 20%. В 22% случаев были идентифицированы герминальные мутации в генах системы репарации.
Регуляторика молекулярно-генетических исследований при раке мочевого пузыря представлена в актуальных рекомендациях NCCN и предполагает определение статуса FGFR, MSI, MMR, HER2, тогда как в российских рекомендациях сделан акцент на отсутствие зарегистрированных систем по FGFR-тестированию и необходимости проведения BRCA и других видов тестирования при наследственной патологии с последующим медико-генетическим консультированием, что требует дополнения российских рекомендаций.
Евгения Кайгородова, д.м.н., доцент НИИ онкологии Томского НИМЦ; ФГБОУ ВО СибГМУ Минздрава России, выступила с докладом «Жидкостная биопсия как инструмент прогнозирования течения опухолей женской репродуктивной системы: данные клинического исследования NCT04817501».
В структуре онкологической заболеваемости женщин наибольший удельный вес имеют злокачественные новообразование органов репродуктивной системы. Около 30% пациентов с начальной стадией заболевания имеют рецидивы и метастазы рака. Прогнозирование того, у кого будут метастазы либо рецидивы, остается сложной задачей.
Циркулирующие опухолевые клетки (ЦОК) являются главной причиной возникновения метастазов и рецидивов рака. Жидкостная биопсия представляет собой минимально инвазивную процедуру, которая основана на заборе крови либо асцитической жидкости, теоретически — любой жидкости организма, для оценки циркулирующих опухолевых клеток, а также факторов производных опухолей в виде циркулирующей ДНК, мРНК, внеклеточных везикул и опухолевых белков.
Источниками ЦОК могут быть первичные опухоли либо метастатические очаги. Подсчет, молекулярное профилирование и распространение ЦОК в неметастатических опухолях может обеспечить лучшее понимание значения ранней диссеминации опухоли.
Как известно, ЦОК представляют собой гетерогенную популяцию. Причем эта гетерогенность может быть как фенотипической, так и функциональной. Показано, что из всей массы ЦОК не более 0,01% дают начало метастазам. Показано также, что локализованные опухоли без клинически видимых метастазов являются источниками ЦОК.
В 2014 году в институте, в котором работает докладчица, было инициировано проспективное клиническое исследование по изучению фенотипического спектра ЦОК у больных с опухолями женской репродуктивной системы. В это исследование вошли больные раком молочной железы, яичников и эндометрия. В качестве материалов исследования служила венозная кровь и асцитическая жидкость.
В исследовании для оценки ЦОК использовали многоцветную проточную цитометрию. Проточная цитометрия является золотым стандартом и основным диагностическим инструментом в онкогематологии.
Было показано, что даже такая малая операционная травма, как биопсия, сопровождается увеличением количества стволовых ЦОК крови.
Неоадъювантная химиотерапия по-разному влияет на различные популяции ЦОК в крови у больных раком молочной железы. Был разработан способ прогнозирования риска плохого ответа опухоли на неоадъювантную химиотерапию у больных на основе данных ЦОК. Используя ROC-анализ, исследователи выявили три значимых фенотипа ЦОК, которые хорошо прогнозировали риск возникновения гематогенных метастазов до начала лечения.
Наличие этих клеток в крови у больных раком молочной железы сопровождается снижением пятилетней безметастатической и безрецидивной выживаемости. Так, EpCAM-отрицательные ЦОК снижали общую выживаемость больных раком молочной железы.
Интересные данные были получены при исследовании асцитической жидкости у больных раком яичников. Использование проточной цитометрии, а также проточной цитометрии с визуализацией показало большую гетерогенность EpCAM-положительных клеток.
Более того, были выявлены атипичные гибридные формы клеток, которые имели признаки как клеток крови CD45, так и маркеров опухолевых клеток EpCAM. И было показано, что данные атипичные клетки имели прямую корреляционную связь с индексом канцерматоза.
В 2022 году коллектив опубликовал обзор, в котором был предложен ряд теорий клеточного слияния и образования атипичных гибридных клеток.
Показано, что наличие одной атипичной гибридной клетки в одном кубическом миллиметре асцитической жидкости снижает общую выживаемость у больных раком яичников.
Была обнаружена прямая корреляционная связь между количеством атипичных гибридных клеток в асцитической жидкости и в крови больных раком яичников. Также показали прямую корреляционную связь количества этих атипичных гибридных клеток в крови с уровнем известных и широко применяемых сывороточных онкомаркеров. Концентрация данных клеток была выше в группе больных раком яичников по сравнению с группами с пограничными опухолями яичников.
Группой докладчицы был разработан способ определения риска опухолевой прогрессии у больных раком яичников на основе этих атипичных гибридных клеток и сывороточных онкомаркеров. Они предложили, что слияние опухолевых клеток с другими типами подвижных клеток может представлять собой дополнительный механизм распространения опухоли.
Ранее было показано, что атипичные гибридные формы ЦОК представляют собой хорошую модель для прогноза риска рецидивов и гематогенных метастазов у больных раком эндометрия. Так, наличие этих клеток сопровождалось снижением выживаемости без прогрессирования и общей выживаемости. Интересные данные также получили при оценке классических CD45-отрицательных клеток. Так, ЦОК с признаками эпителиально-мезенхимального перехода значимо снижали выживаемость без прогрессирования.
Что касается EpCAM-отрицательных ЦОК, которые были обнаружены при раке молочной железы, они точно так же встречались и у больных с раком эндометрия и показали свою хорошую прогностическую значимость по отношению к безметастатической и безрецидивной выживаемости.
Был получен патент на способ дооперационного прогнозирования риска рецидива у больных раком эндометрия 1 стадии на основе выявленных фенотипов циркулирующих опухолевых клеток, в том числе и атипичных и гибридных.
Профессор Ин Ян, Китайский национальный центр биоинформатики; Пекинский институт геномики, прочитала доклад «Epitranscriptomic Regulation of Carcinogenesis». Она рассказала, что модификации РНК (которые изучает эпитранскриптомика) играют фундаментальные роли в патологических процессах, особенно опухолеобразовании.
Помимо генетического кода, существует еще сложная система регуляции экспрессии, включающая модификации РНК. Есть более 170 типов метилирования РНК, включая N6-метиладенозин (m6A), 5-метилцитозин (m3C) и 7-метилгуанозин (m7G).

Вопрос в том, возможно ли обратить вспять метилирование РНК, и есть ли у него биологические роли, как у метилирования ДНК.
Так что идет разработка технологий секвенирования и биоинформатического анализа метилирования РНК, идентификация молекулярного механизма этих модификаций (идентификация ферментов и их ролей в РНК-процессировании), а также ролей модификаций РНК в физиологических и патологических процессах.
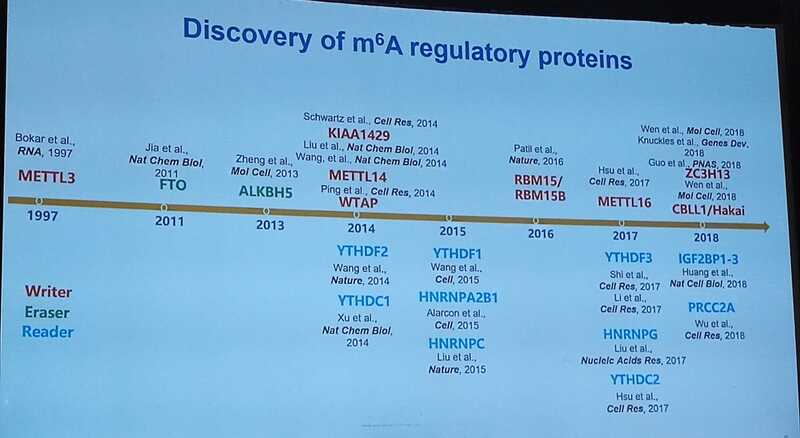
В 1997 году был выявлен фермент, устанавливающий метку m6A, — METTL3. Позже идентифицировали ферменты, убирающие метку, — FTO и ALKBH5, а также целый ряд белков, считывающих ее, включая белки семейства YTH. Они играют роли в процессировании РНК, включая сплайсинг, трансляцию, деградацию, стабилизацию и так далее. Многие регуляторы были выявлены группой докладчицы.
Они сосредоточились на технологии секвенирования m6A, m5A и m7G и на идентификации динамики и биологической роли метилирования РНК через выявление их регуляторов. Оказалось, модификации РНК играют роли в норме и при патологиях — гаметогенезе, эмбриогенезе и опухолеобразовании.
Сначала группа докладчицы сосредоточилась на m6A и идентифицировала ферменты FTO, ALKBH5, WTAP, YTHDC1, YTHDF3 и PRCC2A.
Затем докладчица инициировала изучение m5C. В результате ее группа идентифицировала NSUN2, ALYREF, YBX1, YBX2 и SRSF2. Последние четыре считывают эту метку и играют роли в экспорте мРНК, стабилизации, фазовой сепарации и сплайсинге.
Оказалось, что они играют роли и при колите, раке мочевого пузыря, немелкоклеточном раке легких, раке молочной железы, сперматогенезе и лейкемогенезе.
Ранее было показано, что m5C чаще встречаются в стабильных РНК (тРНК, рРНК). Встал вопрос, есть ли эта модификация в мРНК? Если да, то какова ее функция?
Предыдущие технологии детектировали мало m5C или не детектировали ее вовсе в мРНК. Исследователи разработали и оптимизировали метод секвенирования для выявления этой модификации. Новый метод показал, что она встречается на мРНК часто, и в клетках HeLa, и в клетках рака мочевого пузыря, и в рыбках данио.
NSUN2 — важная m5C-метилтрансфераза для мРНК. NSUN2 много в иммунной системе, особенно в TH17 клетках. Делеция NSUN2 подавляет дифференциацию этих клеток. NSUN2 взаимодействуют с факторами транскрипции для поддержания стабильности специфичных для TH17 транскриптов.
YBX1 «считывает» метку m5C. Были проведены структурные исследования этого фермента. Оказалось, что, когда YBX1 связывает m5C, он рекрутирует другой стабилизирующий фактор — ELAVL1.
NSUN2 и YBX1 на высоком уровне экспрессируются в опухолях мочевого пузыря и связаны с плохим прогнозом. Модификация в том числе стабилизирует мРНК HDGF и других онкогенов. Также группа докладчицы с коллегами из Бельгии идентифицировала SRSF2, «читающий» m5C. Некоторые мутации в SRSF2 связаны с плохим прогнозом при остром миелоидном лейкозе. При немелкоклеточном раке легких уровни экспрессии таких белков, как NSUN2 и YBX1, влияют на чувствительность к терапии.
YBX2 — новый m5C-связывающий белок. При нокауте YBX2 исчезают зрелые сперматозоиды и активируется апоптоз. Идет изучение его функций.
Доклад «Анализ метилирования ДНК плазмы крови для ранней диагностики колоректального рака и предраковых состояний» прочитала Виктория Боробова, ООО «Биолинк».
Колоректальный рак является одной из основных причин смерти от онкологических заболеваний. В России регистрируется около 80 тысяч новых случаев ежегодно, причем процент смертельных случаев в первый год после постановки диагноза крайне высок. Отчасти это связано с тем, что большинство случаев диагностируются на поздних стадиях. В связи с этим актуально внедрение новых опций скрининга, которые, благодаря детекции ранних стадий, смогли бы снизить смертность от данного заболевания, а благодаря детекции предраковых состояний — также число новых случаев.
В данный момент в России охват скрининговой программы — только около 8%, что очень мало. Внедрение тестов анализа крови для диагностики колоректального рака могло бы существенно повысить охват программы скрининга популяции.
Для того, чтобы создать такую опцию скрининга, компания по литературным данным выбрала маркеры метилирования ДНК — SEPT9 и SDC2.
SEPT9 уже давно хорошо изучен и одобрен FDA еще в 2014 году в составе тестов. Однако множественные клинические испытания говорят о том, что он обладает довольно низкой чувствительностью к ранним стадиям и в отношении к прогрессивным аденомам.
Поэтому был выбран еще один маркер — SDC2. Он также довольно хорошо изучен, показано, что он обладает высокой чувствительностью к прогрессивным аденомам. Его чувствительность не зависит от стадии. По-видимому, это связано с тем, что активация этого гена происходит рано в процессе канцерогенеза.
В рамках исследования у пациентов, которые были направлены на колоноскопию, был взят анализ крови. Всего собрали 253 образца, из которых 18 оказались онкологическими. Также собрали 14 образцов прогрессивных аденом и других колоректальных образований (зубчатые поражения и непрогрессивные аденомы).
Оказалось, что, как и было продемонстрировано ранее, маркер SEPT9 дискриминирует онкологические образцы от всех остальных, а SDC2 может также дифференцировать и предраковые состояния, однако специфичность у него ниже. При объединении двух маркеров в одну систему удалось выявить все образцы колоректального рака.
Чувствительность к прогрессивным колоректальным образованиям составила 86%, и основной вклад в обнаружение предракового состояний внес SDC2. Специфичность составила 94%, что соответствует требованиям к скрининговым методам.
Доклад «Сравнение методов оценки копийности генов на примере образцов серозной карциномы яичников» прочитал Павел Гребнев, Институт синтетической биологии и генной инженерии ФГБУ «ЦСП» ФМБА России.
Изменение числа копий генов (CNV) — это довольно значимый драйвер канцерогенеза. Эти изменения влияют на устойчивость пациентов к терапии, а также могут являться новыми маркерами диагностики и прогностическими маркерами. Несмотря на то, что CNV встречаются значительно реже, чем изменения экспрессии генов, они гораздо более стабильны, и поэтому представляют из себя большой интерес для современной молекулярной онкологии.
Также очень важно изучать эти изменения копийности в образцах серозной карциномы яичников, поскольку этот тип опухоли несет очень высокую нагрузку CNV.
Существует множество методов детекции CNV, однако их результаты не всегда коррелируют друг с другом. Целью исследования было провести прямое сравнение трех различных методов детекции CNV, оценить их корреляцию и сделать выводы о наиболее применимых подходах к оценке этих изменений.
Группа докладчика исследовала 12 парных образцов, это опухолевая и нормальная ткани яичников от пациенток с серозной карциномой. Для исследования применяли три лабораторных метода: микрочипы Illumina CoreExome, таргетная панель NanoString nCounter CNV и цифровая капельная ПЦР, которая применялась для валидации первых двух методов.
Микрочипы и таргетная панель представляют из себя гибридизационные методы, то есть для того, чтобы оценить участок генома, его копийность и мутации в нем, используются комплементарные зонды. Для микрочипов эти зонды изначально закреплены на подложке и ловят необходимый участок, а для таргетной панели зонд сначала связывается с ДНК, а потом уже осаждается.
Наилучшие совпадения наблюдалось для методов микрочипов и цифровой ПЦР. По результатам работы была определена группа из семи генов, для которых согласованность между всеми тремя методами была самая высокая. Все эти гены являются известными онкогенами.
Тем не менее, ни один метод сам по себе не является достаточно надежным для того, чтобы однозначно определить изменение копийности в образце, тем более в образце от человека, а не в клеточной линии. Предпочтительно сочетание методов, таких, например, как полногеномное секвенирование или микрочипы для широкого поиска плюс верификация точечными методами, такими как количественная ПЦР.
Информация о докладчиках:
Евгений Наумович Имянитов, чл.-корр. РАН, д.м.н., Заведующий научным отделом биологии опухолевого роста Федерального государственного бюджетного учреждения «Национальный медицинский исследовательский центр онкологии имени Н.Н. Петрова» Министерства здравоохранения Российской Федерации.
Максим Леонидович Филипенко, д.б.н., заведующий лаборатории фармакогеномики ФГБУН ИХБФМ СО РАН, г. Новосибирск, заместитель директора Института репродуктивной генетики ФГБУ «НМИЦ АГИ им. В.И. Кулакова» МЗ РФ, Москва
Ирина Анатольевна Демидова, к.м.н. ГБУЗ «МГОБ № 62 ДЗМ» г. Москвы
Людмила Николаевна Любченко, д.м.н. ФГБУ «НМИЦ Радиологии» МЗ РФ, г. Москва
Евгения Викторовна Кайгородова, д.м.н., доцент НИИ онкологии Томского НИМЦ; ФГБОУ ВО СибГМУ Минздрава России, г. Томск
Виктория Сергеевна Боробова, ООО «Биолинк», г. Новосибирск
Ying Yang, Dr. China National Center for Bioinformation; Beijing Institute of Genomics, Chinese Academy of Sciences, China
Павел Алексеевич Гребнев, Институт синтетической биологии и генной инженерии ФГБУ «ЦСП» ФМБА России, г. Москва


 Меню
Меню





 Все темы
Все темы



 0
0












