МД-2025: Молекулярные методы в криминалистике
Возможно ли установление биологического родства при исследовании объектов, содержащих ДНК двух или более лиц? С чем можно перепутать митохондриальную ДНК другого индивида в образце? Можно ли на основе генетического анализа вычислить фамилию человека и нарисовать портрет? В чем особенности создания референтных баз данных для мегаполисов? Пригодны ли гистологические препараты для проведения генетического исследования? Эти и другие вопросы эксперты обсудили на секции, посвященной криминалистике, в рамках конференции «Молекулярная диагностика 2025».

Алексей Культин, Экспертно-криминалистический центр МВД России, прочитал доклад на тему «Опыт применения результатов исследования "смешанного" объекта в экспертизе по установлению биологического родства».
В рамках доклада рассматривалось уголовное дело, связанное с изнасилованием несовершеннолетней, в результате которого наступила беременность. Был произведен аборт и получен биологический материал плода. Кроме этого, на экспертизу были предоставлены образцы буккального эпителия потерпевшей и подозреваемого. Задачей исследования было определение биологического родства между плодом и предполагаемым отцом.
Однако не удалось получить чистый профиль плода, он был «смешанным». Повторные попытки также не позволили прийти к изолированному образцу.
Распространено мнение о невозможности установления биологического родства при исследовании объектов, содержащих ДНК двух или более лиц. Целью работы являлся поиск достоверного решения экспертной задачи по установлению биологического родства между одним из лиц, образующих этот «смешанный» объект, и предполагаемым отцом.
Оказалось, что достоверно установить полный генотип ребенка не представляется возможным. Но нужно ли это для проведения экспертизы и для принятия решения о родстве?
Используемая в экспертной практике оценка для случая «предполагаемый отец-ребенок-априорная мать» заключается в оценке величины вероятности события: генетические признаки предполагаемого отца случайно совпадают с конкретными отцовскими аллелями ребенка, которые устанавливаются с помощью априорной матери. Чем меньше величина этой вероятности случайного совпадения, тем меньше вероятность того, что предполагаемый отец является случайным лицом.
Если отцовский аллель — «a», а ребенок гетерозиготный и совпадает с матерью по одному аллелю, то вероятность будет складываться из вероятностей отдельных генотипов, обладающих этим аллелем. Основная формула установления родства: P = pa(2 - pa). Аналогичная ситуация в случае, если ребенок гомозиготный.
Последняя комбинация — когда ребенок гетерозиготный и полностью совпадает с матерью. В этом случае нельзя определить, какой аллель отцовский. Тогда допускается возможность и того, и другого аллеля: P = pa(2 – pa) + pb(2 – pb) – 2papb.
По сути, генотип ребенка не нужен, нужен отцовский аллель. И если установить генотип ребенка не удалось, то установить отцовский аллели возможно.
Предполагаемый отец обладал подобными аллелями.
Такое сравнение не всегда возможно. Если мать гетерозиготная, и смесь плода с матерью также формирует двухаллельный профиль, какие же аллели тогда отцовские? И тот, и другой вариант допустим. Можно оценить так называемый показатель гетерозиготного баланса. Но оказалось, что в 17-м аллеле у отца, вероятно, находится мутация.
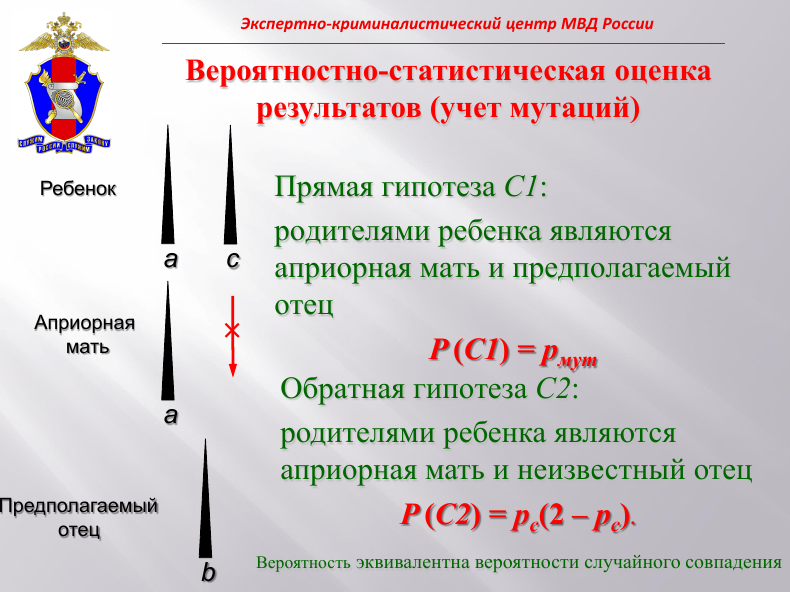
Тогда стандартный расчет вероятности случайного совпадения становится недопустимым. Нужно использовать отношение правдоподобия двух альтернативных событий, двух гипотез, объясняющих происхождение ребенка. Прямая гипотеза: родителями является априорная мать и предполагаемый отец. Тогда вероятность соответствия этой гипотезе будет равняться вероятности или частоте встречаемости мутации в данном локусе. Обратная гипотез: родителями ребенка являются априорной мать и неизвестный отец. Формула, по сути, эквивалентна вероятности случайного совпадения. И так по всем локусам.
В результате всех расчетов получилось значение отношения правдоподобия 3,69 * 1011. Это позволяет сформулировать положительный экспертный вывод об отцовстве подозреваемого по отношению к плоду в категоричной форме.
Таким образом, предложенный алгоритм, не выходя за пределы обычной методики, позволил сделать достоверное исследование «смешанного» объекта, что способствовало раскрытию тяжкого преступления.
Продолжила секцию с докладом «Инсерции фрагментов митохондриальной ДНК в ядерный геном» Мария Голубенко, к.б.н., НИИ медицинской генетики ТНИМЦ.
NUMTS — Nuclear MiTochondrial DNA Sequences — это фрагменты митохондриальной ДНК, которые встроены в ядерный геном человека. В геноме они не активны, это псевдогены. Причем это не те гены, которые миллиарды лет назад от предков митохондрии переселились в ядро; этот процесс давно уже закончен. А образование NUMTS — продолжающийся процесс, такие вставки, инсерции происходят с определенной частотой и сегодня.
В 2011 году насчитали 766 NUMTS в референсной последовательности, которые составляли 0,02% генома человека.
Получается, что митохондриальная ДНК представлена не только в митохондриях, гомологичные ей последовательности многократно представлены в ядерном геноме. В определенных условиях это может вносить определенный шум в исследования, которые проводятся на митохондриальной ДНК (мтДНК), например, они добавляют лишние копии к числу мтДНК.
Сходство последовательностей с референсной последовательностью мтДНК варьируют от 63 до 100%. То есть более давние вставки эволюционировали отдельно, их уже можно отсеять. Но если они произошли недавно, то гомология может достигать 100%.
Практически все исследования показывают, что эти фрагменты мтДНК встраиваются в ядерный геном в процессе негомологичного соединения концов при репарации двунитевых разрывов ДНК в ядре.
Мало того, что NUMTS существуют в референсной последовательности, они еще и полиморфны. Анализ проекта «1000 геномов» показал, что большинство этих вставок произошло в течение последнего миллиона лет.
Каждый из нас имеет в среднем полтора NUMTS, не входящего в референсную последовательность генома человека.
К счастью, большая часть инсерций NUMTS расположена в интронных и межгенных областях. В более современных исследованиях было показано, что у одного из восьми человек есть ультраредкий NUMTS. Примерно один из 10 000 новорожденных имеет какую-то новую вставку фрагмента мтДНК в свой геном. А что касается опухолей, то из-за нестабильности генома там частота выше в десять раз.
Есть крупные и небольшие NUMTS, но большинство из них попадает в диапазон до 250 пар нуклеотидов. Для изучения мтДНК как раз используют ПЦР примерно на всю эту длину. Особенно если образец деградировал, там можно амплифицировать только короткие фрагменты.
Чем могут мешать NUMTS при анализе мтДНК, не только в криминалистике, но и в исследованиях?
Это, во-первых, оценка гетероплазмии. Если ядерная вставка чем-то отличается, то она коамплифицируется с мтДНК, и мы увидим ложную гетероплазмию.
Во-вторых, это оценка уровня метилирования. В некоторых исследованиях было показано метилирование мтДНК на уровне 60–70%, другие говорят, что 0–2%. По мнению докладчицы, это может быть связано с тем, что в ядре NUMTS — это псевдогены, и они могут быть метилированы.
В-третьих, оценка числа копий мтДНК. И, в-четвертых, ДНК-идентификация (дополнительная гетероплазмия, «отцовское» наследование).
Таким образом, чем короче фрагменты, получаемые при обогащении образца с помощью ПЦР или гибридизации со специфичными пробами, тем выше вероятность «контаминации» ядерными псевдогенами.
Однако использование длинных ПЦР-продуктов также не дает 100% гарантию того, что в анализируемом образце не будет NUMTS.
В 2018 году появилась статья, в которой было описано отцовское наследование мтДНК. Авторы при анализе семей обнаружили гетероплазмию мтДНК в трех независимых родословных, в которых на протяжении двух-трех поколений мтДНК передавалась от отца к детям.
Но, возможно, эта ДНК передавалась на хромосомах.
В 2020 году другие авторы, изучая трио, с помощью длинных ридов нашли, что это так называемые конкатенаты. Это редкий случай, когда несколько молекул мтДНК линеаризуются и встраиваются одна за другой в геном, и в результате ребенок оказывается носителем нескольких геномов мтДНК отца.
Таким образом, встроенные в ядерный геном фрагменты мтДНК (NUMTS) довольно распространены и являются значимыми факторами, вносящим «помехи» в результаты исследований мтДНК, так как могут гибридизоваться, амплифицироваться и секвенироваться вместе с митохондриальной ДНК. Это приводит к появлению ложных сайтов гетероплазмии, а в отдельных случаях — к имитации присутствия в исследуемом образце мтДНК другого индивида.
Николай Янковский, академик РАН, д.б.н., Институт общей генетики им. Н.И. Вавилова Российской академии наук (ИОГЕН РАН), прочитал доклад «ДНК-идентификация: индивид, семья, род, народ от деревни до мегаполиса».
ДНК-диагностическая панель по СтепОр каждого народа Союзного государства может по ДНК из биологического следа неизвестного индивида указать на его происхождение из определенного народа, рода, деревни, семьи и на историческую территорию обитания этого народа на географической карте.
Старт раскрытия преступления набором СтепОр укажет на тот единичный народ из 195 народов Союзного государства и его приграничья, из которого происходит искомое лицо, что на порядок сократит затраты средств, времени и повысит вероятность раскрытия преступлений по ФЗ-242 в рамках комплексного научно-технологического проекта Союзного государства с конкретным экономическим результатом (2025–2030).
Докладчик привел пример полученных его группой практических результатов. В Новосибирске серия изнасилований была совершена одним преступником. Согласно СтепОр, он был из Бурятии, за 2000 километров от Новосибирска. Бурятов в Новосибирске мало. Данного индивида искали десять лет, найти его не удавалось. А тут за пару недель удалось выйти на людей, которые знали его. Таким образом преступник был найден.
Более 2 млн преступлений регистрируется в РФ ежегодно. Пятая часть из них относится к категории тяжких и особо тяжких, 85% осужденных — мужчины. Затраты бюджета по каждому из таких преступлений — более 1 млн рублей (раскрытие, судебные и исправительные процедуры), поэтому возможность избежать нецелевых затрат очень важна.
Докладчик привел пример того, как ДНК-диагностика была использована для определения принадлежности неизвестного мужчины к охарактеризованным этно-территориальным группам (народам) Союзного государства. Были проведены мультиплексная амплификация 37 Y-STR СтепОр локусов и фрагментный анализ на Нанофор-5. Расчестное число сочетаний гаплотипов 37 Y-STR локусов превышает численность человечества.
Более 100 экспертиз успешно проведено по заказам управлений СК и МВД от Крыма до Владивостока (убийства, изнасилования, неопознанные останки).
Была проведена апробация набора из 37 STR-маркеров Y-хромосомы (Y-STR СтепОр) в Минске (Беларусь) Научно-практическим центром Государственного комитета судебных экспертиз РБ. Принадлежность по Y-STR СтепОр ДНК совпала с фактической для 23 из 25 образцов (92%) из Минской коллекции биобразцов с известной популяционной принадлежностью при интерпретации данных по программам анализа ДНК, созданным в Томске.
Предсказание для 15 образцов совпало с точностью до популяции, а для 8 образцов совпало с точностью до нескольких близких популяций, имеющихся в базе данных в Томске.
Необходимо определить порядок взаимодействия российской и белорусской сторон при использовании для интерпретации более полных баз данных, созданных по программе «ДНК-идентификация» в российской части программы.
При ДНК-диагностике близкородственных народов (белорусы, русские, украинцы) разрешающая способность СтепОн выше, чем у импортированного набора, но требуется дальнейшее увеличение разрешающей способности для близкородственных народов.
Доклад «Экспертиза без капилляров: нанопоры меняют правила» прочитал Максим Скалин, ООО ГОРДИЗ.
Сегодня основным стандартом в ДНК-идентификации является фрагментный анализ с капиллярным электрофорезом (CE). Этот метод определяет генотип опосредованно через длину ПЦР-продукта. Он внедрен в практику еще в 1995 году.
Это быстрый, недорогой метод, он технически отработан и стандартизирован. Но, как и любому другому методу, ему свойственны некоторые ограничения.
В первую очередь фрагментный анализ ограничен в плане информативности. В мультиплексах для капиллярных электрофорезов можно использовать лишь какое-то конечное количество маркеров, потому что есть ограничение по числу флуорофоров и диапазону длин фрагментов.
Также CE только ограниченно применяются для решения других задач в судебной генетике, помимо STR. Например, это мтДНК, SNP-панели, оценка возраста, видовая принадлежность, предсказание фенотипа, РНК.
Также известно, что эффективность амплификации связана с длиной образующихся ПЦР-продуктов. Чем длиннее ампликон, тем менее эффективно идет ПЦР. Возможно «выпадение» аллеля.
С помощью CE получают лишь условные генотипы, скорее даже фенотипы. Одной длине фрагмента может соответствовать несколько аллелей, эти варианты имеют разные популяционные частоты и разную информативность. Например, в случае с локусом SE33 CE выявляет лишь порядка четверти всех существующих аллелей в этом локусе.
Делеции/инсерции во фланкирующей области влияют на длину ПЦР-продукта.
Также невозможно полностью автоматизировать процесс анализа. Анализ фореграмм требует ручной амплификации. Эксперту постоянно нужно удалять артефакты, просматривать, насколько хорошо получилось исследование. И эксперт тратит свое рабочее время даже не на биологию, генетику или генотирование, а просто на преодоление технических несовершенств.
Еще одна проблема CE — это его относительно узкий динамический диапазон.
Но методы массового параллельного секвенирования (MPS) снимают эти ограничения и обладают рядом преимуществ.
Так, это универсальные методы, подходящие для любых исследований ДНК. Они обладают высокой чувствительностью и широким динамическим диапазоном, позволяют проводить максимально точное генотипирование и обладают широкими возможностями для полной автоматизации.
Им тоже свойственны недостатки: это большое капитальное вложение, длительный цикл анализа, (2–3 дня, что в случае с криминалистикой — очень большой срок), высокая стоимость результата и отсутствие стандартизации.
Однако за последние два года наметился большой прогресс в нанопоровой технологии. Так, появилась новая химия, появились ячейки с двойным сенсором, происходит непрерывное улучшение алгоритмов бэйсколлинга.
Благодаря этому становится меньше ошибок в повторах и коротких ридах. Созрела экосистема — опубликованы эффективные пайплайны для STR, SNP, mtDNS. Доступна отечественная платформа «Нанопорус».
Сможет ли нанопоровое секвенирование стать методом нового поколения для судебной практики?
Чтобы ответить на этот вопрос, нужно сформулировать три направления работы.
Первое направление — это исследование STR-маркеров, оценка конкордантности с CE, полноты профиля на деградированных образцах.
Второе направление работы — это полногеномное секвенирование мтДНК, оценка покрытия и уровня гетероплазмии.
И третье направление — это судебная генетика «в поле»: идентифицировать след, не покидая место преступления.
Был разработан мультиплекс из 24 мини-STR, которые включают в себя 20 стандартных CODIS-маркеров и 4 дополнительных маркера, также представляющих высокий интерес в криминалистике. Система разработана таким образом, что все ампликоны обладают короткой длиной,
И для всех STR-маркеров были получены однозначные генотипы и хорошие профили, полностью конкордантные результатам CE. Но интерпретация результатов SE33 была затруднена. Это связывают с тем, что SE33 обладает довольно сложной структурой.
Исследователи выбрали шесть костных образцов людей, погибших по время боевых действий (>80 лет назад). Метод Сэнгера результата не дал. Результат нанопорового секвенирования: полные последовательности мтДНК получены во всех шести случаях, установлены их гаплотиты.
Наконец, третье направление работы — это мобильность. Зачем нужна экспертиза «в поле»? Это может помочь в случае, если эксперт работает с результатами стихийных действия, массовых катастроф, в случае массовых захоронения и в отдаленных регионах.
Что это дает?
-
Сроки: предварительный результат за часы, а не дни.
-
Отбор на месте: выбор только информативных образцов.
-
Сохранность: меньше деградации и контаминации при транспортировках.
Любая ДНК-лаборатория обладает довольно объемной инфраструктурой. Может ли эксперт в поле обойтись без всего этого разнообразия прибора?
Оказывается, что может, если использовать специальные портативные приборы, например, Lampix или Termix. Lampix используется для обнаружения ДНК, Termix — миниатюрный амплификатор. И MinION для детекции получаемого результата.
Группой докладчика была создана и валидирована система Lampix для обнаружения ДНК человека и определения пола за 20 минут.
Флуоресцентная детекция в реальном времени и возможность измерения концентрации в режиме QUBIT, что необходимо для подготовки амплификационных библиотек перед секвенированием.
Может ли эксперт вообще обойтись без оборудования?
Может, если использовать Recombinase Polymerase Amplification (RPA). Эта изотермическая амплификация, которая протекает при температуре 37–40 градусов, то есть для нее даже не требуется термостат. Реакция протекает довольно быстро (10 минут), обладает неплохой чувствительностью (0,1 нг).
Можно полностью амплифицировать митохондриальный геном, STR-маркеры (без стартеров), что может быть полезно и интересно для анализа «смешанных» образцов.
Полученный результат можно протестировать либо на MinION, либо на обычном CE.
-
Таким образом, пилотные эксперименты подтверждают перспективность технологии для экспертной практики: получены полные профили из старых останков. Планируется расширенная валидация.
-
Нанопоровое секвенирование доступно для внедрения в любую лабораторию.
-
Лаборатория получает инструмент с преимуществами MPS, отвечающий требованиям к современным экспертным методам: доступность, результат «за один день», анализ в реальном времени и портативность.
-
Метод позволяет создавать готовые экспертные инструменты «из коробки».
-
Нанопоровое секвенирование уже сегодня готово стать для криминалистики платформой нового поколения.
С докладом «Особенности создания референтных баз данных для маркеров Y-хромосомы, мтДНК и аутосомных Str для мегаполисов с учетом динамики генофонда населения под действием миграции» выступила Ирина Удина, д.б.н., Институт общей генетики им. Н.И. Вавилова Российской академии наук (ИОГЕН РАН).
Референтная база данных (РБД) — это коллекция ДНК-профилей или генотипов по ДНК-маркерам, используемых в судебно-медицинской экспертизе, полученных от известных индивидов в популяции, которая служит эталоном для статистической оценки.
Цель создания РБД — ответить на вопрос, какова вероятность случайного совпадения найденного на месте преступления ДНК-профиля с профилем (генотипом) конкретного человека в популяции.
В качестве генетических маркеров, которые используются в создании таких баз, выступают аутосомные STR-локусы — короткие повторяющиеся последовательности ДНК, высокополиморфные и стабильные.
Для возможности межлабораторного обмена данными набор маркеров должен быть совместим с международными стандартами.
Также используются дополнительные системы для более узких задач. В частности, Y-STR для анализа мужской линии, мтДНК для анализа сильно деградированной ДНК или родства по материнской линии и SNP для прогнозирования внешности, происхождения и анализа сложных образцов.
Базы данных по ДНК-маркерам необходимы для судебной экспертизы в криминалистике, для установления родства по мужской и женской линиям, для ДНК-идентификации жертв террористических атак, техногенных катастроф, погибших на войне, потерянных людей, а также для проведения исторических идентификаций.
РБД эквивалентна репрезентативной популяционной базе данных по судебным ДНК-маркерам, отражающей генетическое разнообразие популяции. Для нее должна быть характерна репрезентативность, то есть она должна отражать этническую/географическую структуру населения, для которого будет применяться, и достаточно большой размер (обычно несколько сотен или тысяч индивидов на каждую популяционную группу), чтобы обеспечить статистическую значимость. Но иногда статистическая значимость достигается при меньших размерах выборки.
Разработка РБД для ДНК-идентификации — это сложный, многоэтапный процесс, лежащий на стыке генетики, статистики, криминалистики и права. Корректно разработанная РБД является мощнейшим инструментом правосудия, так как позволяет объективно оценивать весомость генетических улик.
Популяционная генетика: использование «неправильной» популяционной базы может привести к значительным ошибкам в расчетах. Например, использование европейской популяции для оценки доказательств по делу с участием человека из другого региона мира недопустимо.
РБД: Рассчитываются частоты каждого аллеля и генотипа для всех STR-локусов каждой популяционной группе. Статистические параметры: частота генотипа, вероятность совпадений (match probability) и отношение правдоподобия LR (likelihood ratio).
Дальше речь шла о выборках из мегаполиса. Мегаполисы представляют специфический новый в историко-эволюционном плане тип популяционной структуры, для которого все еще не разработаны адекватные модели и методы изучения. Основные черты мегаполиса: большой объем населения, полиэтничность, высокий процент межэтнических браков, высокий уровень миграции, территориальная подразделенность населения, воспроизводство населения за счет внешней миграции.
В настоящее время на территория России 16 мегаполисов. В них проживает около 30% всего городского населения страны и почти 24% всех россиян.
Ведущим фактором популяционной динамики мегаполиса является центростремительная миграция.
Исследования в основном проведены в рамках уже принятой на сегодня программы «ДНК-идентификация» СГ и в рамках Мероприятия 10. Также частично исследования продолжались уже в рамках Темы государственного задания ИОГен РАН
В рамках исследования была изучена этническая топография Москвы, Санкт-Петербурга и Новосибирска.
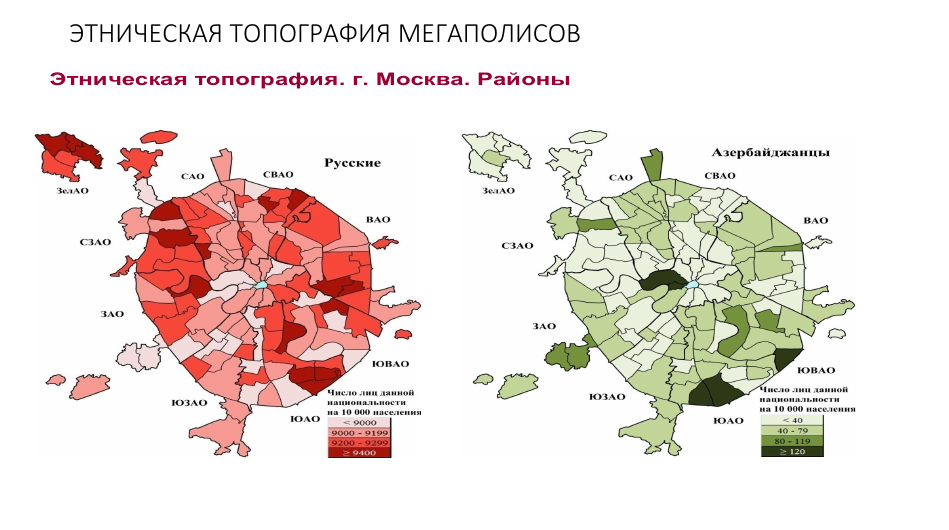
В мегаполисах особенно важна проблема ДНК-идентификации личности для обеспечения безопасности мегаполисов, так как они являются не только центрами политической, экономической и культурной жизни страны, но и криминогенных и техногенных угроз.
Содержание РБД, адекватно отражающих генетическое разнообразие населения, является ключевой задачей для практики судебно-генетической экспертизы. Крупные мегаполисы — центры миграционного притяжения — характеризуются сложной и динамической генетической структурой.
Группа докладчика изучала большие выборки, которые представляют три поколения Москвы: «старшее», «среднее» и «младшее», выборки из Санкт-Петербурга и Новосибирска.
Целью исследования, помимо получения генетико-демографических характеристик для мегаполисов, было изучение профиля частот 18 STR-гаплотипов и гаплогрупп Y-хромосомы, секвенирование ГВСI и ГВСII с последующим определением принадлежности к гаплогруппе мтДНК в трех мегаполисах, а также определение вариабельности 27 аутосомных неCODIS STR в «старшем» и «младшем» поколении населения Москвы в связи с проблемой создания референтных баз с учетом миграционных процессов.
Возраст «старшей» группы из Москвы близок к выборке из Новосибирска – это люди, рожденные до распада Советского Союза, до начала современной интенсивной миграции из регионов Северного Кавказа и Средней Азии.
«Младшая» группа из Москвы родилась уже практически спустя поколение после распада Советского Союза.
По данной переписи населения 2002-го и 2010-го, представители «младшей» группы реже рождались в самой Москве, чем представители «старшей» группы. В Москве и Санкт-Петербурге проживают три четверти уроженцев Центрального федерального округа и Северо-Западного федерального округа соответственно, в Новосибирске — три четверти уроженцев Новосибирска и области и свыше 90% уроженцев Сибирского федерального округа.
Также определили коэффициенты миграции. Самый высокий коэффициент характерен для «младшей» группы Москвы.
Исследователи генотипировали 18 STR-локусов Y-хромосомы по базе ООО «Гордиз» с помощью мультиплексной ПЦР с применением флуоресцентно-меченных праймеров. Аналогично изучено 27 аутосомных STR.
Было проведено определение гаплогрупп Y-хромосомы на основе 18 STR-генотипов.
Для STR Y-хромосомы и 27 аутосомных не входящих в CODIS STR изучены распределения частот аллелей STR-локусов и гаплогрупп, определен уровень генетической дифференциации для изученных выборок. Для гаплогрупп мтДНК рассчитаны частоты и определены оценки Fst. Для аутосомных STR посчитаны идентификационные параметры.
Оценили долю «южных по происхождению» гаплогрупп Y-хромосомы в изученных выборках, а также представленность восточноевразийских и западноевразийских гаплогрупп мтДНК в трех поколениях населения Москвы.

Для изученных 27 STR-локусов выявлено 267 аллелей, что подтверждает высокий уровень генетического разнообразия среди жителей мегаполиса.
Вероятность случайного совпадения двух генотипов по всем 27 STR-локусам в населении Москвы исчезающе мала (2,00024-30), что позволяет рекомендовать данный набор в качестве набора STR-локусов дляДНК-идентификации жителей мегаполиса при проведении судебных экспертиз.
С докладом «Получение поисковой информации из биологических следов с места происшествия» выступила Марина Чухряева, к.б.н., ФГКУ «Судебно-экспертный центр Следственного комитета Российской Федерации».
Идеальной является ситуация, когда с места происшествия получены вещественные доказательства, в лаборатории установлен из них аутосомный ДНК-профиль предполагаемого преступника, и он совпадает с предоставляемыми образцами либо с базой данных.
Увы, такая ситуация бывает не всегда, и тогда на помощь следователем приходит поисковая информация. Это любая информация, получаемая из ДНК, которая может помочь в расследовании преступлений: этногеографическое происхождение, возможные характеристики внешности, цвет волос, глаз, кожи, черты лица, биологический возраст, наследственные болезни и некоторые другие характеристики внешности.
Возможно ли уже сейчас надежно воспроизвести черты лица и по ДНК получить портрет человека? Ученые склоняются ко мнению, что пока это сделать невозможно.
С какой же тогда поисковой информацией можно сейчас работать в российских реалиях?
Это цвет глаз, цвет кожи, цвет волос и этническое происхождение. Во всём мире эти четыре характеристики уже используются в реальной судебной практике. Группа докладчицы также работала именно с ними.
Для определения цвета волос, кожи, глаз апробировали систему «Phenotype expert», которая является разработкой российских исследователей.
Она позволяет идентифицировать 60 коротких генетических детерминант, для которых установлена ассоциация с цветом глаз, волос, кожи, группой крови, базовой гаплогруппой Y-хромосомы и половой принадлежностью. И уже с помощью поставляемого программного обеспечения эти данные позволяют прогнозировать фенотип объекта по указанным параметрам.
Тест-система определяет цвет глаз в трех градациях: карий, серый/голубой и смешанный, цвет волос — в восьми градациях, цвет кожи — в пяти градациях.
Апробация этого программного обеспечения сначала проводилось на базе разработчика. Группа докладчицы предоставила биологические образцы, характеристики внешности, которые были известны им, но не были известны разработчику. Всё было определенно правильно, только для одного из образцов были различия в цвете волос.
Затем уже группа докладчицы проводила апробацию в своём отделе. Каждый образец ставили независимо в трёх повторностях и всегда получали полностью воспроизводимые результаты, что указывает на надёжность системы. Также было показано соответствие для всех, кроме одного образца, у которого выявлено отличие в цвете глаз.
Есть сложности с определением «промежуточных» оттенков, например, зелёного цвета глаз, а также сложности с определением цветов самими следователями/экспертами. Нужно проводить дополнительную работу, объяснять следователям, насколько надёжны получаемые результаты. Также следы должны быть чистыми для получения подобной информации.
Система для у установления этногеографического происхождения по маркерам Y-хромосомы в настоящее время используется в СЭЦ СК России.
Какая информация содержится в предоставляемой справке?
Принадлежность к гаплогруппе на основе предикции, описание и карта распространения данной гаплогруппы, национальность лиц, с которыми обнаружено совпадение, вывод о наиболее вероятном этническом происхождении. Эта информация носит вероятность на характер.
Какие ограничения существуют у этого метода?
Во-первых, метод работает только для лиц мужского пола, происхождение по мужской линии может не отражать сходство с внешностью представителей определенной национальности и не дает точной информации о происхождении индивида.
Есть очень широко распространенные гаплотипы, а есть редкие, по ним невозможно надежно определить происхождение.
Как можно использовать поисковую информацию?
Для сужения круга подозреваемых лиц, для предоставления и опровержения следственных версий и для грамотной организации скрининга биологических образцов.
Светлана Игнатова, Дальневосточный филиал ФГКУ СЭЦ СК России, выступила с докладом «Установление видовой принадлежности дериватов осетровых (Acipenseridae) в интересах судебной экспертизы. Проблема идентификации продукции, полученной от гибридных особей».
В Дальневосточном федеральном округе в р. Амур обитают два вида осетровых: амурский осетр и калуга, вылов которых запрещен. Установление видовой принадлежности целых рыб не составляет труда для специалиста-ихтиолога. В случае же, когда изымается продукция (мясо, икра), необходимы более наукоемкие методы — определение видоспецифичных веществ (белков), либо молекулярно-генетические исследования.
Пробоотбор осуществляется следователем либо самостоятельно, либо с участием специалиста, согласно разработанным совместно с ВНИРО и ГУКом Методологическим требованиям. Из изъятой партии производится статистически репрезентативная выборка. Например, от из партии от 11 до 100 шт. отбирается 10 шт., от 10 001 до 100 000 — 50.
Выделение ДНК производилось с помощью набора реагентов производства ООО «Синтол». Для определения видовой принадлежности применен метод, основанный на анализе продуктов ПЦР, проводимой с использованием видоспецифичных праймеров к контрольным регионам мтДНК осетровых рыб (COrDIS SturGENE NIT).
Для определения происхождения от конкретных особей рыб и выявления особей гибридного происхождения применен метод, основанный на анализе продуктов ПЦР, проводимой с использованием праймеров к микросателитным локусам аутосомной ДНК осетровых рыб (COrDIS SturGENE STR).
Видовая принадлежность устанавливается исследованием мтДНК согласно длинам видоспецифичных контрольных регионов мтДНК. У каждого вида есть своя длина продукта реакции. В результате получалось три возможных результата: амурский осетр, калуга и смешанный профиль. В большинстве случаев для следствия этого достаточно.
В случае же необходимости установить, произошли ли данные продукты от одной либо нескольких особей (для расчета ущерба), производится исследование по STR-маркерам.
Гибриды калуги и амурского осетра не являются охраняемым видом. Строго говоря, они вообще не являются самостоятельным видом и могут предоставлять опасность для охраняемых видов. Решение вопроса о принадлежности деривативов гибридным особям на текущий момент вызывает сложности и требует совершенствования методик исследования.
Доклад «Современные возможности применения массового параллельного секвенирования для решения криминалистических задач» прочитала Анна Субботовская, к.м.н., ФИЦ ФТМ.
В лабораторию на базе Федерального исследовательского центра фундаментальной и трансляционной медицины обратились с вопросом, возможно ли проведение идентификации останков погибших на СВО. Проект стартовал в апреле 2025 года на базе действующей молекулярно-генетической лаборатории.
Каким образом организован технологический процесс?
Идет регистрация биоматериала с использованием ЛИС 1С. Клиническая лаборатория. Каждый образец штрихкодируется индивидуальным номером, который не повторяется. Все образцы маркируются индивидуальным QR-кодом.
Есть зоны подготовки костного материала, выделения, амплификации ДНК и разделения продуктов амплификации.
Почему используется штрихкодирование?
Потому что маркировка материала происходит практически на каждом этапе, и на каждом этапе может возникнуть ошибка. Соответственно, использование штрихкодов количество ошибок снижает. Имея на каждом конверте и на каждой пробирке уникальный QR-код, можно проследить, на каком этапе находится исследование данного биоматериала. Можно использовать различные устройства, сканеры и электронную базу данных. Все это приводит к тому, что можно обрабатывать большее количество образцов в единицу времени и длительно хранить образцы.
Как устроен процесс штрихкодирования?
Сначала происходит регистрация биоматериала и присваивание штрихкода. Далее распечатываются четыре экземпляра уникальной этикетки. Одну этикетку помещают на документацию, сканированный вариант этого документа тоже хранится в системе.
Еще одна этикетка маркирует сам конверт с биоматериалом и две пробирки. Этикетки очень маленькие, они устойчивы к спиртам и к нагреванию. В конце этого процесса происходит так называемая комплектация пакета с биоматериалом. Он содержит первичный биоматериал и две маркированные пробирки Эппендорф. Дальше в таком виде он перемещается в зону подготовки костного материала.
Костный порошок получают спиливанием. Он летучий, соответственно, может перемещаться и контаминировать пробу. За одну смену один человек готовит от 80 до 120 образцов.
Чтобы избежать контаминации, все работы проводят в ламинарном шкафу. Для каждого образца используется индивидуальная укладка, которая содержит перчатки, салфетку, керамическую фрезу, ветошь, силиконизированную бумагу и чашку Петри.
В ламинар одновременно допускается заносить только один пакет с биоматериалом. При вскрытии пакета с биоматериалом оператор, который проводит спил, обязательно сверяет маркировку пакета с этикетками на вложенных пробирках. После спила оператор пересыпает порошок в две пробирки. Первый образец используется, а второй — резервный.
В лаборатории используется так называемый слотовый режим работы, то есть выделены временные слоты для работы с материалом. Материал поступает непосредственно в тех же пробирках, в которых оператор из зоны подготовки разместил костный порошок, далее происходит ночной лизис. После этого пробирки центрифугируются, ДНК выделяется на автоматической станции. Одновременно выделяется 92 образца. За одну смену можно выделить на одной станции порядка 5–6 планшетов. Далее в этот же день производится количественная оценка ДНК, нормализация и амплификация. Уже к вечеру продукты ставятся на электрофорез, за ночь происходит разделение продуктов ПЦР.
Таким образом можно разогнать четыре 96-луночных планшета в течение дня. Анализ данных проводится стандартно в специализированном ПО для точной интерпретации результатов.
Таким образом, сейчас пропускная способность 2500 образцов в неделю; примерно трое суток занимает обработка одного результата; 80% идентифицированных образцов.
Такой высокой производительности удалось достичь за счет автоматизации, использования штрихкодирования, оптимизации протоколов, высокой пропускной способности и опытному персоналу.
Но какие проблемы остаются?
Это деградация ДНК, достаточно низкое количество ДНК в некоторых образцах, контаминация и ингибиторы ПЦР. Эти задачи как раз и может помочь решить применение высокопроизводительного секвенирования.
Таким образом, есть часть образцов, которые не идентифицированы, есть «смешанные» образцы, которые могут быть отправлены для дальнейшего тестирования именно методом NGS. Возможно, удастся получить профили и идентифицировать погибших.
Результаты, полученные методом NGS, — это большие массивы данных. Для того, чтобы их достаточно быстро анализировать, понадобятся какие-то разработки на основе машинного обучения и искусственного интеллекта. На текущий момент NGS где-то на порядок дороже, чем капиллярный форез. Но, вероятно, NGS войдет в будущем в криминалистику достаточно плотно.
Доклад «Гистологический архив при проведении судебно-генетических экспертиз. Сложно, но можно» прочитала Светлана Алпатова, ГБУЗ ПК «Краевое бюро судебно-медицинской экспертизы и патологоанатомических исследований» (Соавтор: Лесникова О.А.).
В судебно-медицинской практике имеют место случаи, когда объектами исследования и сравнения служат фиксированные ткани, так называемые гистологические архивы. Это «влажные» архивы, то есть препараты, фиксированные в формалине и хранящиеся в нем в течение года, парафиновые блоки и гистологические препараты на стеклах.
Необходимость исследования данных объектов возникает:
-
в уголовных делах, если фигуранты дела умерли, и есть необходимость идентификации их со следами с места преступления;
-
в гражданском судопроизводстве при установлении факта родственных отношений с умершим, если это не было установлено прижизненно, а другие возможные варианты установления родства отсутствуют;
-
когда после проведенных хирургических вмешательств или биопсии возникают сомнения в принадлежности объекта конкретному лицу или правильности постановки диагноза, а также в случаях обращения страховых компаний.
Причины невозможности установления генетического профиля объекта, указанные в тексте судебных актов:
-
деградация ДНК вследствие нарушения технологии заливки биологического материала в парафин и (или) ингибирования реакции амплификации ввиду разрушающего воздействия на ДНК различных факторов окружающей среды в период до назначения экспертизы;
-
деградация ДНК в тканях под действием воздействия внешних факторов (в том числе фиксации в формалине);
-
отсутствие оборудования для проведения СГЭ конкретной экспертной организацией и высокой степенью деградации исходного биологического материала (однако другой экспертной организации по этому же делу удалось установить отцовство умершего в отношении ребенка по тому же биологическому материалу).
Есть пять этапов приготовления гистологического препарата: фиксация, проводка, заливка, микротомирование и окрашивание.
Наиболее критичным является первый этап — фиксация, когда используются жидкости-фиксаторы для обработки тканей. Ткани, фиксированные в 10% забуфернном формалине, этаноле, ацетоне и залитые в парафин, пригодны для ПЦР. При использовании фиксаторов Кларка и Замбони, параформальдегида, формалина/этанола/уксусной кислоты результат возможен. Не пригодны для ПЦР ткани, обработанные фиксаторами Зенкера, Карнауа, Буэна.
Когда ткани содержатся в фиксаторе более 1–3 суток, происходит ее необратимое изменение, образуются ошибки в основании, которые препятствуют амплификации. После заливки ткани в парафин стабильность ДНК повышается, однако вследствие ее продолжающейся медленной деградации в очень старых (более 10 лет) парафиновых блоках эффективность амплификации снижается.
Следует помнить, что гистологические препараты изготавливают для проведения других видов СМЭ, для генетического исследования они «условно пригодны».
Еще был сделан запрос в Министерство Здравоохранения Российской Федерации с целью разъяснения. Был получен ответ, что конкретные условия транспортировки парафиновых блоков с фрагментами ДНК и РНК, направляемых из морга медицинской организации через суд, назначивший судебно-медицинскую экспертизу, в судебно-экспертную организацию, осуществляющую проведение генетической экспертизы, не определены.
В отделении генетической экспертизы ГБУЗ ПК «КБСМЭПАИ» производится такая экспертиза, процент положительных результатов — 73%. В 38 парафиновых блоках получили положительные результаты, в 9 результат не был получен. Гистологические препараты, которые предоставляют на стеклах, тоже исследуются. В 5 был получен результат, в 1 — нет. А во «влажном» архиве результат был получен один раз, в 2 случаях — нет.
Трудности: малое количество выделенной ДНК, контаминация посторонней или «свежей» ДНК, неспецифическая амплификация, ингибиторы ПЦР и деградация.
Факторы, влияющие на ДНК: длительность нахождения ткани в реактиве, температура, УФ-лучи, влажность, время, кислород, инвазия бактерий.
По наблюдениям, сделанным в лаборатории, положительные результаты были получены при исследовании:
-
препаратов от трупов, исследованных в патологоанатомических отделениях;
-
препаратов, в которых имеется срез сосуда;
-
препаратов из тканей, взятых прижизненно и заключенных в парафин.
Сохранность ДНК в этих препаратах и возможность успешного получения генетического профиля невозможно предвидеть заранее, и вопрос об их пригодности или непригодности для проведения экспертизы становится очевиден только в процессе исследования.
Информация о докладчиках:
Алексей Юрьевич Культин, Экспертно-криминалистический центр МВД России, г. Москва
Мария Владимировна Голубенко, к.б.н., НИИ медицинской генетики ТНИМЦ, г. Томск
Николай Казимирович Янковский, академик РАН, д.б.н., Институт общей генетики им. Н.И. Вавилова Российской академии наук (ИОГЕН РАН), г. Москва
Максим Дмитриевич Скалин, ООО ГОРДИЗ, г. Москва
Ирина Геннадьевна Удина, д.б.н., Институт общей генетики им. Н.И. Вавилова Российской академии наук (ИОГЕН РАН), г. Москва
Марина Игоревна Чухряева, к.б.н., ФГКУ «Судебно-экспертный центр Следственного комитета Российской Федерации», г. Москва
Светлана Викторовна Игнатова, Дальневосточный филиал ФГКУ СЭЦ СК России, г. Хабаровск
Анна Игоревна Субботовская, к.м.н., ФИЦ ФТМ, г. Новосибирск
Светлана Валерьевна Алпатова, ГБУЗ ПК «Краевое бюро судебно-медицинской экспертизы и патологоанатомических исследований», г. Пермь


 Меню
Меню





 Все темы
Все темы



 0
0












