МД-2025: Нанопоровое секвенирование и SBS-секвенирование на российском рынке
На конференции «Молекулярная диагностика 2025» прошел сателлитный симпозиум компании «Альбиоген», где обсуждались возможности и вызовы применения секвенирования нового поколения в современной отечественной науке и медицине.

Доклад Алексея Пенина (ИОГен РАН, лаборатория геномики растений) назывался «Геномика для всех, и пусть никто не уйдет обиженным: что может, а чего не может мономолекулярное секвенирование».
Технологии мономолекулярного секвенирования, способные получать длинные прочтения, появились относительно недавно. Алексей кратко рассказал о двух основных методах в данном классе. Одномолекулярное секвенирование в реальном времени (SMRT), разработанное компанией Pacific Biosciences, основано на регистрации флуоресцентно меченных нуклеотидов, присоединяемых единичной молекулой ДНК-полимеразы. Нанопоровое секвенирование изначально было разработано компанией Oxford Nanopore Technologies, однако сейчас собственные разработки предлагают многие компании, включая QiTan Tech и CycloneSeq. Принцип метода — определение последовательности нуклеотидов при протягивании молекулы ДНК через нанопору. Метод SMRT обладает более высокой точностью — около 1 ошибки на 1000 п.н.; у нанопорового секвенирования примерно 1 ошибка на 100 п.н., оно также более склонно к делециям и испытывает больше проблем с GC-богатыми регионами.
За последние два года технологии мономолекулярного секвенирования внесли значительный вклад в геномные исследования. Так, проект Human Pangenome Reference Consortium поставил целью получить 700 фазированных геномов человека. К настоящему времени с использованием SMRT и нанопорового секвенирования получено уже более половины запланированных геномов. При этом было выявлено большое количество ранее неизвестных генов — пангеном человека оказался на 5–6% больше стандартного референсного генома.
Активное развитие нанопорового секвенирования позволяет ожидать, что в будущем для решения большого количества геномных задач можно будет использовать одну платформу на основе длинных прочтений вместо целого арсенала. Повышение конкуренции и спроса на рынке может привести к значительному снижению цен.
Технологии мономолекулярного секвенирования внесли вклад и в понимание структуры генов. Так, вышедшая в 2023 году статья показала, что методы предыдущих поколений секвенирования не захватывают существенной части экзонов и изоформ.
Несмотря на обширные научные достижения, мономолекулярное секвенирование не может похвастаться коммерческим успехом — за последние года акции разрабатывающих их компаний существенно упали в цене. Это не связано с «геномной зимой» — сокращением финансирования после пандемии COVID-19: акции других биотехнологических компаний, таких как BioFicher, находятся на гораздо более благоприятном уровне.
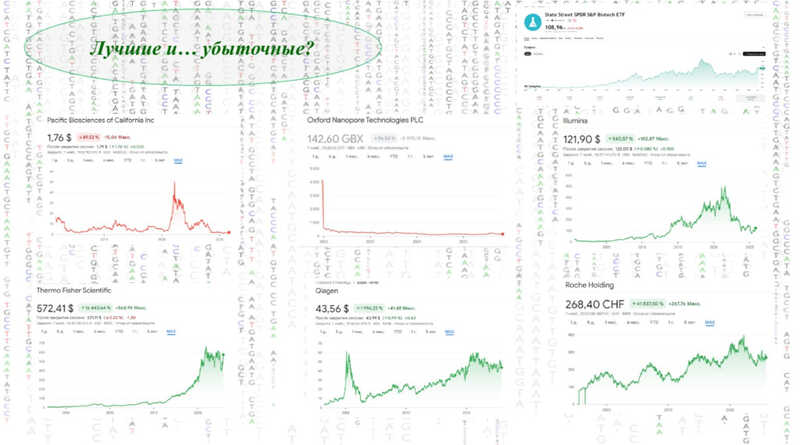 Акции компаний: верхний ряд слева направо — PacBio, Oxford Nanopore, Illumina, нижний ряд — Thermo Fisher, Qiagen, группа компаний Roche. Мономолекулярное секвенирование (красные графики) находится в печальном положении
Акции компаний: верхний ряд слева направо — PacBio, Oxford Nanopore, Illumina, нижний ряд — Thermo Fisher, Qiagen, группа компаний Roche. Мономолекулярное секвенирование (красные графики) находится в печальном положении
По мнению Алексея, такой экономический спад является свойством «молодой» платформы. Так, для методов секвенирования второго поколения разработано множество диагностических пайплайнов, а именно применения в медицинской практике приносит наибольшую прибыль биотехнологическим компаниям. В то же время для секвенирования третьего поколения до недавнего времени не существовало утвержденных протоколов. В том числе это связано с высокой стоимостью и невысокой точностью и стабильностью платформ, что критично для диагностических применений.
Биотехнологические компании активно работают над устранением недостатоков мономолекулярного секвенирования, снижая стоимость и повышая точность работы, однако большое число передовых технологий, включая стремительно дешевеющий SMRT производства PacBio, в настоящее время в России недоступны.
В то же время разработчики методов секвенирования второго поколения не сдают позиции и активно повышают конкурентоспособность своих платформ по сравнению с новыми технологиями, прежде всего снижая цены. Для российского пользователя это ощутимо в первую очередь благодаря возможности использовать аналоги западных разработок. Так, поставляемый компанией «Альбиоген» секвенатор Salus Pro (подробнее о нем рассказано в следующем докладе) позволяет осуществлять секвенирование в несколько раз дешевле Illumina — по цене около 600 рублей за гигабазу. При этом количество ошибок в сравнении с технологией NovaSeq снижено за счет использования адаптированной четырехцветной детекции нуклеотидов.
Повышается и точность технологий секвенирования второго поколения. В первую очередь это разработки, направленные на повышение точностей жидких биопсий. Однако в связи со сложностью в обслуживании, большими размерами, дороговизной и западным происхождением новых разработок вероятность их появления на российском рынке в ближайшем будущем минимальна.
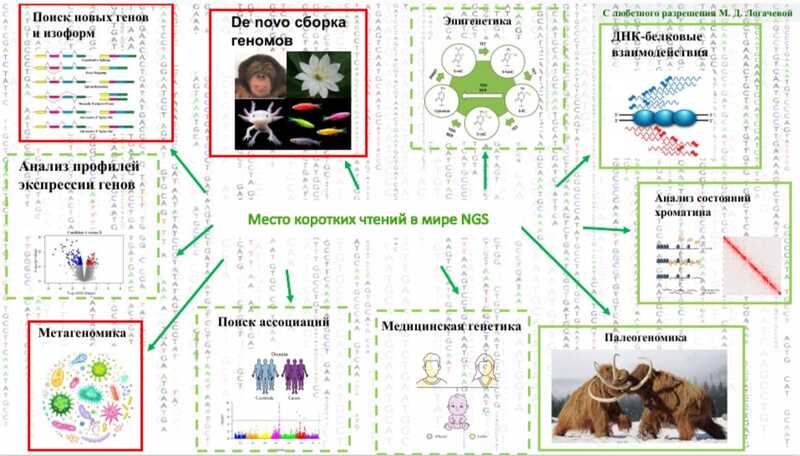
В завершающей части доклада обсуждалось, в каких областях технологии с длинными прочтениями уже заняли доминирующую позицию, а в каких короткие риды еще сохраняют актуальность. Так, сборка геномов уже почти полностью перешла на длинные риды, все активнее используется третье поколение в метагеномике. Вытесняют короткие прочтения и из эпигенетики — длинные прочтения позволяют напрямую детектировать модификации. В задачах анализа состояния хроматина технология Pore-C, использующая нанопоры, постепенно вытесняет более классический Hi-C, что дает возможность решать аналогичные задачи быстрее, легче и дешевле. В медицинской генетике технологии третьего поколения позволяют разрешать изменчивость в длинных повторяющихся участках, что критично при ряде ряда заболеваний, например, спиноцеребеллярной атаксии, появляется возможность прямого анализа метилирования. Также становится возможным быстрое (в течение 3–4 часов) определение профилей устойчивости к антибиотикам и видового состава патогенов. Применение секвенирования третьего поколения для анализа жидких биопсий позволяет выявлять одиночные молекулы ДНК, несущие мутации. Также в диагностике используется детекция циркулирующей РНК для выявления широкого спектра нарушений.
В то же время секвенирование второго поколения все еще занимает доминирующие позиции в исследованиях экспрессии генов (так как требуется множество прочтений), ДНК-белковых взаимодействий (так как длинные прочтения не нужны), палеогеномике (так как молекулы ДНК сильно деградированы и длинные прочтения зачастую невозможны). В рамках поиска ассоциаций методы второго поколения пока на порядок дешевле третьего поколения.
После доклада Алексей Пенин и слушатели обсуждали сложности использования методов третьего поколения для задач метагеномики, в частности, вирусов — отсутствие готовых решений и необходимость значительной модификации протоколов делают работу сложнее, чем при использовании второго поколения. По мнению Алексея, эти проблемы также связаны с молодостью технологии и будут смягчаться в ближайшие 5–7 лет.
Второй доклад симпозиума — «Российский рынок NGS: новинки и тренды» — представил руководитель отдела технической поддержки продукции ООО «Альбиоген» Игорь Шаповалов.
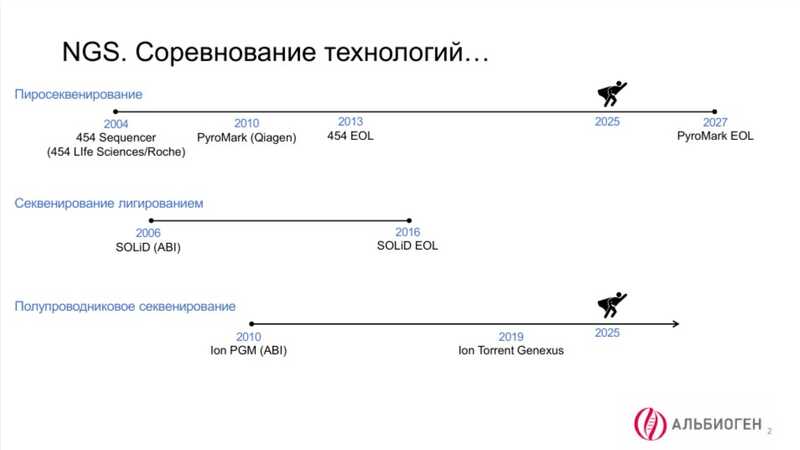
Пионерами NGS второго поколения стали секвенаторы компании 454 Life Sciences, использующие технологию пиросеквенирования. Именно на них были получены первые геномы методом NGS. В марте 2007 года компанию приобрела Roche. Поддержка секвенаторов 454 прекратилась в 2013 году. Далее технология была передана Qiagen, которая до сих пор используют ее в нишевых диагностических целях, однако планирует прекратить поддержку в 2027 году.
Технология секвенирования методом лигирования SOLiD просуществовала недолго и в настоящее время на рынке фактически не представлена, хотя все еще выходят работы на полученных с ее помощью данных.
Большой популярностью пользовалось полупроводниковое секвенирование (широко известна платформа Ion Torrent компании Thermo Fisher), которая применялась в том числе в больших проектах. Сейчас эта технология применяется главным образом в клинической практике, где есть необходимость в высокой степени автоматизации.
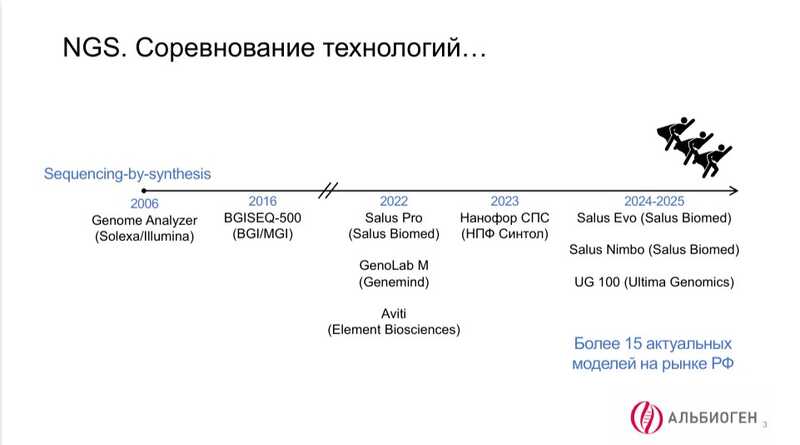
Наконец, доминирующая на данный момент технология — секвенирование путем синтеза (Sequencing by Synthesis, SBS) — появилась в 2006 году и долгое время использовалась только компанией Illumina. Однако в настоящее время ее осваивает множество компаний. Так, в 2022 году резко выросло число производителей SBS-секвенаторов в Китае. Сейчас в России возможно приобрести более 15 моделей SBS секвенаторов, включая Нанофор СПС отечественного производства (НПФ «Синтол»).
Технологическая гонка в том числе, привела к значительному снижению цен на секвенирование. Хотя темпы снижения и замедлились, приблизившись к выходу на плато, а не уйдя «в ноль» вопреки прогнозам, за последние 10 лет стоимость снизилась еще на порядок — с тысяч до сотен долларов за геном.
Параллельно со снижением цен растет спрос на генетические исследования. По самым скромным подсчетам (включающим только проекты, которые отсчитываются о количестве отсеквенированных геномов) на 2024 год получено около двух миллионов полных геномов, в том числе около 10000 геномов древних людей.
Расширяется и область применения секвенирования — кроме базовых геномных исследований, все чаще его методы применяются в транскриптомике, эпигеномике, протеомике, анализе отдельных клеток, в том числе пространственном.
Еще один аспект развития NGS — значительное расширение его использования в медицинской практике. В 2026 году, наиболее вероятно, ряд NGS исследований будет включен в полис ОМС. В связи с этим возникает необходимость в наличии у приборной базы регистрационных удостоверений для использования в медицинских исследованиях на территории РФ.
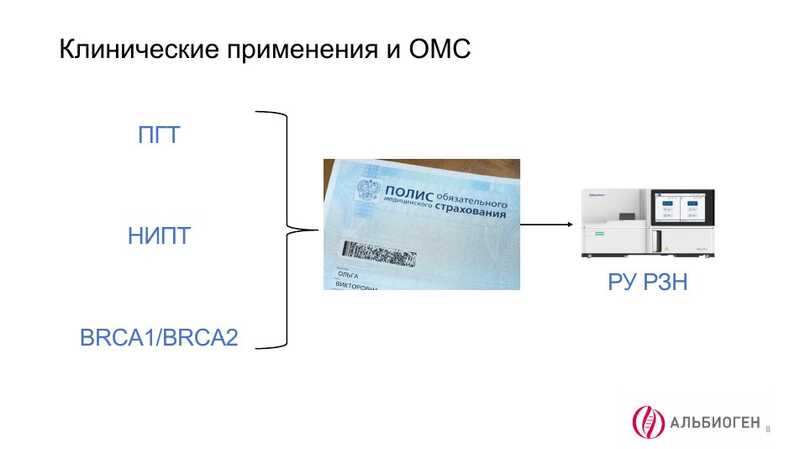
Таким образом формируется «портрет» оптимального востребованного NGS прибора — SBS-технология, низкая цена и наличие регистрационного удостоверения.
Этим критериям удовлетворяют приборы компании Salus Biomed, поставляемые ООО «Альбиоген». Компания была основана в 2020 году в Китае, в 2022 году представила первый секвенатор, а в 2024-м выпустила флагманский высокопроизводительный прибор. Весть процесс разработки и производства целиком осуществляется на территории Китая, без привлечения импорта, что защищает компанию от риска санкционного давления.
В настоящее время в модельном ряду компании представлено три секвенатора — Nimbo, Pro и Evo. Все они используют технологию SBS с четырьмя флуорофорами и совместимы с библиотеками Illumina.
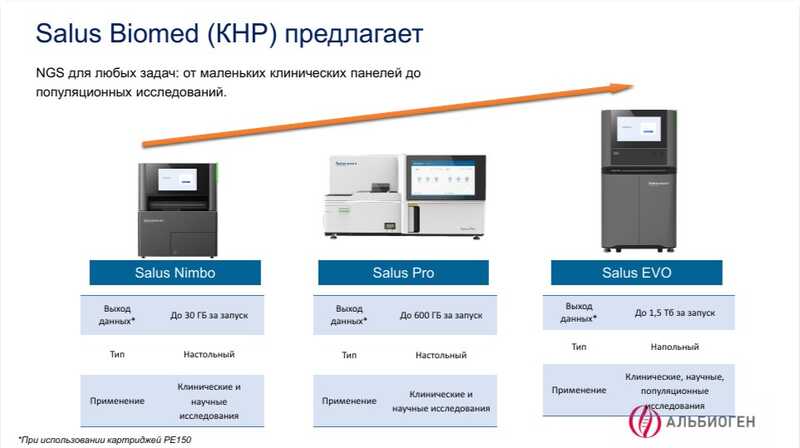
Salus Nimbo — компактное настольное решение для быстрого секвенирования в небольших объемах. Модель Nimbo позволяет получать 25-100М прочтений на ячейку с длиной SE75-PE300. Производительность составляет до 40 Gb за запуск, время запуска 11–13 часов (для PE150).
Salus Pro — основная модель линейки, обеспечивающая высокую производительность исследований. Две ячейки способны работать параллельно в разных режимах, обеспечивая гибкую производительность. Модель позволяет получать 80–500 М прочтений на ячейку с длиной прочтений SE75–PE300 и производительностью до 300 Gb за запуск. Отдельная модификация позволяет повысить производительность до 1000 М прочтений на ячейку и 600 Gb за запуск. Время запуска для PE150 — 8–42 часа. В лаборатории компании «Альбиоген» прибор протестирован для геномных, экзомных, транскриптомных и других исследований.
Наконец, Salus Evo представляет собой флагманскую модель для лабораторий, нуждающихся в больших объемах потокового секвенирования. Это единственная напольная модель, все еще сохраняющая компактность, что позволяет легко встроить ее в лабораторию. Прибор позволяет получать 1500-3000 М прочтений на ячейку с длиной SE75–PE150. Производительность до 1800 Gb за запуск с длиной запуска 21–24 часа для PE150.
В 2025 году компания «Альбиоген» запустила процесс локализации и регистрации приборов Salus Pro и Nimbo для использования в клинической практике на территории России.
Компания «Альбиоген» предоставляет всестороннюю поддержку пользователям приборной базы Salus — команда инженеров и специалистов, прошедших обучение на заводе Salus в Китае готова к решению любых проблем, а локальный склад запасных частей обеспечит быстрый ремонт. Также в лаборатории «Альбиоген» установлены демонстрационные приборы.
Завершающий доклад симпозиума представил Дмитрий Полев (группа метагеномных исследований НИИ эпидемиологии и микробиологии им. Пастера). В начале доклада Дмитрий также напомнил историю NGS-секвенирования, отметив, что все три поколения методов до сих пор сохраняют собственные области применения.
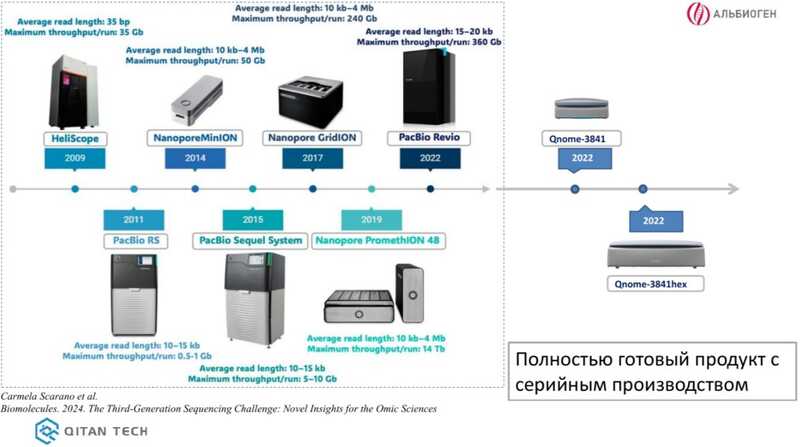
После этого он рассказал о собственном опыте применения нанопорового секвенатора Qnome-384 (Qitan Tech). Решение о приобретении этого секвенатора лаборатория приняла после проблем в работе с Oxford Nanopore, связанных с требованиями отключения системного блока от сети и, как следствие, остановкой обработки данных.
По данным производителя, у прибора, имеющего одну ячейку с 384 порами, производительность 5 Gb за запуск (хотя большинство отзывов указывает скорее на 3 Gb), длина N50 30000, что сравнимо с Nanopore R9.4.1 и максимальная длина прочтений — более 4 млн. оснований. К моменту получения лабораторией набора реактивов до окончания срока годности оставалось 1,5 месяца.
Тестирование секвенатора проводили на трех библиотеках — двух метагеномных (баркодированная и небаркодированная) и одной библиотеке бактериальных геномов. Подготовку проб осуществляли по стандартным протоколам, с восстановлением концов ДНК и лигированием адаптеров с индексами или моторными белками. Специальной подготовки под запуск на нанопорах не проводилось. Запуски осуществляли в разное время.
Все ячейки показали хорошее количество живых пор даже после истечения срока годности на 1,5 месяца — при заявленной гарантии не менее 120 живых пор из 384 фактически живыми были 223–263. После хранения в течение 5,5 месяцев их число составило 241. Таким образом, даже при маленьком заявленном сроке годности фактический срок использования значительно выше вне клинической практики.
 Фото: Андрей Константинов
Фото: Андрей Константинов
Выход данных составил 2,86–3,03 Gb. Анализ скорости утилизации пор показал, что ячейка живет около суток: это не позволяет разбивать запуски на несколько дней.
N50 для метагеномных библиотек составил 4,31–5,38 kb, для геномной — 16,72 kb. По мнению Дмитрия дополнительная оптимизация пробоподготовки может еще повысить длину прочтений. Точность достигла Q 11,5–13.
Далее докладчик рассказал о применении полученных данных. Из 12 проанализированных бактериальных геномов 10 удалось собрать в кольца, еще для двух количество контигов не соответствовало количеству колец, таким образом, данные пригодны к работе. Для почвенных метагеномов основным критерием был процент ридов, который удалось классифицировать по базе данных Kraken, — 77,24–92,10%. При этом кривые накопления числа выделенных таксонов в зависимости от глубины секвенирования в рамках одного запуска на плато не выходили. Это указывает на то, что единичного запуска недостаточно для полноценного метагеномного анализа.
Также Дмитрий упомянул, что существует вариант исполнения прибора с шестью ячейками (Qnome-3841hex) и готовится к выпуску линейка QPursue с 12 ячейками.
Наконец, докладчик рассказал о нескольких нюансах использования секвенатора — жесткие требования к ПО (только Ubuntu 20/22), необходимость подключения через USB v.3 и уже упомянутое вырабатывание ячейки за сутки. В то же время впечатления от работы с прибором положительные — качество сопоставимо с конкурентами.
Информация о докладчиках
Пенин Алексей Александрович, к.б.н., зав. лабораторией геномики растений Института общей генетики им. Н.И. Вавилова Российской академии наук (ИОГен РАН), Москва
Шаповалов Игорь Сергеевич, руководитель отдела технической поддержки продукции ООО «Альбиоген»
Полев Дмитрий Евгеньевич, к.б.н., с.н.с., руководитель группы метагеномных исследований НИИ эпидемиологии и микробиологии им. Пастера, Санкт-Петербург


 Меню
Меню





 Все темы
Все темы



 0
0












