МД-2025: Сенсоры на транзисторах и карманные тест-системы
Какие компактные приборы уже сегодня доступны для передвижных лабораторий? Как разработать автоматическую картриджную систему для ПЦР и ИФА? Можно ли применять для создания сенсоров транзисторы и твердотельные нанопоры? Может ли стать реальностью самотестирование на гепатит С? Эти вопросы эксперты обсудили на секции «Методы point-of-care диагностики инфекций» конференции «Молекулярная диагностика 2025».
Кирилл Прусаков
Фото:
Андрей Константинов
Секцию «Методы point-of-care диагностики инфекции» открыл Сергей Долгушин, представляющий компанию «Айвок», которая уже восемь лет занимается производством медицинского и аналитического оборудования. Доклад был посвящен российским приборам для иммунологических и молекулярно-генетических исследований.
Компания выпустила систему QuattroPlex Lab, которая позволяет детектировать до 50 биомаркеров (антитела, белки, патогены) одновременно с помощью мультиплексного иммунофлуоресцентного анализа. Эта технология аналогична системе Luminex xMAP и работает на основе магнитных кодированных микросфер. Так как система открытая, можно использовать любые тест-системы для анализа широкого спектра маркеров. Технология отличается высокой чувствительностью и пропускной способностью: можно использовать 96-луночный планшет с образцами, в каждом из которых детектируются сразу несколько маркеров одновременно.
QuattroPlex Chip — более компактная система, которая работает по той же технологии. В этом случае образец вносят в одноразовый чип и помещают в прибор, при этом время анализа составляет всего несколько секунд.

Компания также выпустила автоматическую станцию для выделения ДНК и РНК — GeneMack Strela. Прибор имитирует ручное выделение нуклеиновых кислот на магнитных наночастицах. Станция позволяет одновременно обработать от одного до 13 образцов и подходит для лабораторий с небольшим или средним объемом работы. Создатели прибора утверждают, что с его помощью можно выделять нуклеиновые кислоты из сложных биологических образцов, и это открывает перспективы применения не только в молекулярной диагностике и научных исследованиях, но и, например, в криминалистике.
Для измерения концентрации ДНК и белков «Айвок» предлагает Qubix — компактный флуориметр, позволяющий одновременно анализировать до 8 образцов. Прибор измеряет концентрацию ДНК или белков по интенсивности флуоресценции красителя, который входит в набор реактивов.
Компания «Айвок» также разработала серию компактных амплификаторов, подходящих для мобильных PoC-центров. С помощью ДНК-амплификатора LAMPIX8 можно диагностировать инфекции методом петлевой изотермической амплификации (LAMP) при комнатной температуре. Время реакции составляет всего 30 минут.

LAMPIX mini — еще более компактная альтернатива этому прибору, позволяющая анализировать две пробы одновременно. Этот прибор работает от переносного аккумулятора, а ПО доступно на телефоне. По мнению производителя, LAMPIX mini может быть полезен в полевых исследованиях.

Миниатюрный ПЦР-термоциклер TERMIX также позволяет использовать ПЦР даже в передвижных лабораториях. Есть возможность устанавливать собственные программы амплификации, при этом для работы с прибором не требуется компьютер: ПО «вшито» в сам амплификатор. С 2017 года компания «Айвок» произвела более 350 таких приборов.
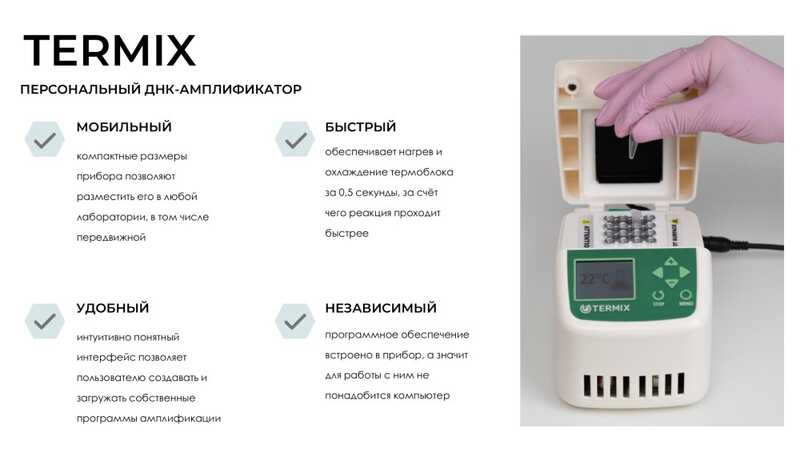
«Айвок» занимается разработкой и другого оборудования, например, для анализа частиц (TRAEKTORIX) или для микрофлюидных систем. Компания самостоятельно разрабатывает ПО для своих приборов.
Докладчик упомянул еще один проект компании — сервис LABbooking. Он представляет собой агрегатор рынка анализов, который, как предполагается, поможет клиенту найти лаборатории и пункты анализа с более низкими ценами и меньшей загруженностью. Это обеспечит двойную выгоду: и для клиентов, и для лабораторий, которые смогут лучше распределить нагрузку между различными пунктами.
Елена Пойманова (Институт синтетических полимерных материалов им. Н.С. Ениколопова РАН), рассказала об органических электролитических транзисторах — основе для изготовления портативных жидкостных биосенсоров.
Органические электролитические транзисторы (ОЭТ) состоят из подложки с контактами и полупроводникового слоя. В каплю электролита (деионизированная вода или биологическая жидкость) на поверхности полупроводникового слоя погружается затвор, в результате на границе раздела фаз создаются двойные электрические слои с большой емкостью. ОЭТ работают с низким напряжением — меньше вольта, поэтому биомолекулы в водных системах не разрушаются.
Исследователи протестировали ОЭТ для работы с широким спектром биоаналитов и выяснили, что с ними можно добиться низких пределов обнаружения — вплоть до дзетамолярных концентраций. Благодаря этому ОЭТ могут применяться в области превентивного здравоохранения, а так как устройства получаются компактными, теоретически любой человек сможет использовать их в быту.
ОЭТ подразделяются на два класса: с электролитическим затвором и электрохимические. В первом случае затвор непроницаем для ионов, а во втором — проницаем. В лаборатории молекулярных сенсорных технологий и устройств работают с первым типом ОЭТ, так как в этом случае электрод или полупроводниковый слой можно легко модифицировать для разработки новых устройств.
В качестве полупроводников ученые используют аннелированные сопряженные системы, малые молекулы или полимеры. Наиболее перспективное решение — смесь полупроводника с полимерами: такой полупроводниковый слой работает стабильнее и дольше.
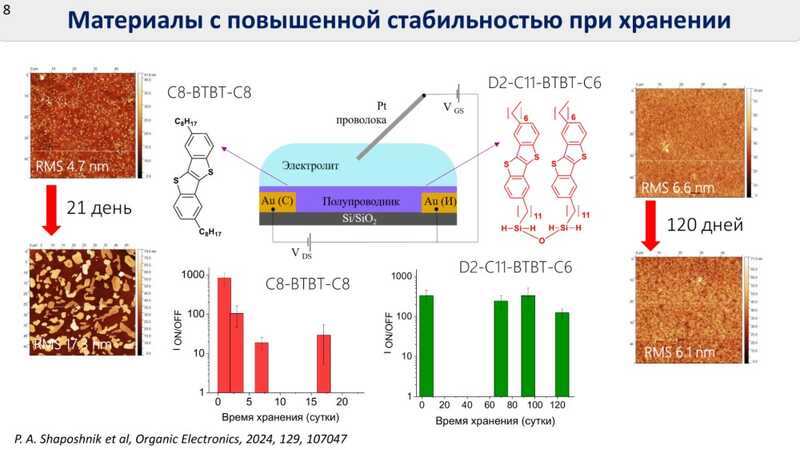
Для диагностических целей в ОЭТ помещают биоузнающий слой. Узнающими элементами в нем могут быть антитела или аптамеры — последние предпочтительнее, ведь их легче синтезировать под конкретную мишень.
Так, исследователи разработали аптасенсор на основе ОЭТ для детекции вируса птичьего гриппа А. В нем аптамер против вируса соединили с ОЭТ за счет биотин-стрептавидинового взаимодействия. С помощью сенсора исследователи действительно смогли детектировать вирус птичьего гриппа А, причем иммобилизацию вирусных частиц подтвердили с помощью атомно-силовой микроскопии.
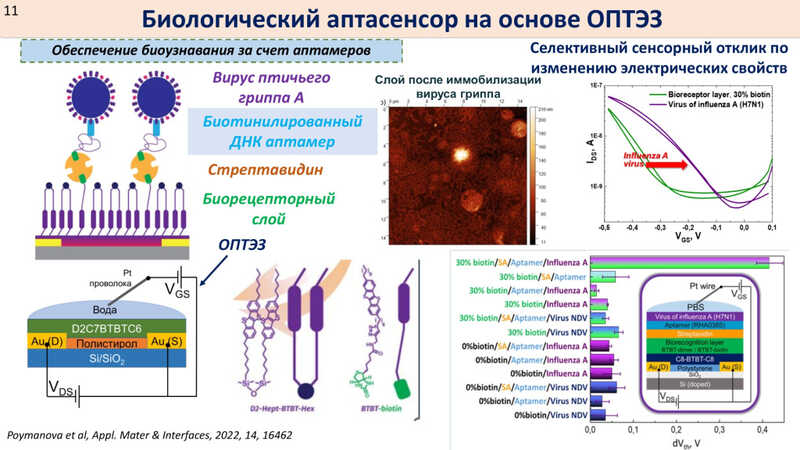
В основном ученые разрабатывали небольшие (1,5х2 см) одноразовые чипы. Однако перед ними также встала задача разработки многоразовых сенсоров. Биоузнающий слой в таком сенсоре сделали на основе полимерных мембран, модифицированных золотом, и на них размещали аптамеры. Однако исследователи столкнулись с проблемой: вирионы в таком режиме работы через некоторое время просто забивают поры мембраны.
Помимо аптамеров, ученые использовали моноклональные антитела для детекции олигосахаридов. Такой сенсор можно применять для диагностики аспергиллеза.
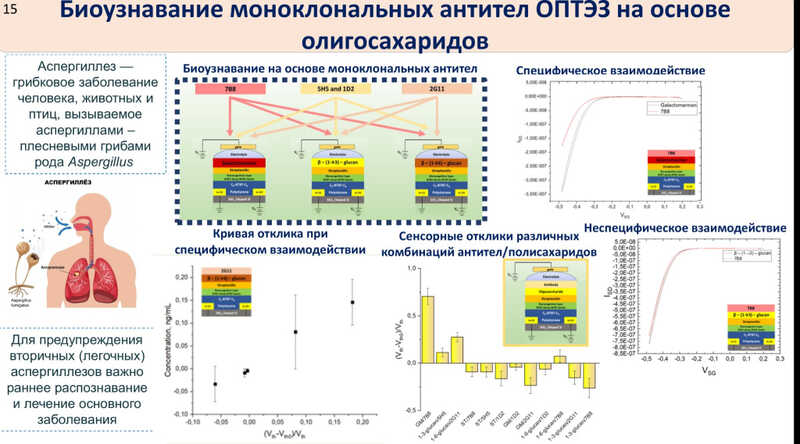
ОЭТ — потенциально масштабируемые системы: органическую электронику можно совмещать с печатной. Так, исследователи из Саудовской Аравии разработали печатный сенсор для определения глюкозы.
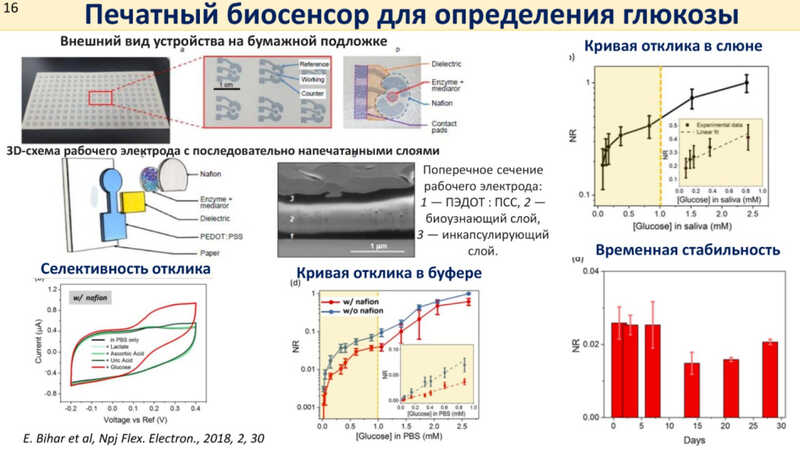
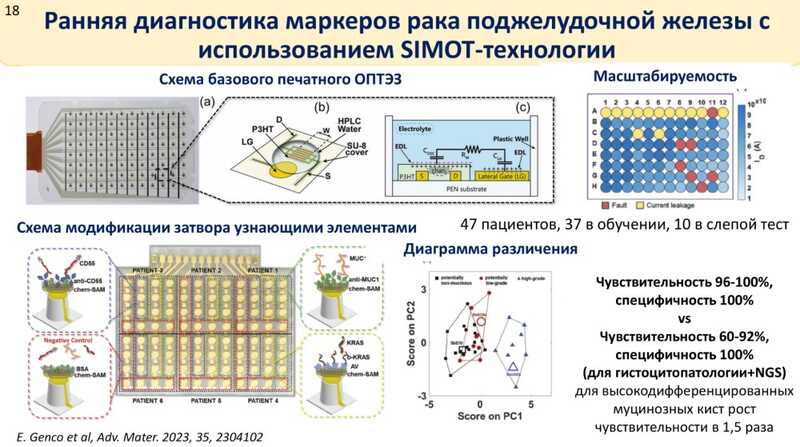
За счет использования большого транзистора (SIMOT-технология — single-molecule-with-a-large-transistor) международной группе исследователей удалось добиться большой чувствительности сенсора: разработанный ими сенсор IgG может детектировать вплоть до одной молекулы в слюне. Это достигается за счет механизма домино: при детекции даже одной молекулы сигнал далее просто амплифицируется. Эта технология отличается хорошей масштабируемостью и позволяет анализировать несколько образцов одновременно, в том числе контроли. На ее основе авторы попробовали создать сенсор для ранней диагностики маркеров рака поджелудочной железы в плазме или кистозной жидкости.
Аптасенсоры на основе ОЭТ позволяют детектировать разные мишени. Например, исследователи протестировали аптасенсоры из I-мотивов — такие структуры ДНК чувствительны к pH. Получились устройства, которые при одном pH улавливают катионы серебра, а при другом — частицы вируса гриппа А.
Большое преимущество сенсоров на основе ОЭТ состоит в том, что они могут работать в разных биологических жидкостях. При тестировании сенсоров сначала используют водные буферные растворы, но в дальнейших экспериментах применяют различные биологические жидкости: слюну, плазму, сыворотку крови и т.д. Елена Пойманова перечислила и другие преимущества сенсоров на основе ОЭТ, которые делают их перспективной основой для жидкостных биосенсоров: гибкость архитектурных решений, низкое энергопотребление, высокая чувствительность, сравнимая с ИФА.
Далее Денис Лебедев (СПбАУ им. Ж.И. Алферова) рассказал о твердотельных нанопорах, которые могут использоваться для анализа единичных биомолекул.
Идея нанопорового секвенирования ДНК была предложена еще в 1980-х годах, а сейчас биологические нанопоры уже входят в состав коммерческих приборов. Однако эти поры подвержены внешним воздействиям, так что нанопоровые картриджи имеют срок годности не более 3 месяцев. Кроме того, специфичность биологических пор ограничивает спектр возможных исследований.
Высокая чувствительность биологических нанопор объясняется их малым диаметром: чем меньше отверстие, тем меньше объект, который можно анализировать. Преимущество же твердотельных нанопор в том, что молекулярно-ионным транспортом внутри них можно управлять, например за счет изменения геометрии поры или ее модификации. Также на проходящие через твердотельную пору объекты можно воздействовать внешним электрическим или оптическим сигналом.
Основная проблема твердотельных нанопор — плохое соотношение сигнал/шум. Это связано с тем, что такие молекулы, как ДНК, очень быстро «проскакивают» через них. В биологических порах этот вопрос решается за счет моторных белков. В твердотельных же порах транслокацию молекулы может замедлить за счет лазеров.
При изготовлении твердотельных нанопор используют пучки заряженных частиц или метод контролируемого диэлектрического пробоя. Первый подход — точный и дорогой, а второй — маловоспроизводимый и дешевый.
Исследователи научились изготавливать нанопоры из свободно подвешенной мембраны нитрида кремния толщиной 25–500 нм с диаметрами пор 5 и 10 нм. Они также обнаружили, что облучение нанопоры галогеновой лампой, мощность излучения которой на 5 порядков ниже по сравнению с лазером, приводит к изменению проводимости нанопоры на 20%. Это связано с поверхностными состояниями в нитриде кремния, которые находятся в запрещенной зоне и поэтому могут возбуждаться в широком оптическом спектре, а не только с помощью лазера.
При добавлении ДНК к твердотельной поре было видно, что молекула успешно проходит через нее. Ученые определили это по изменению проводимости поры.
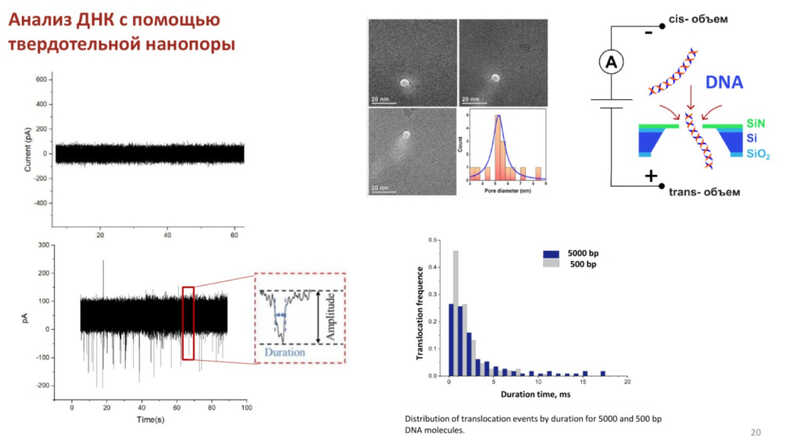
С коллегами из Института биоорганической химии им. М.М. Шемякина и Ю.А. Овчинникова РАН исследователи попробовали проанализировать с помощью твердотельной нанопоры 20S-субъединицу протеасомы. К системе из единичных молекул 20S-субъединиц добавляли молекулы-активаторы — PA28 и MBP. Так впервые удалось исследовать динамику разложения субстрата протеасомой in situ, а не на замороженных молекулах.
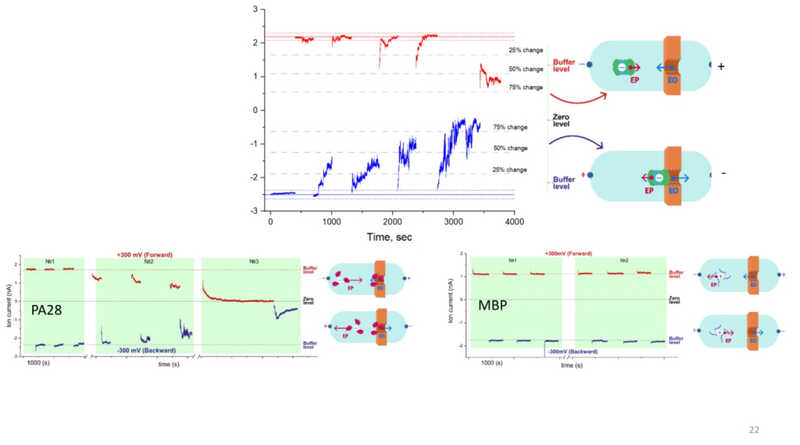
А с коллегами из НИИ биомедицинской химии им. В.Н. Ореховича ученые проанализировали функциональную активность единичных молекул пероксидазы хрена и цитохрома P450. Денис Лебедев заключил, что твердотельные нанопоры можно использовать для анализа большего числа биомолекул, чем биологические нанопоры, что значительно расширяет возможные сферы их применения.
Станислав Пауль из ООО «Троицкий инженерный центр» рассказал об опыте разработки экспресс-тест-систем.
Троицкий инженерный центр — компания полного цикла разработки приборов с собственным опытным производством, основанная в 2013 году. В 2022 году в ООО «ТИЦ» был создан карманный анализатор Veeny, работающий на микрофлюидном картридже. Анализатор состоит из станции весом 50 г с информационным светодиодом и картриджа с восемью реакционными лунками (две из них для контролей). Программа амплификации в приборе длится всего 45 мин, но предварительные результаты можно увидеть уже через 20–35 мин. Детекция сигнала производится визуально: цвет лунки меняется с синего или красного на желтый.

Раствор с образцом самотеком заполняет реакционные камеры внутри картриджа за 20–30 секунд. Прибор уже проверяли для диагностики респираторных инфекций: в этом случае в картридж помещается сразу мазок. Исследователи также разработали прототип мобильного приложения для обработки данных: пользователю достаточно сфотографировать прибор, и приложение проанализирует цветовые значения в лунках.
Компания нашла партнера для разработки тест-систем для ветеринарии: особый интерес представляла диагностика африканской чумы свиней (АЧС). Вместе с фирмой SkyLAMP ученые разработали прибор SkyLAMP ScanSpace на 10 картриджей. Для диагностики АЧС использовался картридж ASF ScanPoint, вместе с которым поставляются микропипетки и пробирки для загрузки образцов. Запустить реакцию может неквалифицированный сотрудник: нужно всего лишь взять одну каплю сыворотки, смешать ее с буфером в пробирке и нанести на картридж. В лунках картриджей есть положительный и отрицательный контроль. Длительность детекции — всего 45 мин, но о положительном результате можно узнать уже через 30 мин.
Система ASF-Scanpoint выявила у всех 10 свиней, экспериментально зараженных вирулентным штаммом АЧС, вирус в сыворотке крови и в смыве носовой полости, то есть чувствительность достигла 100%, превысив показатели как иммунохроматографического анализа, так и ПЦР. При этом детектировать инфекцию можно было уже на 3-й день после заражения.

Кирилл Прусаков (ФНКЦ ФХМ им. Лопухина ФМБА России) посвятил свой доклад разработке картриджных систем для диагностики «у постели больного» и в полевых условиях. Он отметил, что обычно для диагностики анализы проводятся в открытых объемах, но в диагностике в «прикроватном» формате, напротив, стараются переходить к анализу в замкнутых микрофлюидных системах — «лабораториях на чипе».
Так, например, широкой популярностью пользуется платформа одноразовых микрофлюидных картриджей для ПЦР GeneXpert (Cepheid): в картридж помещают образец, затем картридж устанавливают в анализатор, который в автоматическом режиме смешивает растворы, проводит инкубацию и детектирует сигнал амплификации. В России уже появились аналоги этого прибора, такие как «БиоЭксперт» или «Изаскрин-8».
Иммуноферментный анализ (ИФА) — тоже популярный вид анализа в диагностике. Картриджные системы для ИФА существуют, но они часто работают в качественном или полуколичественном формате и не позволяют измерять низкие концентрации аналитов. Есть полноценные системы картриджного ИФА — например, Ella от фирмы ProteinSimple с одноразовыми картриджами, — но их немного. Кирилл Прусаков связал этот факт со сложностью самого механизма реакции ИФА —специфического аффинного взаимодействия.
В ФНКЦ ФХМ попробовали создать свою картриджную систему для ИФА, взяв за основу поворотные микрофлюидные распределители. Такие устройства уже используются в некоторых PoC-системах. Для автоматизированного ИФА на магнитных микрочастицах разработали специальный поворотный клапан-распределитель. Пользователю необходимо всего лишь поместить пробу во входной порт картриджа.
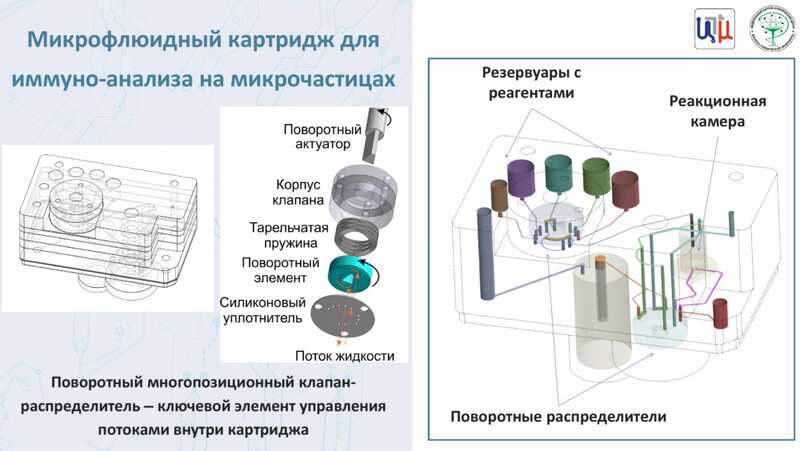
По сравнению с ручным анализом у автоматического сохраняется линейная зависимость между концентрациями аналита и электрохимическим сигналом. Эти результаты удалось получить на сыворотках пациентов.
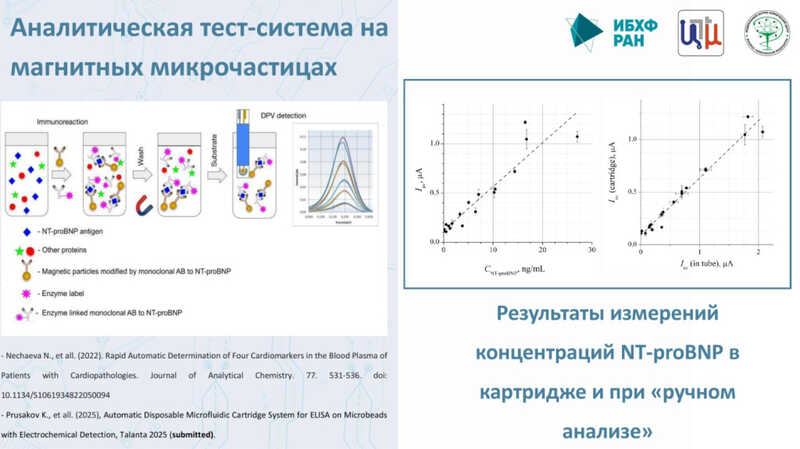
Также исследователи разработали универсальный картридж для ИФА. Обычно при использовании сэндвич-ИФА сенсорные антитела, улавливающие аналит, нанесены на лунки, а затем происходит связывание с детектирующим антителом. Поэтому исследователи хотят строить картриджи «вокруг» лунок из стандартных наборов ИФА, чтобы остальная реагентика была универсальной.
Докладчик с коллегами уже создали прототипы картриджа и стенда для его процессирования, используя для их производства методы литья и ультразвуковой сварки. Разработчики считают, что такая система позволит значительно продвинуть методы диагностики в местах оказания медицинской помощи.

С завершающим докладом о перспективах самостоятельного тестирования на гепатит С выступил доктор Аджит Сингх Бхадория из Всеиндийского института медицинских наук.
В 2016 году ВОЗ обозначила гепатит С как одну из основных угроз здравоохранению, которую требуется устранить к 2030 году. Для этого к 2020 году нужно было диагностировать 90% всех инфицированных гепатитом С. Однако в 2019 году удалось диагностировать лишь 21% больных.
Докладчик представил результаты нескольких исследований самотестирования — стратегически важного инструмента для диагностики гепатита С, который при этом не будет определяющим или замещающим другие способы диагностики.
Согласно систематическому анализу орального самотестирования, почти все пациенты успешно справились с анализом и рекомендовали его другим. С тестом, в котором требовалось взять у себя кровь, справились почти все участники после детальных инструкций и демонстраций, но меньше половины тех, в чьем распоряжении была только инструкция.
Другое исследование показало, что с самотестированием лучше справляются молодые люди, а также люди с высшим образованием. Еще одно исследование оценивало эффективности самотестирования среди заключенных в тюрьмах Индии, где заболеваемость гепатитом С выше, чем в среднем по популяции: 98% заключенным требовалась помощь в сборе образца, лишь 67% сообщили, что процедура им понравилась и они готовы ее рекомендовать другим.
В некоторых работах оценивали эффективность доставки наборов для самотестирования на дом. В Грузии, Малайзии и Пакистане это позволило значительно повысить уровень тестирования населения по сравнению с обычными методами диагностики. Сравнивалось также применение наборов для самотестирования в больнице или же в домашних условиях. Если наборы предлагали для использования на дому, то соглашалось 72% людей против 58% людей, которым предлагали применить такой набор в медучреждении. Многие опрошенные отказывались из-за нехватки времени, боязни игл или из-за убеждения, что им просто не требуется такая диагностика.
Аджит Сингх Бхадория рассказал о том, как самотестирование пробовали интегрировать в медицинскую систему в тюрьмах в Северной Индии. Заключенным провели демонстрацию, показывающую, как использовать набор для самотестирования, а также рассказали о рисках, связанных с гепатитом С, регулярно проводили консультации с использованием телемедицины. Среди заключенных 3,4% были заражены гепатитом С, при этом 84% прошли самотестирование. Из тех, кто получил положительный результат, 60% начали лечение, но только 28% из них завершили его. Вероятная причина в том, что многие покидали места заключения, так как отбывали срок за мелкие правонарушения, и в итоге «выпадали» из поля зрения системы здравоохранения.
Информация о докладчиках
Долгушин Сергей Анатольевич, к.ф.-м.н., ООО «Айвок» г. Зеленоград
Пойманова Елена Юрьевна, к.х.н., Институт синтетических полимерных материалов им. Н.С. Ениколопова РАН
Лебедев Денис Владимирович, к.ф.-м.н. СПбАУ им. Ж.И.Алферова, ИАП РАН, г. Санкт-Петербург
Пауль Станислав Юрьевич, ООО «Троицкий инженерный центр», г. Троицк.
Прусаков Кирилл Александрович, ФНКЦ ФХМ им. Ю.М. Лопухина ФМБА России, г. Москва
Аджит Сингх Бхадория, Всеиндийский институт медицинских наук (All India Institute of Medical Sciences)


 Меню
Меню





 Все темы
Все темы



 0
0











