На эффект популярных препаратов против ожирения влияют генетические факторы
Препараты на основе агонистов рецептора GLP1, такие как семаглутид или тирзепатид, значительно снижают вес у большинства людей. Однако примерно каждый десятый пациент теряет менее 5% веса, а многие во время лечения страдают от тошноты и расстройств пищеварения. Сотрудники 23&Me проанализировали свою базу данных и показали, что на индивидуальные вариации эффекта этих препаратов могут влиять генетические факторы. Наибольший вклад внесли варианты в генах мишеней семаглутида и тирзепатида — рецепторов GLP1 и GIP. Однако негенетические факторы, связанные со здоровьем и образом жизни, остаются более мощными предикторами потери веса.

Препараты для лечения ожирения и диабета, содержащие агонисты рецептора глюкагоноподобного пептида 1 (GLP-1, ГПП-1), сейчас принимают миллионы взрослых людей во всем мире, и ожидается, что число их будут расти. Многим пациентам удается снизить вес на 20% за относительно короткое время — результат, который еще недавно казался невообразимым.
Однако хотя большинство людей, принимающих эти препараты, добиваются снижения не менее чем на 10%, примерно один из десяти теряет менее 5%, а некоторые вообще не отвечают на терапию. Примерно у одного из трех проявляются побочные эффекты — тошнота и рвота, диарея или запор. Возможные генетические причины такого разброса исследовали сотрудники компании 23andMe, предоставлявшей услуги по потребительской генетике. Их статья опубликована в Nature.
Агонисты рецептора GLP-1, включая семаглутид (коммерческие названия Оземпик, Вегови) и тирзепатид (Мунджаро, Зепбаунд; у тирзепатида есть и вторая мишень, к чему мы еще вернемся), имитируют естественные гормоны, вырабатываемые клетками кишечника. И естественные гормоны, и лекарства помогают регулировать аппетит, высвобождение инсулина и пищеварение. Однако не до конца ясно, почему одни люди теряют больше веса, чем другие, или почему одни страдают от тошноты, а другие нет.
Чтобы выявить потенциальные генетические факторы, вызывающие эти различия, авторы статьи провели полногеномный поиск ассоциаций (GWAS) в данных 23andMe. (Подробнее о банкротстве этой компании в прошлом году и перспективах использования ее данных в научных целях. Позднее основательница компании Энн Воджицки выкупила 23andMe за $305 млн. В настоящее время 23andMe Research Institute позиционирует себя как некоммерческую медицинскую исследовательскую организацию и публикует новости о научных исследованиях, однако в то же время постоянным клиентам предлагает новые услуги.)
Данные включали как генетическую информацию, так и самоотчеты 27 885 человек, получавших агонисты GLP-1. Люди из этой выборки потеряли в среднем 11,7% (11,3 кг) массы тела примерно за 8.3 месяца лечения. Однако стандартное отклонение было большим — 9.5%, то есть были люди, которые почти не потеряли веса, а кто-то потерял гораздо больше среднего, отдельные лица — до 30%.
GWAS провели более чем для 15 000 человек, причем выявили четкие ассоциации между рассматриваемыми признаками и вариантами в генах GLP1R и GIPR, которые кодируют две основные мишени препаратов.
Вариант rs10305420 в гене GLP1R рецептора GLP-1 был связан с несколько бо́льшим (на 0,641%) снижением индекса массы тела (ИМТ), что соответствует примерно 0,76 кг дополнительной потери веса на каждый аллель гена с таким вариантом по сравнению с теми, кто его не имеет. Это миссенс-вариант — замена нуклеотида цитозина (С) в гене на тимин (Т) проводит к замене аминокислоты в белке (пролин на лейцин). Таким образом, люди с заменой С на Т в обеих копиях гена GLP1R теряли на 1,5 кг больше, чем люди без замен в обеих копиях.
Аллель Т встречается с наибольшей частотой среди людей европейского происхождения: 64%имеют хотя бы одну копию, 16% имеют две. Для лиц африканского происхождения она нехарактерна: лишь около 6% — носители хотя бы одной копии, 0,1% — двух копий.
Связывание рецептора GLP-1 с его естественным или искусственным агонистом передает организму сигнал о насыщении (это и есть причина, по которой люди гораздо меньше едят во время лечения). Замена Pro7Leu находится близко к N-концу белка, и авторы предполагают, что она стабилизирует структуру этого участка и это способствует усилению сигнала. Для аллеля Т также показаны ассоциации с более высокой экспрессией рецептора в тканях и меньший риск диабета 2 типа.
Поскольку опросники 23andMe для клиентов были довольно подробными и оригинальными, удалось также установить, что носители аллеля Т реже едят красное мясо и орехи по сравнению с неносителями, чаще — сладкие блюда и напитки, чаще предпочитают шоколадное мороженое ванильному и чаще сообщают о кариесе зубов. Значение этих находок остается неясным, но можно предположить, что аллель влияет также на пищевое поведение.
Еще два варианта в гене GLP1R (rs11760106 и rs9357296) также были ассоциированы с потерей веса, но кроме того, с побочными эффектами, в том числе тошнотой и рвотой. Не исключено, что первое было следствием второго.
Вариант rs71338792 в другом гене — GIPR, гене рецептора глюкозозависимого инсулинотропного полипептида (GIP), был связан с тошнотой и рвотой у людей, принимающих тирзепатид. В отличие от семаглутида, этот препарат действует на две мишени — рецепторы GLP-1 и GIP. На потерю веса вариант rs71338792 не влиял. Ранее для него была показана связь с некоторыми другими признаками, в частности, со сниженным риском ожирения и дисфункции почек.
Примечательно, что rs71338792 почти всегда наследуется вместе с распространенным миссенс-вариантом rs1800437, который приводит к замене аминокислот Glu354Gln в рецепторе и, как считается, нарушает его функцию. Возможно, поэтому связывающийся с GIP компонент тирзепатида не может подавить тошноту, вызванную GLP1-компонентом.
Авторы предположили, что повышенная вероятность тошноты на фоне приема тирзепатида должна быть у носителей аллелей, вызывающих обе замены (Pro7Leu в GLP1R и Glu354Gln в GIPR) — это примерно 0,6% людей европейского происхождения. Возможно, им не следует назначать тирзепатид, тем более что выбор препаратов этого класса становится все шире.
Таким образом, действие агонистов GLP1 модифицируется различиями в генах — мишенях лекарственных препаратов. Однако авторы подчеркивают, что важными предикторами потери веса и побочных эффектов при лечении этими препаратами остаются негенетические факторы, такие как возраст, пол, тип лекарства и дозы, наличие диабета второго типа, гипертензии и неалкогольной жировой болезни печени. По сравнению с ними влияние генетики представляется незначительным.
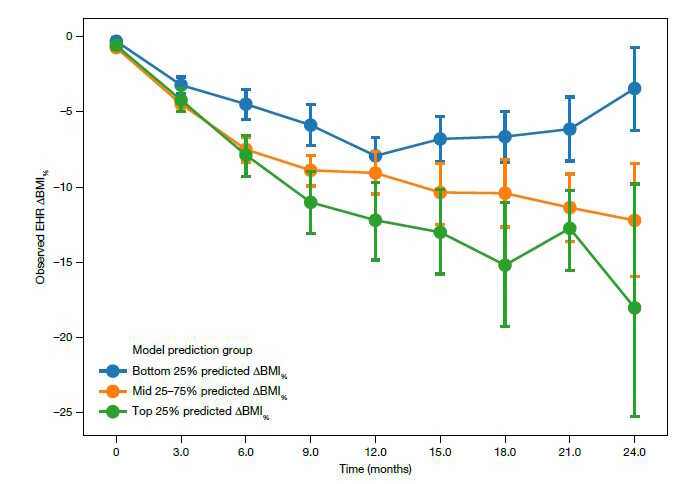 Авторы создали математическую модель для прогнозирования пользы от препаратов, снижающих вес, на основе генетического фона человека, демографических факторов и наличия заболеваний. Прогнозы по средней, наибольшей и наименьшей потере веса (в процентных изменениях массы тела) оказались верными. Credit: Nature, 2026. DOI:
10.1038/s41586-026-10330-z |
CC BY-NC-ND 4.0
Авторы создали математическую модель для прогнозирования пользы от препаратов, снижающих вес, на основе генетического фона человека, демографических факторов и наличия заболеваний. Прогнозы по средней, наибольшей и наименьшей потере веса (в процентных изменениях массы тела) оказались верными. Credit: Nature, 2026. DOI:
10.1038/s41586-026-10330-z |
CC BY-NC-ND 4.0
Есть и еще один беспокоящий фактор, который отмечает автор комментария в Nature, Рут Лоос из Центра фундаментальных метаболических исследований Фонда Novo Nordisk в Копенгагенском университете. Связь между вариантом rs10305420 в гене GLP1R и потерей веса была подтверждена у более 4800 человек из когорты биобанка All of Us, однако метаанализ прошлого года, включавший 6750 человек из девяти биобанков, этой ассоциации не выявил. Так что для подтверждения надежности этих результатов нужны дальнейшие исследования.
Тем не менее результаты могут помочь выбрать наиболее подходящий препарат с учетом генетических данных пациента, а также создать более совершенные препараты против ожирения и диабета.
Источники
Qiaojuan Jane Su, et al. Genetic predictors of GLP1 receptor agonist weight loss and side effects // Nature, 2026. DOI: 10.1038/s41586-026-10330-z
Ruth J. F. Loos. Genetics reveal why effects of GLP-1 drugs vary // Nature, 2026. DOI: 10.1038/d41586-026-00905-1


 Меню
Меню





 Все темы
Все темы




 0
0











