Развитие обсессивно-компульсивного расстройства связано с изменениями в протеомах нейронов и астроцитов
Новый подход к изучению протеомов различных типов клеток головного мозга обнаружил изменения экспрессии астроцитарных белков при обсессивно-компульсивном расстройстве (ОКР). Например, нейрональный белок SAPAP3, для которого уже была известна связь с ОКР, найден и в астроцитах стриатума у мышей. Показано, что уровень экспрессии SAPAP3 в них также ассоциирован с фенотипическими проявлениями ОКР.

Исследование сетей белок-белковых взаимодействий в различных типах клеток головного мозга может улучшить понимание механизмов развития заболеваний ЦНС (в том числе психических расстройств) и способствовать разработке более эффективных подходов к терапии. Среди свежих работ по этому направлению — вышедшая в Nature статья о новом подходе к исследованию протеомов нейронов и астроцитов и их связи с механизмами развития обсессивно-компульсивного расстройства (ОКР).
Количественные протеомные исследования нейронов и астроцитов, и прежде всего изучение взаимодействий между этими типами клеток на белковом уровне, осложнены особенностями применяемых в настоящее время методов. Одна из проблем состоит в том, что диссоциация ткани на отдельные клетки и последующая изоляция отдельных типов клеток при помощи FACS сильно влияет на протекание различных процессов в нейронах и астроцитах. К примеру, в ходе диссоциации может существенно изменяться морфология клеток. Подобные методы в первую очередь повреждают именно астроциты, которые участвуют в ответе на стресс, — в результате протеом таких клеток может быть сильно изменен стрессовым воздействием, вызванным пробоподготовкой.
Авторы новой работы предложили альтернативный подход, не требующий диссоциации клеток. Он основан на применении таргетированных в различные типы и компартменты клеток биотинлигаз BioID2 (ферментов, пришивающих биотин к лизиновым остаткам) и последующей детекции биотинилированных белков.
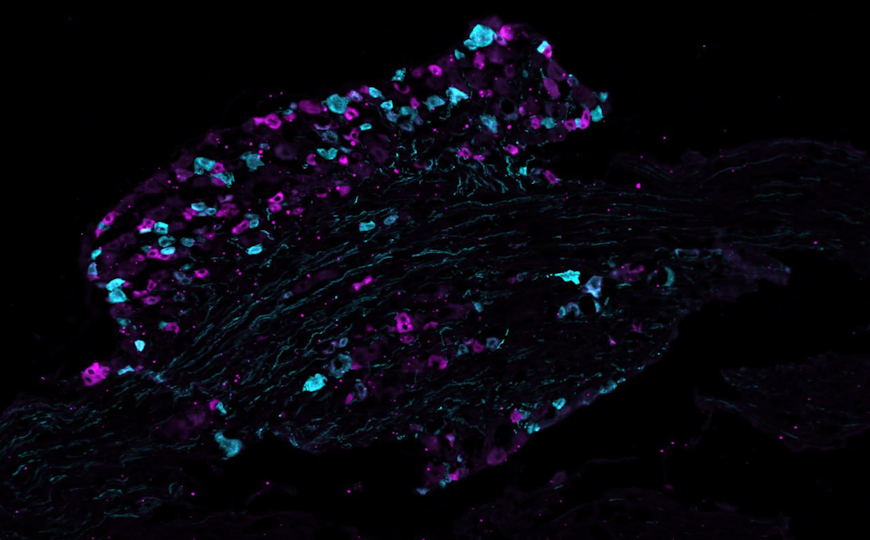
Основная структура головного мозга, ассоциированная с патогенезом ОКР — стриатум (полосатое тело). BioID2 доставляли в нейроны или астроциты стриатума мышей in vivo при помощи аденоассоциированных вирусов (AAV). Специфичность экспрессии в нейроне либо астроците обеспечивало наличие в векторной конструкции соответствующего промотора. Кроме того, в каждом случае использовались два варианта BioID2 — биотинлигаза локализовалась в цитозоле либо в плазматической мембране клетки. Такой метод позволил охарактеризовать субпротеомы отдельных клеточных компартментов исследуемых астроцитов и нейронов мыши без применения повреждающих методов пробоподготовки.
Для валидации работоспособности подхода авторы получили и сравнили различные субпротеомы клеток стриатума. Анализ протеомных данных выявил основные сигнальные пути, характерные для астроцитов (метаболизм липидов, межклеточный сигналинг и ряд ассоциированных с актиновыми филаментами процессов) и нейронов (синаптический и рецепторный сигналинг, а также ионсвязывающая активность). При этом ключевые пути биосинтеза оказались общими для астроцитов и нейронов стриатума.
Затем авторы провели сравнение основанного на биотинилировании in vivo метода и традиционного FACS. Биотинилирование in vivo идентифицировало 3274 белка, тогда как FACS — только 1378. «Утерянные» белки были ассоциированы с регуляцией морфологии астроцитов, которая также нарушается при использовании стандартных методов.
Дальнейшая часть исследования была связана с обнаружением в астроцитах белков, которые ранее считались нехарактерными для этого типа клеток. Одним из них оказался SAPAP3, который кодируется геном Dlgap3 и имеет высокие уровни экспрессии в клетках стриатума. Этот структурный цитозольный белок обычно обнаруживается в средних шипиковых нейронах стриатума (medium spiny neurons, MSN); он ассоциирован с повторяющимися паттернами поведения и с развитием ОКР у человека. На мышиных моделях также было показано, что нокаут SAPAP3 приводит к развитию характерного для ОКР поведения (повышенная тревожность и постоянный груминг, приводящий к повреждениям кожи на мордочке).
Детекция экспрессии SAPAP3 в астроцитах, его взаимодействие с рядом мембранных белков и полученные на мышиной модели подтверждения роли астроцитарного SAPAP3 развитии ОКР поставили вопрос: как изменяется протеом мембран астроцитов в стриатуме мышей с нокаутом по этому белку? Полученные авторами протеомные данные указывают на снижение экспрессии 182 белков, локализованных возле мембран астроцитов, и на увеличение экспрессии ещё 275 (в их числе EZR и GLT1, для которых в рамках этого же исследования было показано взаимодействие с SAPAP3).
На мышиной модели ОКР авторы показали, что восстановление экспрессии SAPAP3 в астроцитах стриатума при помощи доставки в AAV-векторах улучшает состояние животных. Например, снижение избыточного груминга было сопоставимо с эффектом флуоксетина, применяемого в качестве терапевтического агента при ОКР. Восстановление экспрессии SAPAP3 в нейронах стриатума также имело положительное влияние — оно ослабило тревожность мышей, оцененную по соотношению пребывания на открытых и закрытых пространствах, и снизило продолжительность груминга.
Полученные результаты, по мнению авторов, будут способствовать дальнейшему изучению механизмов развития ОКР, в том числе с точки зрения пространственных паттернов экспрессии белков, ассоциированных с заболеванием, а также разработке терапевтических стратегий. В частности, эффективными могут оказаться методы лечения, которые затрагивают как нейроны, так и астроциты стриатума.
Источник
Soto, J.S. et al. // Astrocyte–neuron subproteomes and obsessive–compulsive disorder mechanisms // Nature (2023). DOI: 10.1038/s41586-023-05927-7


 Меню
Меню





 Все темы
Все темы




 0
0