Вариант омикрон вируса SARS-CoV-2 мог эволюционировать в грызунах
Ученые из США показали, что мутации в S-белке штамма омикрон SARS-CoV-2 лучше адаптированы к рецептору, располагающемуся на поверхности клеток мышей, чем к человеческому рецептору. Возможно, мыши или другие грызуны были резервуаром, в котором возник и эволюционировал омикрон.
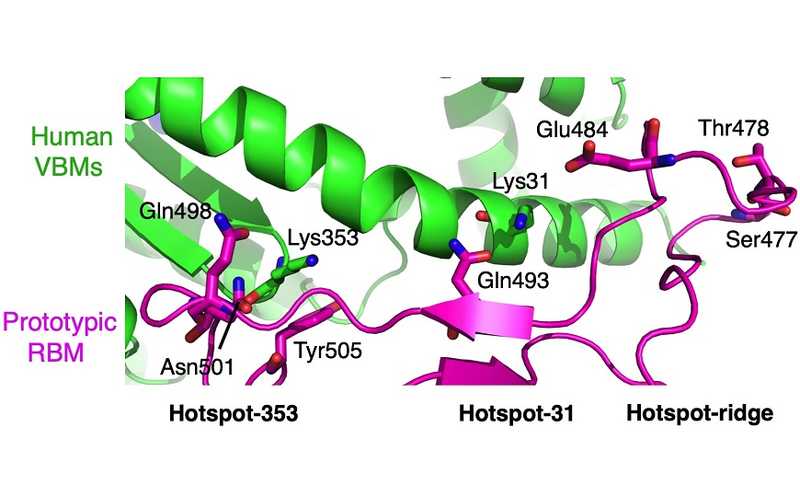
Структурная модель области взаимодействия рецептор-связывающего мотива коронавируса (малиновый) и ACE2 клетки-хозяина (зеленый).
Credit:
PNAS 119(44), e2206509119 (2022) | Open Access
Поиск резервуара среди животных принципиально важен для понимания особенностей эволюции вирусов, в частности SARS-CoV-2, и предотвращения пандемий в будущем. Указанием на животное-хозяина могут быть особенности взаимодействия между рецептор-связывающим доменом (RBD) S-белка коронавируса и его рецептором на поверхности клетки — ангиотензин-превращающим ферментом 2 (ACE2). Например, большое сходство RBD коронавируса летучих мышей и прототипного штамма SARS-CoV-2, зафиксированного в провинции Ухань в 2019 году, было веским аргументом в пользу происхождения SARS-CoV-2 от коронавируса летучих мышей.
Когда SARS-CoV-2 начал циркулировать в человеческой популяции, в структуре его RBD стали накапливаться мутации, способствующие ускользанию вируса от иммунного ответа. В настоящее время в человеческой популяции доминирует штамм омикрон. Два генетических варианта этого штамма, BA.2 и BA.1, были обнаружены примерно в одно и то же время осенью 2021 года, но вскоре BA.2 стал более распространенным во многих частях мира. Штамм омикрон имеет гораздо больше мутаций в сравнении со всеми предыдущими вариантами SARS-CoV-2, что вызвало к жизни гипотезы об участии других видов млекопитающих в его возникновении и эволюции.
Чтобы восстановить эволюционные следы, оставленные мутациями в S-белке, научная группа из Университета Миннесоты исследовала адаптации RBD штамма омикрон к ACE2 человека и ACE2 мыши — двух возможных источников его происхождения. Ранее эта научная группа уже показала «горячие точки» взаимодействия RBD коронавируса с ACE2 клетки-хозяина. Исследователи выделили две области, в которых часто происходят мутации, с центрами в аминокислотных остатках Lys31 и Lys353, и рецептор-связывающий гребень. Примечательно, что в случае омикрона только часть мутаций усиливает взаимодействие RBD с ACE2 человека, а другие мутации ослабляют его.
В новой работе исследователи проанализировали взаимодействие между RBD омикрона и мышиным ACE2, сосредоточив внимание на четырех мутациях в «горячих точках» (Q493R, Q498R, N501Y и Y505H). Сначала они исследовали методом поверхностного плазмонного резонанса (ППР) взаимодействие вируса и рецептора. Затем в RBD штамма омикрон внесли обратные мутации, обусловившие возвращение к прототипному варианту (R493Q, R498Q, Y501N и H505Y), и оценили влияние замен на аффинность к мышиному ACE2. Аффинность снизилась — иными словами, мутации, свойственные омикрону, усиливают взаимодействие с мышиным рецептором.
Для подтверждения данных ППР авторы исследовали проникновение псевдовирусных частиц в клетки, экспрессирующие на своей поверхности мышиный ACE2. Псевдовирусные частицы на основе ретровируса содержали S-белок омикрона, причем исследователи сконструировали четыре разных псевдовируса, каждый из которых имел одну из обратных мутаций. Эффективность проникновения в клетки, экспрессирующие мышиный ACE2, была снижена у всех четырех псевдовирусов. Таким образом, все исследуемые мутации штамма Омикрон способствуют взаимодействию с мышиным рецептором.
Основываясь на своих предыдущих разработках, авторы сконструировали химерный RBD, содержащий сердцевину от вируса SARS-CoV-1 и активный рецептор-связывающий мотив от штамма омикрон, а также химерный ACE2, имеющий три вирус-связывающих мотива мышиного ACE2 и базу в виде человеческого ACE2. Затем получили кристаллы комплекса RBD с рецептором, чтобы изучить детали их взаимодействия методом рентгеноструктурного анализа. Оказалось, что «горячие точки» стабилизировали центральную и боковую области контакта. В целом, изучаемые мутации структурно мало совместимы с человеческим ACE2, но хорошо адаптированы к мышиному ACE2.
«Передача коронавирусов от животных к человеку, вероятно, будет и впредь угрозой для глобального здоровья. Есть предположение, что все коронавирусы, циркулирующие среди людей, произошли от животных», — отметил ведущий автор статьи доктор Фан Ли, директор центра по изучению коронавирусов Университета Миннесоты. Дальнейший эпидемиологический мониторинг вариантов SARS-CoV-2, циркулирующих среди мышей и других грызунов, может прояснить вопросы, связанные с эволюцией и трансмиссией вируса в человеческую популяцию.
Источники
Zhang, W. et al. Structural basis for mouse receptor recognition by SARS-CoV-2 omicron variant // PNAS 119(44), e2206509119 (2022), published online October 18, 2022. DOI: 10.1073/pnas.2206509119
Цитаты по пресс-релизу


 Меню
Меню





 Все темы
Все темы




 0
0











