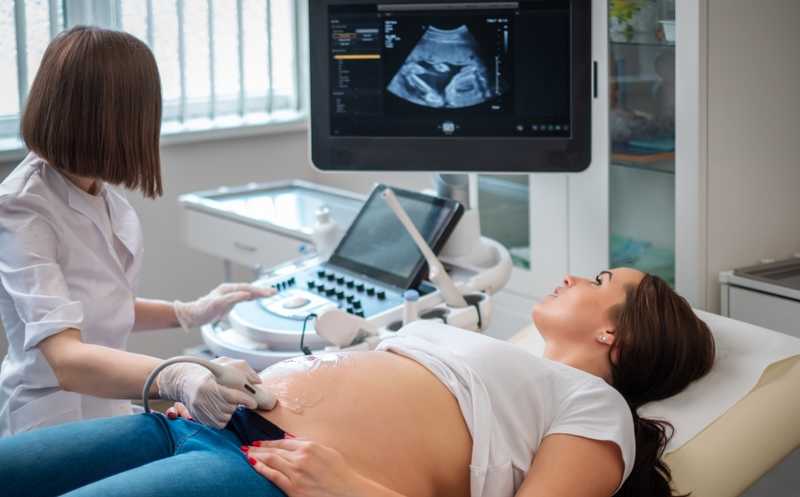
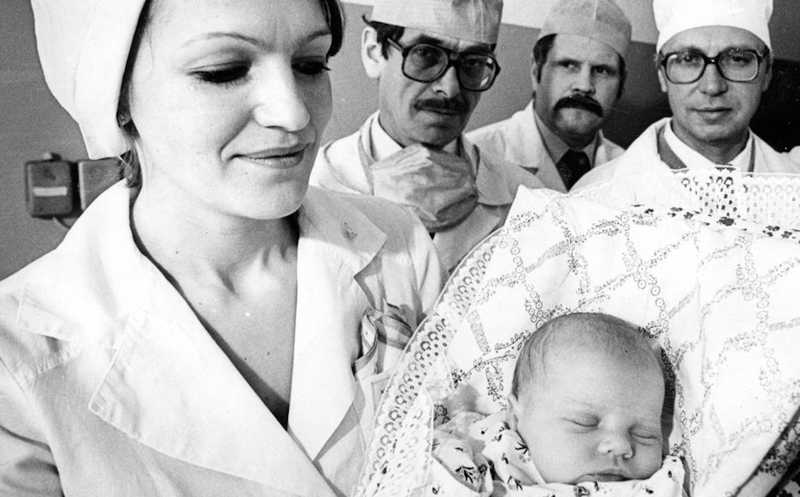
Чтобы начать диагностику наследственного заболевания, его надо сначала заподозрить
16 февраля на площадке московского технопарка «Медтех» состоялась конференция «Генетические технологии в диагностике и лечении заболеваний». Специалисты обсудили предотвращение и диагностику наследственных заболеваний, полигенные риски психоневрологических расстройств и возможности секвенирования в онкологии.

На церемонии открытия Сергей Куцев, академик РАН, главный внештатный специалист Минздрава России по медицинской генетике и директор МГНЦ им. Бочкова, подчеркнул необходимость публично заявлять о существующих проблемах, так как это способствует их решению. В качестве примеров успешных кейсов он привел расширение неонатального скрининга до 36 нозологий и образование фонда «Круг добра», который обеспечивает препаратами пациентов с орфанными заболеваниями.
По словам Куцева, особенность орфанных заболеваний в том, что каждое из них по отдельности встречается очень редко, но в совокупности их частота достигает 5%. Следующим шагом в их мониторинге и менеджменте должен стать единый регистр российских пациентов с орфанными заболеваниями. Специалисты уже работают над ним.
Спикер также отметил, что необходимо подбирать метод диагностики в зависимости от типа заболевания. Так, для нервно-мышечных нарушений лучше подходят экзомные и полногеномные исследования, при подозрении на лизосомные болезни накопления целесообразно в первую очередь оценить активность маркерных ферментов с помощью тандемной масс-спектрометрии, а выявление ряда аутовоспалительных заболеваний используются NGS-панели. Программы селективной диагностики наследственных болезней работают в МГНЦ.
 Credit: Денис Зыбин | Medtech.moscow
Credit: Денис Зыбин | Medtech.moscow
Первая сессия была посвящена генетическим технологиям, сопровождающим деторождение. Ее открыла Жанна Глинкина, генеральный директор Центра генетических исследований «Хайтек Генетикс», докладом о современном состоянии преимплантационного генетического тестирования (ПГТ).
Для ПГТ у эмбриона в возрасте 5 дней, полученного при ЭКО, отбирают несколько клеток. Многие мамы переживают за сохранность эмбриона и сомневаются в необходимости биопсии и ПГТ, но Глинкина пояснила, что на этом сроке эмбрион обладает мощной способностью к регенерации, поэтому процедура не травматична для него. Опасной может быть повторная биопсия, так как после первой биопсии эмбрион замораживают, и новый цикл разморозки и заморозки снижает его потенциал.
NGS-технологии позволяют проанализировать все хромосомы эмбриона одновременно. Исследователь получает информацию об анеуплоидиях, делециях и дупликациях внутри хромосом, а также хромосомных транслокациях. Докладчица отметила, что вспомогательные репродуктивные технологии, в том числе ПГТ, могут рассматриваться как способ родить здорового ребенка при генетических аномалиях, а не при бесплодии. Она привела в пример сознательную семью, первый ребенок в которой оказался болен, и при планировании второго ребенка семья прибегла к ЭКО. С помощью ПГТ также можно уточнить кариотип родителей. Неточности анализа, как правило, связаны с мозаицизмом эмбриона. Оно является вариантом нормы, но родителей необходимо информировать о нем перед тестированием.
По мнению Глинкиной, при отсутствии прямых медицинских показаний к ПГТ, связанных с генетическими аномалиями, вопрос о его необходимости следует решать отдельно в каждом конкретном случае.
Следующей выступила Елена Баранова, медицинский директор ООО «Эвоген». Ее доклад был посвящен неинвазивному пренатальному тестированию (НИПТ). Она сделала обзор существующих НИПТ. Есть тесты, которые определяют риски только самых распространенных анеуплоидий (по 21, 18 и 13 хромосомам). Есть анализы с дополнительными опциями, в том числе полногеномные. Баранова отметила, что это скрининговые тесты, а не диагностические, их результаты требуют подтверждения, но для скрининга их чувствительность и специфичность достаточно высоки.
Согласно приказу ДЗМ от 30 ноября 2021 г. № 1181 «Об организации проведения современных молекулярно-генетических исследований в городе Москве беременным женщинам и супружеским парам с отягощенным анамнезом» НИПТ проводится тем пациенткам, для которых высок риск хромосомных аномалий по результатам пренатального скрининга I триместра. Однако Баранова считает, что неправильно тестировать только группы риска.
Сессия продолжилась выступлением Дмитрия Трофимова, директора Института репродуктивной генетики НМИЦ АГП им. В.И. Кулакова. Он представил предварительные итоги проекта экзомного скрининга новорожденных «ЭКЗАМЕН». Проект работал на базе НМИЦ с мая 2021 г. по декабрь 2022 г. К настоящему времени получено более 10 000 образцов; обработаны 7 583 экзома. Исследовались кодирующие и регуляторные области, а также сайты сплайсинга для примерно 22 000 генов. Промежуточные результаты проекта были озвучены на конференции NGS-2022.
По результатам экзомного секвенирования можно определить причины имеющегося заболевания, спрогнозировать риск моногенных заболеваний и подобрать терапию. Если человек условно здоров, экзомный анализ позволяет выявить 99% известных генетических вариантов. Если анализируется человек с патологией, экзом дает информацию об особенностях фенотипа в 94% случаев.
В рамках проекта у новорожденных отбиралась пуповинная кровь со стороны плаценты. Экзомное секвенирование выполнялось на платформе Illumina NoveSeq 6000. При анализе выявленных вариантов использовались базы HGMD, ClinVar, OMIM и другие. Обработку результатов выполняли с помощью собственного ПО. Условно здоровых новорожденных направляли только на скрининг; в их экзомных данных искали только патогенные варианты. Новорожденные с особенностями фенотипа проходили экзомный скрининг и расширенные исследования, для них определяли патогенные варианты и варианты с неопределенной значимостью.
В период работы «ЭКЗАМЕНа» поучаствовать в проекте предлагали всем пациентам, поступившим в НМИЦ АГП им. Кулакова; дали согласие 82%. Из пациентов, согласившихся на расширенное исследование, 85,2% дали согласие на выявление вариантов высокого риска, связанных с заболеваниями, для которых нет лечения; 85,6% захотели узнать о вариантах средней пенетрантности; 85,4% согласились получить информацию о рисках для других членов семьи; 83,8% дали согласие на хранение данных для повторного анализа.
Из 7 583 новорожденных 7 000 были условно здоровыми, у 583 были врожденные или перинатальные заболевания. В первой группе было обнаружено 96 мутаций в экзонах, 13 хромосомных аномалий. Во второй группе количество находок составляло 77 и 45, соответственно. Таким образом, всего была сделана 231 находка, из которых только 8 входят в расширенный скрининг на 36 заболеваний.
В рамках проекта были выявлены 39 не описанных ранее мутаций в генах, ассоциированных с моногенными заболеваниями и 3 гена, ранее не ассоциированные с моногенными заболеваниями. Так, ген KCNJ9 оказался связан с неонатальными судорогами, TOPBP1 — с врожденной микроцефалией, HIRA — предположительно с синдромом Ди Джорджи. Частота носительства аутосомно-рецессивных моногенных заболеваний составила 88,5%. Из всех детей 1,5% несли варианты, связанные с риском заболевания во взрослом возрасте.
Трофимов отметил, что экзомный скрининг не только помогает выявить заболевание, но также дает информацию для планирования следующих беременностей, а именно для пренатального и преимплантационного генетического тестирования. То есть речь уже идет о профилактике моногенных заболеваний. Если выявлен риск курабельных заболеваний с поздним началом, можно своевременно начать специфическое лечение, не пропустить терапевтическое окно и не допустить необратимых последствий. Это, в частности, касается таких расстройств, как нейросенсорная тугоухость, синдом Марфана, туберозный склероз и др.
Несмотря на явные преимущества экзомного скрининга, его внедрение в клинику осложнено рядом этических и правовых вопросов. Так, необходимо провести грань между профилактикой генетических заболеваний и селекцией человека, точно определить цели скрининга — поиск мутаций, связанных с тяжелой патологией, либо основание для персонализированной медицины с рождения. Еще одна проблема — правовые аспекты обращения с генетической информацией как с персональными данными. В экзоме ребенка зашифрованы и риски заболеваний для других членов семьи, но в настоящее время нет юридической ясности, можно ли раскрыть эту информацию семье.
После Дмитрия Трофимова выступила Ольга Щагина, заведующая лабораторией в МГНЦ им. Бочкова. Она рассказала об особенностях диагностики наследственных болезней, которые определяются целью диагностики и природой заболевания. Метод генетического анализа будет выбран исходя из того, что нужно найти. Например, для поиска частых мутаций и анализа единичных генов подойдут ПЦР в реальном времени или секвенирование по Сэнгеру. Если же нужно охватить большой участок генома, можно обратиться к полногеномному, полноэкзомному, полнотранскриптомному анализам или к кастомным генным панелям.
Затрудняют постановку верного диагноза генетическая гетерогенность наследственных заболеваний, клинический полиморфизм проявлений вариантов одного гена, а также ошибки специалистов на разных этапах ведения пациента.
В качестве примера относительно простого для диагностики заболевания Ольга Щагина рассмотрела СМА 5q, вызванную мутациями в гене SMN1. Гораздо сложнее дело обстоит с наследственными заболеваниями сетчатки, за которые могут отвечать множество генов. Щагина рассказала об исследовании с участием 169 пациентов, выполненном с помощью 162-генной кастомной NGS-панели. В результате было обнаружено 80 патогенных и вероятно патогенных вариантов в 32 генах. Еще один пример — оптимизация панели для диагностики периферической нейропатии. Специалисты МГНЦ, основываясь на результатах собственных исследований и опубликованных данных, расширили коммерческую панель с 15 до 21 гена, причем один ген из исходной панели убрали.
В дискуссии после доклада была названа одна из важных проблем диагностики наследственных заболеваний: чтобы начать диагностику заболевания, его надо сначала заподозрить. В настоящее время существуют клинические рекомендации по диагностике отдельных болезней. Разработка универсальных клинреков вряд ли возможна.
Виктория Воинова, зам. директора по трансляционной медицине НИКИ педиатрии и детской хирургии им. Вельтищева ФГБОУ ВО РНИМУ им. Пирогова, в своем докладе смоделировала диалог между врачом-генетиком и детским кардиологом о преимуществах и эффективности генетического анализа для выявления наследственной патологии. В докладе были освещены сильные и слабые места клинического секвенирования. Воинова рассказала о терапии генетических заболеваний, в том числе о персонализированном лечении с помощью антисмысловых олигонуклеотидов. Она срабатывает в тех случаях, когда блокирование мутантного аллеля может восстановить нормальный фенотип.
По словам Воиновой, 9 февраля в НИКИ им. Вельтищева была введена первая доза отечественного генотерапевтического препарата против СМА. Ребенок чувствует себя хорошо.
Завершил первую сессию доклад генерального директора ООО «Генотек» Валерия Ильинского о работе, выполненной на 150 000 геномов жителей России. Он отметил, что для гисследований ученые часто стремятся сформировать выборку неродственных друг другу людей. Однако чем больше выборка, тем выше шанс найти в ней родственников, поэтому стоит корректировать результаты исследований с учетом степени родства. Установить ее поможет генетический анализ.
Еще один важный пункт — этническая принадлежность, так как распространенность заболеваний в разных этносах неодинакова. Проверить происхождение можно, используя полигенные и другие индексы, которые рассчитываются при анализе больших генетических баз.
 Дмитрий Трофимов. Credit: Денис Зыбин | Medtech.moscow
Дмитрий Трофимов. Credit: Денис Зыбин | Medtech.moscow
Вторая сессия была посвящена генетическим технологиям в лечении заболеваний. Спикеры обсуждали в основном применимость этих технологий к выявлению и терапии неврологических и психических расстройств. Артем Шарков, научный сотрудник НИКИ педиатрии и детской хирургии им. Вельтищева, рассказал о взгляде неврологов на генетические методы. Он отметил, что 80% генов активно экспрессируются в ЦНС и более 40% генетических заболеваний имеют неврологические симптомы.
Генетические технологи помогают диагностировать редкие неврологические отклонения и направить терапию. Информация о поломках в определенных генах позволяет модифицировать симптоматическое лечение и, в некоторых случаях, перенацелить уже известные препараты. Так, при GRIN-ассоциированных эпилепсиях происходят изменения структуры рецептора NMDAR. Если мутация привела к приобретению функции, заблокировать патогенный NMDAR можно с помощью декстрометорфана, который присутствует в сиропе от кашля, или мемантина, который используется при деменциях, ассоциированных с болезнью Альцгеймера. Если же мутация связана с потерей функции, скорректировать состояние пациента можно, добавляя в схему лечения L-серин. Шарков также рассказал о терапии метаболических эпилепсий и современном состоянии генной терапии неврологических расстройств.
Александр Кибитов, главный научный сотрудник Института трансляционной психиатрии, представил результаты поиска маркеров высокого риска депрессии в российской популяции. GWAS — хороший метод для подобных исследований, но он требует больших выборок. Команда Кибитова поставила задачу разработать полигенные шкалы на основе полногеномного исследования с клинической валидацией. Однако Россия большая, охватить всю страну генетическим анализом не представляется возможным. Вместе с тем данных по психиатрической генетике в стране нет. Поэтому ученые протестировали концепцию онлайн-фенотипирования.
Сначала они провели онлайн-анкетирование о симптомах депрессии в популяционной выборке, состоящей из 4 520 клиентов компании «Генотек», и определили 14 фенотипов. Для каждого фенотипа провели независимый GWAS. На основе результатов GWAS для каждого фенотипа был сформирован индекс полигенного риска. Индексы валидировали на небольшой клинической когорте, состоящей из пациентов с подтвержденным диагнозом и здоровых контролей. Эту когорту набрали в шести медицинских центрах Москвы, Санкт-Петербурга, Уфы и Ростова-на-Дону. В целом все предложенные фенотипы оказались специфичными и эффективными, хоть и в разной степени. Авторы планируют валидацию полигенных индексов на расширенной клинической выборке.
Главный внештатный специалист-психиатр ДЗМ и главный врач ГБУЗ «ПКБ № 1 ДЗМ» Георгий Костюк отметил несоответствие общемировой и российской статистик. В России официальная распространенность болезни Альцгеймера и РАС не превышает сотых долей процента, что в десятки раз ниже, чем в среднем по миру. В настоящее время ведется поиск оптимальных маркеров психических расстройств. Диагнозы в этой сфере чаще всего ставятся на основании беседы врача с пациентом, но такой способ нельзя назвать объективным. Генетические и метаболические маркеры могли бы обеспечить объективность. Так, ведется исследование связи липидов крови с риском шизофрении.
Болезнь Альцгемера в России диагностируется плохо — по словам Костюка, это связано с особенностями системы здравоохранения. Коллега Костюка Анна Морозова рассказала о наборе реагентов «Биочип-А» для определения генетического риска заболевания. Набор разработан специалистами из ГБУЗ «ПКБ № 1 ДЗМ» и ИМБ им. Энгельгардта в рамках московской программы поддержки научных разработок и инноваций в сфере медицины. К набору прилагаются флуоресцентный анализатор и ПО. Анализ проводится по 21 генетическому маркеру и полиморфизмам rs429358 и rs7412, определяющим аллели гена APOE.
На сессии также выступил Павел Волчков, исполнительный директор Центра живых систем МФТИ. Он рассказал о генетическом риске развития и современных методах терапии диабета 1 типа. Сейчас это заболевание диагностируется уже после нарушения гликемического контроля, то есть в тот момент, когда в организме уже наступили необратимые изменения. Патогенные аутоантитела появляются до очевидных изменений. Если отследить моноклональные антитела на ранней стадии, с болезнью можно справиться, например, с помощью иммуносупрессии. Но проверять всех подряд на антитела невозможно, чтобы внедрить такой подход, необходимо сначала сузить выборку. Потенциально это можно сделать с помощью генетического анализа, однако генетическая архитектура диабета 1 типа сложна для изучения. В частности, не существует оптимальной мышиной модели. Попытка решить эту проблему была предпринята в рамках проекта T1DGC, но пока существующая оценка генетического риска заболевания далека от совершенства. В дискуссии после доклада поднялся вопрос о том, насколько полигенные заболевания действительно полигенны. По словам Волчкова, в экспериментах на мышах было показано, что полигенные заболевания часто оказываются моно-, ди- и тригенными.
 Александр Кибитов. Credit: Денис Зыбов | Medtech.moscow
Александр Кибитов. Credit: Денис Зыбов | Medtech.moscow
Участники третьей сессии обсудили московский проект, посвященный полногеномному секвенированию онкопациентов с целью выявления и изучения наследственного опухолевого синдрома (НОС). Проект утвержден приказом ДЗМ № 69 от 01.02.2021 и работает на базе нескольких учреждений, в том числе ГБУЗ «ГКОБ № 1 ДЗМ» и МКНЦ им. Логинова. Все образцы накапливаются ГКОБ № 1 ДЗМ и отправляются на секвенирование в компанию «Эвоген». Анастасия Данишевич, врач-генетик и врач-онколог МКНЦ, отметила, что из всех онкогенетических исследований в ОМС пока включен только анализ BRCA 1/2. Пройти другие генетические тесты можно либо платно, либо в рамках научных исследований, подобных московскому проекту.
Данишевич представила результаты проекта для пациентов с раком молочной железы. В исследовании приняли участие пациенты с РМЖ младше 50 лет, либо с двусторонним РМЖ, либо с отягощенным семейным анамнезом. Секвенирование осуществлялось на платформе MGI. Было получено 1800 полных геномов. Специалисты определяли спектр герминальных мутаций и долю НОС среди всех случаев рака. При выявлении патогенных и вероятно патогенных вариантов проводили подтверждение с помощью секвенирования по Сэнгеру, вызывали родственников 1 и 2 степени родства и предоставляли им генетическое консультирование. Чаще всего обнаруживались мутации в BRCA 1/2. НОС составили 12,5% среди всех случаев РМЖ.
Заведующая центром патологоанатомической диагностики и молекулярной генетики ГБУЗ «ГКОБ № 1 ДЗМ» Анна Семенова рассказала об одном из этапов проекта — создании «Кабинета наследственной патологии». Этот этап предполагает создания регистра людей с наследственной патологией и здоровых людей с опасными герминальными мутациями и формирование мультидисциплинарной команды врачей, включающей онколога, медицинского психолога и медицинского генетика.
Мария Макарова, руководитель направления онкогенетики ООО «Эвоген», напомнила, что полногеномное тестирование — это не только помощь пациентам, но и возможность фундаментальных исследований, по результатам которых будут созданы новые генетические тесты. Руководитель биоинформатической службы ЦГРМ «Генетико» Дарья Хмелькова обсудила особенности интерпретации NGS-данных при НОС. Важно отслеживать, какая информация войдет в заключение для пациента. В настоящее время принято сообщать о патогенных и вероятно патогенных вариантах, а также о вариантах с неопределенной значимостью, однако надо учитывать, что последние в 75–90% случаев позже переклассифицируются в безвредные. О доброкачественных вариантах сообщать не нужно. Кроме того, Хмелькова предлагает ввести презумпцию невиновности для миссенс-вариантов и других мутаций, не связанных с потерей функции.
Доклад Александра Ракитько (ООО «Генотек») о полигенных рисках рака спровоцировал дискуссию. По мнению Марии Макаровой, полигенные риски не применимы в клинике и их показатели завышены. Ракитько же считает, что на полигенные риски стоит обратить внимание, так как растет посвященныйим объем научной литературы.
Завершил третью сессию старший научный сотрудник НИИ трансляционной медицины РНИМУ им. Пирогова Андрей Зарецкий. Он рассказал об анализе соматических мутаций при солидных злокачественных опухолях. Такой анализ позволяет определить происхождение опухоли (первичная или метастаз), провести дифференциальную диагностику и установить тип и подтип клеток-предшественников.
 Credit: Денис Зыбов
Credit: Денис Зыбов
В рамках конференции также состоялся круглый стол «Биоэтика в генетике: оценка рисков и пользы».


 Меню
Меню





 Все темы
Все темы




 0
0