EASYPREP: жидкостная цитология против рака шейки матки
В России скоро появится EASYPREP от корейской компании YD Diagnostics — первая в мире полностью автоматизированная система пробоподготовки для жидкостной цитологии на основе технологии клеточного обогащения. Одно из самых важных применений жидкостной цитологии — массовый скрининг на рак шейки матки с целью раннего выявления предраковых изменений и снижения смертности среди женщин.

YD Diagnostics
Рак, который можно победить
В ноябре 2020 года Всемирная организация здравоохранения (ВОЗ) представила Глобальную стратегию по ускорению темпа ликвидации рака шейки матки (РШМ). Пока он остается четвертым по распространенности онкологическим заболеванием среди женщин в мире. Это достаточно «молодой» вид рака, чаще всего он встречается у женщин среднего возраста (35–55 лет). В отсутствие дополнительных мер по борьбе с РШМ ежегодная численность новых случаев, как ожидается, с 2018 по 2030 годы вырастет с 570 000 до 700 000, а ежегодное количество смертей — с 311 000 до 400 000.
Подавляющее большинство случаев РШМ связано с папилломавирусной инфекцией, при этом за 70% случаев отвечают два подтипа папилломавируса человека: ВПЧ16 и ВПЧ18.
В конце XX — начале XXI века распространенность ВПЧ среди женщин без признаков онкологических заболеваний достигала 11,7%. В странах Восточной Европы инфицирован примерно каждый пятый человек. В большинстве случаев инфицирования иммунная система уничтожает вирус самостоятельно, однако, если он проникает в клетки эпителия, то интеграция вирусного генома в ядерную ДНК может привести к злокачественной трансформации.
Хорошая новость состоит в том, что профилактика РШМ в мире достигла больших успехов. Заболеваемость и смертность снижаются благодаря вакцинации, ранней диагностике предраковых изменений, а также современным методам лечения. Как результат, в странах с высоким уровнем дохода заболеваемость РШМ почти в два раза ниже, а смертность в три раза ниже, чем в странах низким и средним уровнями дохода.
В соответствии с планом ВОЗ необходимо вакцинировать 90% девочек до 15 лет; проводить профилактическое обследование не менее 70% женщин в возрасте 35 и 45 лет и обеспечить лечение 90% женщин с установленным диагнозом. Если удастся достичь этих показателей, то к середине века заболеваемость РШМ сократится на 40% и будут предотвращены 5 миллионов смертей.
Для решения второй из трех задач, поставленных ВОЗ, — массовой диагностики предраковых изменений у женщин — необходим организованный скрининг. Рак шейки матки — один из немногих видов злокачественных новообразований, которые удовлетворяют всем требованиям для проведения популяционного скрининга: это широко распространенное заболевание, представляющее серьезную проблему для здравоохранения и экономики государства; оно имеет чётко распознаваемую преклиническую фазу и длительный период развития (10-15 лет); существуют надежные скрининговые тесты, а также возможности для дальнейшей верификации диагноза и эффективного лечения.
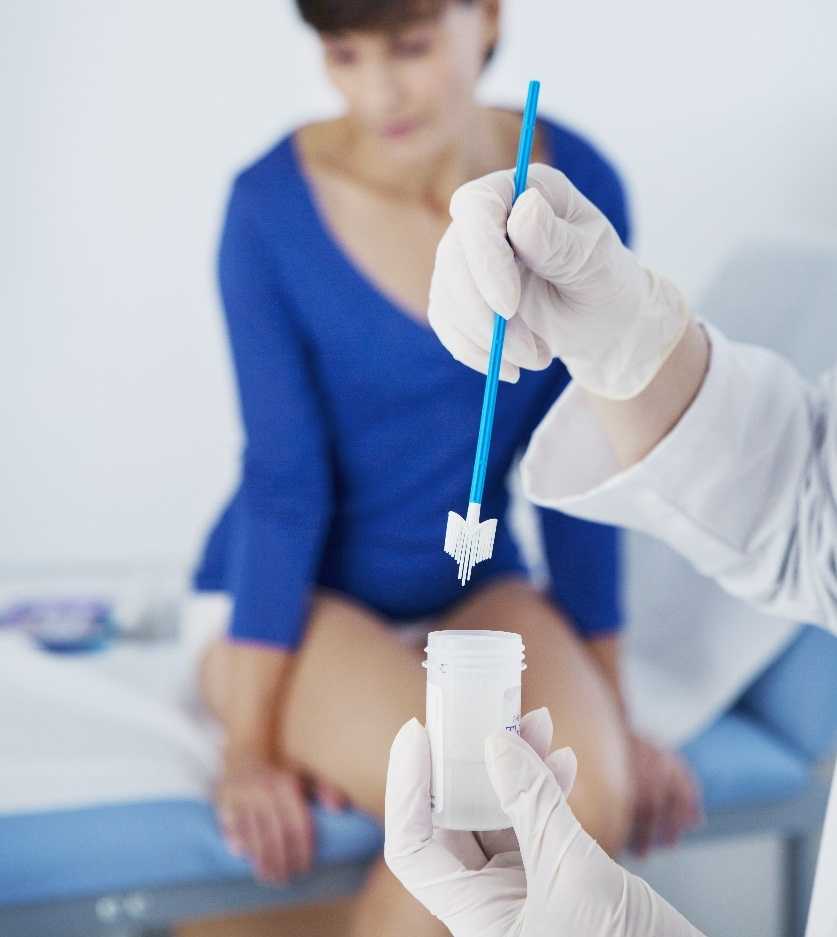
Традиционно в качестве скринингового теста на РШМ выбирается цитологическое исследование. Как оно выполняется? Аномальные клетки эпителия выявляют с помощью мазка по Папаниколау (Пап-мазок): образец собирают маленькой щеточкой с поверхности шейки матки, наносят на предметное стекло, быстро фиксируют, затем окрашивают и микроскопируют. Современная альтернатива классическому Пап-мазку — жидкостная цитология: образец помещают в жидкую среду, которая стабилизирует клетки, затем центрифугируют либо фильтруют и только после этого «отмытые» клетки наносятся на стекло. Жидкостная цитология может дополняться молекулярной диагностикой ВПЧ.
 Credit: Shutterstock.com
Credit: Shutterstock.com
Впервые (с 1949 года) цитологический скрининг РШМ начали проводить в канадской провинции Британская Колумбия. В 50-х годах программы скрининга появляются в США и Китае, с начала 60-х годов — в Японии, Финляндии, Швеции, Исландии, с начала 70-х годов — в Германии, Бразилии и других странах. На рубеже 70-х-80-х гг. скрининг РШМ был организован и в СССР; в стране создали десятки централизованных цитологических лабораторий. Благодаря этим мерам заболеваемость за 25 лет — с 1965 по 1989 гг. — снизилась на 53,1%.
К сожалению, Россия не переняла эту практику. Сейчас у нас не существует национальной программы скрининга РШМ, и пока невозможно сказать, когда она появится. В некоторых регионах действуют региональные программы, а кроме того, цитологическое исследование можно сделать в рамках диспансеризации или на платной основе. При этом в России злокачественные новообразования шейки матки стабильно занимают 5-е место (примерно каждый двадцатый случай) в структуре онкологической заболеваемости женщин. В 2018 году было выявлено 17 766 случаев, что на 22,3 % больше, чем в 2008-м (13 807 случая). Растет доля женщин репродуктивного возраста с диагнозом РШМ. В 2017 году удельный вес этого вида рака среди злокачественных опухолей репродуктивных органов у женщин до 40 лет составил 62,2%.
В возрастной группе 15–29 лет заболеваемость РШМ увеличилась в 5,3 раза по сравнению с 1990 годом, а смертность, несмотря на появление новых технологий терапии, возросла вдвое — с 11,44 до 23,43 случаев на 100 000 женщин. (С более подробными статистическими данными можно ознакомиться здесь.) После лечения многие молодые женщины теряют способность к деторождению.
Кроме потери многих жизней, высокая заболеваемость и смертность от РШМ приводит и к существенным экономическим потерям. Совокупный непрямой экономический ущерб вследствие смертей от РШМ составляет почти 46,5 млрд руб. в год, Специалисты давно говорят о необходимости национальной и региональных программ по предупреждению РШМ в России.
ВОЗ рекомендует включать в скрининговые программы всех женщин старше 30 лет, однако многие страны начинают скрининг с 20 лет — во время наибольшей активности репродуктивной системы. В результате общее количество заболеваний снижается, а среди заболевших увеличивается количество пациенток с ранними стадиями. (Хотя необходимо отметить, что полностью победить РШМ пока не смогла даже Финляндия, где охват скринингом женщин в возрасте от 30 до 60 превышает 90%.)
Автоматизация — в помощь врачам
Большие объемы тестирования, необходимые для скрининга в масштабах страны, требуют автоматизации, и здесь жидкостная цитология получает дополнительное преимущество перед традиционным Пап-тестом. Образец в жидкой среде можно не только хранить длительное время и выполнять повторные мазки. Менее вероятно появление артефактов из-за высыхания клеток, удаляются элементы, мешающие микроскопии (слизь, лейкоциты, эритроциты). В результате на стекле образуется монослой хорошо различимых клеток.
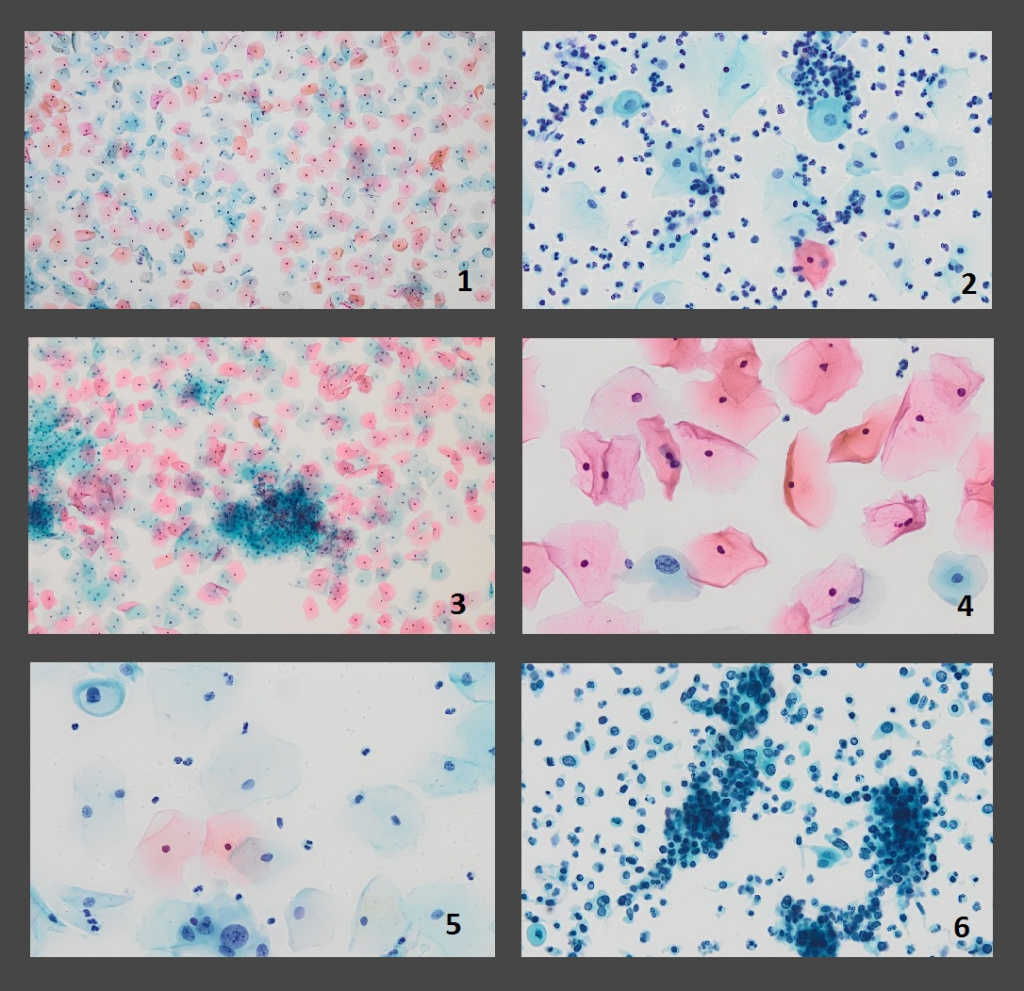 Микрофотографии мазков, полученные с помощью системы EASYPREP YD Diagnostics: 1 —негативный образец (100х), 2 — воспаление (400х), 3 — Candida (400x), 4 — поражение низкой степени риска (ASCUS, 400х), 5 — дисплазия (HSIL, 400х), 6 — плоскоклеточная карцинома (400х). Credit: YD
Микрофотографии мазков, полученные с помощью системы EASYPREP YD Diagnostics: 1 —негативный образец (100х), 2 — воспаление (400х), 3 — Candida (400x), 4 — поражение низкой степени риска (ASCUS, 400х), 5 — дисплазия (HSIL, 400х), 6 — плоскоклеточная карцинома (400х). Credit: YD
Автоматизация пробоподготовки по жидкостному методу существенно увеличивает чувствительность исследования по сравнению с традиционной цитологией, потому что количество неадекватных препаратов снижается в несколько раз, а кроме того, исключается риск допустить ошибку — человеческий фактор сводится к минимуму. Возможно автоматизировать и процесс «просмотра» стекол — сканирующие микроскопы и специальное программное обеспечение, в основе которого лежит искусственный интеллект, проводят оцифровку, преклассификацию и архивацию препаратов.
По оценкам, опубликованным в сентябре 2020 года, объем мирового рынка цитологии и тестирования на ВПЧ в 2019 году составлял $7,87 млрд, а к 2027 году вырастет в 1,6 раз. Цитологические исследования в 2019 году занимали самую большую долю рынка — более 67%, и в основном за счет тестирования на РШМ. Это объясняется большим количеством «классических» Пап-тестов, однако рост ожидается в том числе из-за увеличения спроса на высокотехнологические методы тестирования. Поэтому ведущие мировые производители медицинского оборудования, в том числе Becton Dickinson, Hologic, Biodyne, предлагают автоматизированные решения.
ThinPrep, SurePath, EASYPREP
Разные системы автоматизированной пробоподготовки отличаются, в частности, методом перенесения клеток из жидкости на стекло. В конце 1990-х — начале 2000-х, когда жидкостная цитология только появилась, многие разработчики предпочитали метод фильтрации из-за простоты и невысокой стоимости: жидкость из флакона удаляют через фильтр с применением вакуума, клетки собираются на фильтре, который затем прижимается к предметному стеклу. Такой метод реализован, например, в ThinPrep от Hologic.
Однако клетки, особенно незрелые и метапластические, деформируются, когда давление прижимает их к фильтру. Кроме того, процесс фильтрации затрудняет слизь, которую в большом количестве секретируют клетки цервикального канала и влагалища.
Другой способ использует система пробоподготовки SurePath от Becton Dickinson (BD): образец наслаивают на реагент, создающий градиент плотности, центрифугируют, отделяя целевые клетки от посторонних примесей, а затем наносят на предметное стекло. В России наибольшее распространение получила именно эта технология — Becton Dickinson сейчас занимает наибольшую долю рынка.
В системах EASYPREP производства корейской компании YD Diagnostics также реализована технология клеточного обогащения на градиенте плотности. Весь процессинг автоматизирован — от загрузки образцов, реагентов и расходных материалов до получения готового тонкослойного препарата. Кроме того, на EASYPREP можно одновременно подготавливать как гинекологические образцы, так и негинекологические: моча, слюна, ликвор, выпоты серозных полостей, а также материалы, полученные с помощью тонкоигольной аспирационной биопсии.
 Автоматизированная система пробоподготовки EASYPREP | Credit: YD Diagnostics
Автоматизированная система пробоподготовки EASYPREP | Credit: YD Diagnostics
В целом системы пробоподготовки от различных производителей не особенно сильно различаются по качеству образцов. Однако метаанализ работ, в которых сравнивалась доля мазков неудовлетворительного качества, выявил преимущество SurePath перед ThinPrep: 0,3% против 1,3%.
В нескольких работах корейских авторов сравниваются EASYPREP и SurePath. Так, сопоставимую диагностическую ценность показало сравнение на 253 образцах щитовидной железы, полученных с помощью тонкоигольной аспирационной биопсии. В более обширном исследовании были собраны мазки с поверхности шейки матки у 1000 пациенток, а затем исследованы с помощью EASYPREP и SurePath. Согласованность методов достигла 96,5%, а при использовании SurePath в качестве стандарта чувствительность, специфичность, положительная и отрицательная прогностическая ценность EASYPREP составили 90,7%, 99,2%, 94,8% и 98,5% соответственно.
Прибор работает без вас
У специалистов по клинической диагностике, конечно, возникают конкретные вопросы о том, чем одна автоматизированная система отличается от другой, и что может каждая из них. Об особенностях EASYPREP — системы новой для отечественного рынка — рассказывает Дерек Ли (Derek Lee), руководитель отдела маркетинга YD Diagnostics.
 Штаб-квартира YD Diagnostics. Йонъин-си, Кёнгидо, Республика Корея
Штаб-квартира YD Diagnostics. Йонъин-си, Кёнгидо, Республика Корея
Что можно сказать про «степень» автоматизации EASYPREP? В нем автоматизировано столько же этапов, сколько у SurePath, больше или меньше?
Система EASYPREP работает по принципу walk away: в ней автоматизированы все этапы пробоподготовки. Достаточно загрузить образцы, реагенты и расходные материалы, а на выходе получаются готовые препараты — окрашенные или не окрашенные. Система производства BD полуавтоматизированна — это значит, что отдельные этапы процессинга выполняются автоматически, но между этапами требуются ручные манипуляция оператора, такие как загрузка, разгрузка, перенос образцов и т.д. Здесь растет вероятность совершить ошибку.
Производительность работы системы достигает 64 теста в час — это так?
Верно, за один запуск EASYPREP может обрабатывать от 4 до 64 препаратов. Продолжительность рабочего цикла зависит от настроек протокола, и в среднем составляет от 1 до 1,5 ч при полной загрузке.
Возможно ли котестирование образцов молекулярными методами, например, параллельное генотипирование субтипов вируса с помощью ПЦР?
Да, из флаконов с консервирующим раствором EASYPREP возможно отобрать материал для выделения нуклеиновых кислот и далее исследовать его на ВПЧ или другие инфекции. Например, некоторые авторы предполагают возможное синергетическое действие ВПЧ и возбудителей хламидиоза (Chlamydia trachomatis) и гонореи (Neisseria gonorrhoeae) при прогрессировании поражений шейки матки. Такие работы подтверждают гипотезу о том, что некоторые заболевания, передающиеся половым путем, могут играть роль кофакторов в канцерогенезе шейки матки, опосредованном ВПЧ.
В EASYPREP осаждение клеток производится центрифугированием, а не вакуум-фильтрацией, как у ThinPrep от Hologic. Это не замедляет процесс по сравнению с ThinPrep? Похож ли метод на тот, что используется в SurePath от BD?
Действительно, жидкостная цитология на основе фильтрации может выполнять обработку материала быстрее — например, на системе Cellprep Plus от Biodyne при постоянном присутствии оператора можно подготовить до 120 препаратов в час, а производительность ThinPrep 5000 достигает примерно 20 препаратов за 40 минут. Однако сама технология фильтрации обладает некоторыми недостатками — многие пользователи отмечают, что «фильтры» не всегда хорошо справляются со слизью и кровью, обычно в обилии присутствующими в гинекологических образцах. Что касается технологии, реализованной в EASYPREP, она полностью аналогична SurePath от BD, только полностью автоматизирована.
Утверждается, что при центрифугировании не происходит потерь клеток, в отличие от фильтрования. За счет чего это достигается?
Это не совсем так. Клетки теряются при подготовке препарата традиционным способом — после нанесения материала на стекло щеточка утилизируется, а ведь на ней остается множество потенциально патологических клеток. В жидкостном методе головку щеточки со всем биоматериалом помещают в консервирующую среду, ни одна клетка не утилизируется, и риск упустить элементы неоплазии или рака устраняется.
Отдельный вопрос — выявление атипических железистых клеток. Жидкостной метод обладает меньшей или большей чувствительностью для выявления железистой патологии по сравнению с традиционным Пап-мазком?
Многие авторы утверждают, что чувствительность жидкостного метода значительно выше. В первую очередь это достигается меньшим количеством неадекватных препаратов, связанных с неправильной ручной обработкой в ходе традиционного метода.
Фиксация и окрашивание клеток: есть ли отличия от обычного Пап-теста?
Отличий нет: фиксацию проводят в 95%-ном спирте, окрашивание — по стандартным протоколам Папаниколау, в отдельно стоящих автоматических стейнерах либо при помощи встроенного в EASYPREP модуля окрашивания (что, однако, удлиняет продолжительность рабочего цикла). Большинство пользователей в Корее используют для окрашивания отдельные системы.
 Credit: 123rf.com
Credit: 123rf.com
«Молодые женщины не спешат обследоваться…»
На российском рынке систему EASYPREP представляет компания «ИнтерЛабСервис». Елизавета Мазурина, ведущий специалист по продукции компании, отвечает на вопросы PCR.NEWS.
Почему ваша компания решила вывести на российский рынок именно EASYPREP?
ИнтерЛабСервис традиционно фокусируется на комплексных решениях для лабораторий, отдавая предпочтение автоматизированным системам. Мы знаем, насколько велика нагрузка на медицинский персонал в современных клинико-диагностических центрах, поэтому стремимся максимально упростить рабочие процессы лаборатории, чтобы врачи могли сконцентрироваться на результатах. EASYPREP полностью соответствует нашим высоким требованиям и, мы уверены, что он станет достойным игроком на рынке.
Когда EASYPREP пройдет регистрацию и появится на рынке?
Ориентировочно через 2 месяца. Мы уже подали заявление в Росздравнадзор и сейчас находимся в процессе получения регистрационного удостоверения.
То есть, возможно, летом она уже станет доступна?
Да, верно.
Система более автоматизированная по сравнению с BD. А что можно сказать про обучение персонала работе на новом устройстве? Сложная ли это задача?
Нет, не очень сложная. Приезжает специалист, проводит настройку прибора с учетом того, как цитолог привык видеть готовое стекло под микроскопом, делает первые прогоны, а дальше пользователю остается только запускать протоколы самостоятельно, нажатием нескольких кнопок на сенсорном экране.
Первичную техподдержку обеспечиваете вы?
Да, как официальные дистрибьюторы компании YD Diagnostics на территории РФ.
Насколько велик сейчас российский рынок жидкостной цитологии?
Серьезных исследований на эту тему мне не встречалось, точные цифры назвать трудно. Однако в 27 регионах страны жидкостная цитология включена в ОМС, в том числе, например, в Москве, Санкт-Петербурге и многих других городах. Исследований уже сейчас выполняется довольно много.
Каков будет порядок величин, если мы возьмем всех женщин репродуктивного возраста и будем обследовать, как рекомендует ВОЗ, 70%? Или 90%, как в Финляндии?
Даже в хорошо развитых странах редко охват скринингом превышает 80% целевой группы. В той же Корее общий средний охват — чуть больше 50%, несмотря на то, что у них скрининг уже давно введен. И мы берем не только репродуктивный возраст. Даже в первую очередь берем женщин старшего возраста, от 55 и выше, потому что у них чаще встречается заболеваемость РШМ вне всякого рода профилактики. Если рассчитать примерно, то это женщины в возрасте от 20 до 65 лет, и обследования, по рекомендациям ВОЗ, раз в три года. Или раз в пять лет, если мы делаем совместный тест — цитология и молекулярная диагностика на ВПЧ.
Молекулярная диагностика на ВПЧ дает возможность делать больший промежуток?
Да, верно. Это снижает и психологический дискомфорт для пациенток, потому что женщины, конечно, хотели бы попадать на кресло к гинекологу как можно реже. Увеличение безопасного промежутка между обследованиями до пяти лет — это и для женщин хорошо, и для государства экономия средств.
В любом случае, это значительная часть населения России, десятки миллионов человек, которым нужно обследование, и не один раз, а каждые 3-5 лет?
Все верно. (По данным Росстата, в начале 2020 года численность женщин в возрасте от 20 до 65 лет в России превышала 48,5 миллионов. — PCR.NEWS.) Чтобы регулярно тестировать 70-80% от всех женщин 20-65 лет, нужен хорошо отлаженный процесс. Недостаточно дать возможность бесплатных обследований, надо еще убедить женщин в том, что им это нужно. Необходима просветительская работа среди населения, и это должно лечь на плечи государства.
Даже в Корее, где каждая женщина получает персональное приглашение, все равно обследуются только 50%?
Да, несмотря на все усилия. Есть мешающие факторы: и дискомфорт, и то, что молодые девушки не спешат обследоваться, потому что проблема рака ассоциируется с более пожилым возрастом.
А применительно к раку шейки это как раз не так? Это рак молодых?
Он зарождается в молодом возрасте, а преклиническая фаза длится 10-15 лет, но в головах непросвещенного населения это, к сожалению, не укладывается. Еще вопрос работы: как в России, так и в Корее нас не очень стремятся отпускать на медицинские обследования, из-за этого работающие женщины реже проходят скрининг. Многие работодатели выделяют время для тестирования на COVID, это важно здесь и сейчас. А рак, который может развиваться много лет, наших работодателей не настолько заботит. Поэтому важная задача организованного скрининга — донести до общественного сознания, что это вопрос здоровья каждой женщины.
 EASYPREP. Credit: YD
EASYPREP. Credit: YD
Как это делается
Скрининг на РШМ в Южной Корее
Национальная программа скрининга в Южной Корее действует с конца прошлого века. Мы узнали у сотрудников YD Diagnostics, как она работает и какое место в ней занимает автоматизированная жидкостная цитология.
История
1988. ПАП-тест впервые введен в качестве стандартного скринингового теста для промышленных рабочих и членов их семей.
1990. Для государственных служащих, учителей и членов их семей, которые готовы платить 50% стоимости за тест, ввели скрининг на рак желудка, печени, толстой кишки, груди и шейки матки. Однако в программу скрининга все еще не включены беднейшие слои населения, хотя более низкий социально-экономический статус связан с более высокой заболеваемостью и смертностью от рака.
1996. Правительство Кореи инициировало «10-летний план борьбы с раком». В Министерстве здравоохранения и социального обеспечения создано Отделение по борьбе с раком, построены исследовательский корпус и больница Национального онкологического центра и Национальный института борьбы с раком.
1999. Запущена программа скрининга РШМ, цитология шейки матки предложена всем женщинам, зачисленным в программу медицинской помощи (не имеющим страховки). В 2002 году для 20% граждан с самым низким уровнем дохода, застрахованным в системе национального страхования, стали доступны скрининговые исследования, если им было более 30 лет. В 2003 году охват этой группы расширили до 30%, в 2005-м — до 50%.
2006. В систему страхования введен ПАП-тест, выполняемый методом жидкостной цитологии.
2016. Начало национальной программы вакцинации против ВПЧ. Возраст начала скрининга сдвигается с 30 до 20 лет.
Современный порядок скрининга на РШМ
-
Возраст женщин-участниц — 20—74.
-
Интервал обследований — раз в два года. Скрининг прекращается для женщин старше 74 лет при наличии трех подряд отрицательных результатов цитологического исследования за последние 10 лет и при отсутствии в анамнезе дисплазии шейки матки средней или тяжелой степени за последние 20 лет.
-
Скрининговый тест – традиционная цитология (ТЦ) или жидкостная цитология (ЖЦ). Комбинированный тест (цитология + ВПЧ) рекомендуется как опциональный вариант с учетом индивидуальных рисков или предпочтений пациента.
-
Итоговый средний охват — более 50 %.
Финансирование и организация
Скрининг РШМ финансируется следующим образом: беднейшие слои населения, которые не имеют возможности оплачивать взносы в Национальную систему страхования, получают бесплатный ПАП-тест, который финансируется наполовину центральным правительством, наполовину — местным. Из числа граждан, застрахованных в Национальной системе страхования, беднейшие 50% тоже получают бесплатный ПАП-тест, остальные оплачивают 10% стоимости теста, а остальная сумма возмещается страховкой.
Все женщины целевой группы получают письмо-приглашение от Национальной системы страхования в начале года. Женщин, рожденных в четный год, приглашают на скрининг по четным годам, рожденных в нечетный — по нечетным. Комитет системы страхования отвечает за рассылку писем, а центры общественного здравоохранения отслеживают уровень участия.
Клиники, госпитали и специализированные скрининговые учреждения имеют возможность подать заявку на право участвовать в национальном скрининге на РШМ. Они получают сертификат, если оснащение их лабораторий соответствует определенным критериям. Большая часть исследований, таким образом, выполняется в частных центрах. Результаты вносят в базу данных Национальной системы страхования.
Помимо госпрограммы, в Корее, как в и России, доступен оппортунистический скрининг (по запросу пациента, направлению врача и т.д.). Очевидно, однако, что организованные программы скрининга рака эффективнее оппортунистических.
Методы
Тесты на основе традиционной цитологии показывают высокий уровень ложноотрицательных результатов — по корейским данным, до 20%. Это приводит к дополнительным расходам (кольпоскопические исследования без необходимости) и психологическому дискомфорту пациенток. Поэтому в скрининговую программу внедряется метод жидкостной цитологии. Как уже сказано, в Корее ЖЦ с 2006 года покрывается медицинским страхованием.
Сейчас ЖЦ-тесты составляют более 25% от всех тестов в рамках скрининга. Наиболее часто в Корее используются системы ThinPrep (Hologic), CellPrep (Biodyne), TriPath (BD) и EASYPREP (YD Diagnostics). Среди фильтрующих систем наиболее распространены ThinPrep, а среди центрифугирующих — TriPath, однако система EASYPREP набирает популярность.
Результаты
На протяжении действия программы национального скрининга в Корее снижаются показатели заболеваемости и смертности от РШМ. Заболеваемость на 100 000 женщин с 1999 по 2020 год снизилась с 18,6 до 7,6; смертность — с 2,8 до 1,7. Однако наблюдается та же тенденция, что и в России: заболеваемость преинвазивным раком шейки матки увеличивается у женщин в возрасте от 20 до 30 лет. Женщин младше 30 начали приглашать на скрининг лишь пять лет назад, с другой стороны, рост может быть обусловлен внешними факторами риска или изменениями сексуального поведения. Недавние исследования показали, что корейские девушки начинают половую жизнь все раньше: возраст начала снизился с 13,9 лет в 2008 году до 13,2 в 2015-м. Кроме того, женщины до 30–40 лет хуже всего посещают скрининговые исследования. Хотя участие в скрининге положительно коррелирует с уровнем образования и общим уровнем дохода, работающие женщины реже участвовали в обследованиях, чем неработающие. Это проблема, которую еще предстоит решить.
Партнерский материал


 Меню
Меню





 Все темы
Все темы




 0
0