Белок TRIM3 подавляет опухолеобразующую активность клеток меланомы путем убиквитинирования YAP1
Ученые из Медицинского университета Цзиньчжоу (Китай) исследовали влияние экспрессии убиквитинлигазы TRIM3 на фенотип клеток меланомы in vitro. Нокдаун TRIM3 увеличивал их пролиферацию, подвижность и инвазивность, а также снижает частоту апоптоза. Его оверэкспрессия оказывала противоположное влияние. Значительная часть эффектов TRIM3 опосредуется его влиянием на уровень белка YAP1, одного из ключевых коактиваторов транскрипции сигнального пути Hippo.
Меланома — злокачественная опухоль, развивающаяся из меланоцитов, — наиболее инвазивный тип рака кожи, склонный к метастазированию и с самым плохим прогнозом. Авторы исследования, опубликованного в Scientific Reports, проверили, как влияет уровень экспрессии белка TRIM3 на патогенез меланомы.
Белки семейства TRIM участвуют в различных процессах, играющих важную роль в прогрессии рака, включая модуляцию роста клеток, апоптоза и мобильности. TRIM3 известный прежде всего своей активностью E3 убиквитинлигазы, регулирует стабильность и функцию белка через убиквитин-протеасомную систему. Однако экспрессия и молекулярные функции TRIM3 при меланоме еще не были описаны.
Авторы исследования установили, что по данным GEPIA (сайт для интерактивного анализа экспрессии генов) в большинстве образцов меланомы снижен уровень экспрессии TRIM3. Снижение его экспрессии в клетках меланомы подтвердило иммуногистохимическое исследование клинических образцов. Не было показано достоверной корреляции экспрессии TRIM3 с возрастом или полом пациентов, однако наблюдалась сильная корреляция с патологической стадией заболевания. На стадиях I и II экспрессия TRIM3 была снижена в 10 из 37 образцов, а на стадиях III–IV — во всех пяти проанализированных образцах.
Влияние оверэкспрессии или нокдауна TRIM3 на фенотип клеток in vitro изучали на клеточных линиях меланомы M14 и A375. Клетки M14 были трансфицированы плазмидой с геном TRIM3, которая обеспечивала оверэкспрессию TRIM3, а клетки A-375 – плазмидами с генами малых интерферирующих РНК (si-TRIM3-1 или si-TRIM3-2), нацеленных на мРНК TRIM3 для подавления экспрессии.
Оверэкспрессия TRIM3 снижала оптическую плотность культуры клеток, в то время как нокдаун TRIM3 ее увеличивал. (Оптическая плотность является показателем пролиферации и выживания клеток.) Клоногенный анализ показал, что повышенная экспрессия TRIM3 уменьшала, а ее подавление увеличивало количество колониеобразующих клеток. Кроме того, оверэкспрессия TRIM3 уменьшала, а его нокдаун увеличивал количество клеток, способных к инвазии, а также дистанцию миграции клеток. Можно сказать, что уровень экспрессии TRIM3 отрицательно коррелировал с пролиферацией, инвазивностью и подвижностью клеток миеломы.
С помощью проточной цитометрии авторы показали, что сверхэкспрессия TRIM3 увеличивает, а нокдаун уменьшает частоту апоптоза. Анализ уровней белков апоптоза методом вестерн-блоттинга подтвердил, что TRIM3 способствует апоптозу клеток меланомы.
Известно, что белок YAP1 играет важную роль в инициации, инвазивности и резистентности опухоли к терапии и может активно экспрессироваться в клетках меланомы. Авторы показали, что сверхэкспрессия TRIM3, не влияя на количество мРНК YAP1, снижала уровень YAP1 и уровни мРНК его мишеней (генов CTGF и CYR61). Подавление экспрессии TRIM3 давало противоположный эффект.
Для анализа белок-белкового взаимодействия между TRIM3 и YAP1 клетки котрансфицировали плазмидами, экспрессирующими рекомбинантные белки HA-YAP1 и Flag-TRIM3. (Гемагглютинин НА и октапептид Flag — искусственные эпитопы, к которым имеются специфичные антитела. Прикрепление такой метки-тега к белку, к которому антитела нет, облегчает его исследование.) Коиммунопреципитация белковых комплексов с антителами к Flag и последующий вестерн-блот анализ с антителами к НА подтвердили, что белки взаимодействуют.
Авторы также показали, что TRIM3 участвует в деградации YAP1, прикрепляя к нему убиквитиновую метку и направляя в протеасому. Клетки с нокдауном TRIM3 обрабатывали циклогексимидом (ингибитор трансляции, останавливающий продукцию белков) и наблюдали уменьшение количества YAP1 со временем. Нокдаун TRIM3 замедлял деградацию YAP1.
Чтобы доказать, что TRIM3 регулирует количество YAP1 именно за счет убиквитинирования, клетки трансфицировали одновременно плазмидами Flag-TRIM3 и HA-UB (для экспрессии меченного НА убиквитина), культивировали 48 часов и обрабатывали мощным обратимым ингибитором протеасом MG132. Уровень убиквитинированного YAP1 также оценивали с помощью иммунопреципитации и вестерн-блот-анализа, и он возрастал в присутствии TRIM3.
В заключение, чтобы показать, что физиологические эффекты TRIM3 связанны именно с воздействием TRIM3 на YAP1, авторы провели эксперимент по восстановлению фенотипа (rescue assay). Они осуществили нокдаун YAP1 в клетках с нокдауном TRIM3, и это значительно ослабило «противораковые» эффекты инактивации TRIM3 — увеличение инвазивности, подвижности, ускорение роста, увеличение экспрессии CTGF и CYR61 и др.
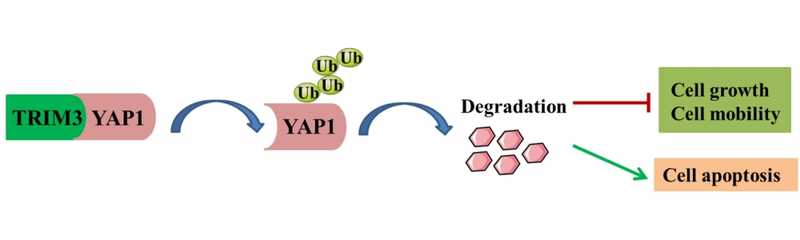 Высокая экспрессия TRIM3 приводит к убиквитинированию и деградации YAP1 и затем к ингибированию пролиферации клеток и стимуляции апоптоза. Credit: Sci Rep (2025). DOI:
10.1038/s41598-025-11317-y |
CC BY-NC-ND 4.0
Высокая экспрессия TRIM3 приводит к убиквитинированию и деградации YAP1 и затем к ингибированию пролиферации клеток и стимуляции апоптоза. Credit: Sci Rep (2025). DOI:
10.1038/s41598-025-11317-y |
CC BY-NC-ND 4.0
Итак, во многих образцах меланомы наблюдается пониженная экспрессия TRIM3, ее подавление усиливает рост и подвижность, а также подавляет апоптоз клеток меланомы in vitro. Данные эффекты, что для меланомы было показано впервые, в значительной мере обусловлены влиянием TRIM3 на содержание коактиватора транскрипции YAP1 путем его убиквитинирования и деградации.
Сигнальные пути Hippo и PI5PI4 совместно регулируют работу коактиватора транскрипции YAP
Источник
Wang, Yt., et al. TRIM3 suppressed the tumorigenicity of melanoma cells by ubiquitinating YAP1. Scientific Reports, 15, 27264 (2025). DOI: 10.1038/s41598-025-11317-y


 Меню
Меню





 Все темы
Все темы




 0
0










