Нобелевская премия-2020: CRISPR-Cas, система геномного редактирования
Нобелевская премия 2020 года по химии присуждена Эмманюэль Шарпантье и Дженнифер Дудне за разработку метода геномного редактирования (for the development of a method for genome editing).

«Эмманюэль Шарпантье и Дженнифер А. Дудна открыли один из самых точных инструментов генной технологии: генетические ножницы CRISPR-Cas9. Используя их, исследователи могут изменять ДНК животных, растений и микроорганизмов с чрезвычайно высокой точностью. Эта технология оказала революционное влияние на науки о жизни, вносит свой вклад в новые методы лечения рака и может воплотить мечту о лечении наследственных заболеваний», — говорится на сайте Нобелевского комитета.
В основу этой технологии положен механизм, обеспечивающий бактериям иммунитет против вирусов. CRISPR (Clustered Regularly Interspaced Palindromic Repeats, «скопление разделенных регулярными промежутками коротких симметричных повторов», произносится «криспер») — участок ДНК бактерий, который включает в себя короткие повторы и вставки между ними, гомологичных геномам бактериофагов.
«Система CRISPR-Cas9 состоит из двух частей,— говорил несколько лет назад одному из авторов этого текста Евгений Кунин сотрудник Национального центра биотехнологической информации Национальных институтов здравоохранения США, Бетесда). — Одна часть — это адаптивный модуль, который занимается тем, что выбирает из чужеродной ДНК вируса фрагменты и вставляет их во вполне определённое место в геноме бактерии или археи. Вторую часть можно назвать операционной. Она обрабатывает эти уникальные вставки, делает из них короткую РНК и с её помощью атакует исходную, чужеродную ДНК. Инактивирует вирус или плазмиду. <…> сама эта система — инструмент эволюции генома. Когда она функционирует, геном всё время меняется, в него вставляются все новые куски ДНК в ответ на вирусы и прочую чужеродную ДНК, приходящую из окружающей среды. Это, нравится кому или нет, в чистом виде ламарковские принципы. Пожалуй, наиболее яркий, хотя и не единственный пример такого рода эволюции.
Вся эволюция — это непрерывная гонка вооружений, борьба и одновременно эволюция паразитов с хозяином. И эта система — одна из наиболее сложных среди архей и бактерий, которая участвует в этом взаимодействии с паразитами».
Открытие системы CRISPR-Cas9 и создание инструментов для редактирования геномов — заслуга десятков ученых. Однако Нобелевскую премию получат лишь две замечательные женщины — Дженнифер Дудна (Калифорнийский университет, Беркли, США) и Эммануэль Шарпантье (Отделение Макса Планка изучения патогенов, Берлин, Германия).
В августе 2012 года авторский коллектив под руководством Шарпантье и Дудны сообщил о применении системы CRISPR-Cas9 для редактирования генома. Спустя всего месяц, в сентябре того же года, аналогичные результаты опубликовала группа, которую возглавлял Виргиниюс Шикшнис из Вильнюсского университета. Вильнюсцы могли быть первыми — ранее в 2012 году они посылали статью на ту же тему в Cell, но статью отклонили без рассмотрения. Заслуги Шикшниса были отмечены различными премиями, в том числе он в 2018 году получил престижную премию Кавли вместе с Шарпантье и Дудной, однако Нобелевская медаль ему не досталась.
Группа под руководством Фэна Чжана из Института Бродов опубликовалась позже — в феврале 2013 года. Зато в их работе технология была испытана на клетках млекопитающих — человека и мыши, что впоследствии оказалось принципиальным для патентования. Поскольку человек — млекопитающее, понятно было, что эти патенты станут ключевыми для практических применений.
В апреле 2014 года Институт Бродов получил первый из нескольких патентов на использование CRISPR в клетках млекопитающих. (Свою патентную заявку Чжан подал позже Дудны, в декабре 2012 года, но Институт Бродов запросил ускоренное рассмотрение в Бюро по патентам и товарным знакам США, заплатив небольшую сумму и ограничив сферу действия патента эукариотами.) Юристы Калифорнийского университета оспорили это решение, однако в феврале 2017 года Совет по патентным судам и апелляциям вынес решение в пользу Института Бродов. Акции Editas Medicine, один из соучредителей которой — Фэн Чжан, сразу поднялись в цене — было ясно, что именно этой компании достанется лицензия. (Кстати, Дудна тоже была соучредителем Editas — на тот момент никто не собирался воевать, — но покинула ее после начала патентного спора «по семейным обстоятельствам».)
На протяжении всех этих лет продолжается патентная тяжба между Дудной, Шарпантье и их учреждениями, с одной стороны (эту сторону в судебных документах сокращенно называют CVC — California, Vienna, Charpentier), Фэном Чжаном и Институтом Бродов — с другой, и перевес, очевидно, останется на стороне Института Бродов. Зато оппонентки Фэна Чжана получают заслуженную Нобелевскую премию. И права на технологию в Европе, по-видимому, также остаются у Шарпантье и Дудны.
С 2012 года появилось огромное множество модификаций технологии и множество вариантов ее применения в науке и медицине. Мы с увлечением следили за перспективами применения технологии CRISPR для редактирования человеческого генома, в том числе в клетках зародышевой линии. Поражались сенсационным заявлениям Хэ Цзянькуя и Дениса Ребрикова, обсуждали с Шухратом Миталиповым реальные перспективы CRISPR в «редактировании человека». Тем временем редактирование отдельных соматических клеток (например, клеток иммунной системы) находило практическое применение в медицине. . Уже идут клинические исследования CRISPR-терапии наследственных заболеваний — бета-талассемии, серповидноклеточной анемии, заболеваний зрения. И конечно, CRISPR стал любимым инструментом исследователей всего мира.
Важно помнить, что CRISPR — это не только редактирование. Пионеры CRISPR использовали свою технологию для создания точных и быстрых диагностических тест-систем. Совсем недавно и технология Фэна Чжана с соавторами — SHERLOCK, и технология Дженнифер Дудны с коллегами — DETECTR были применены для выявления SARS-CoV-2.
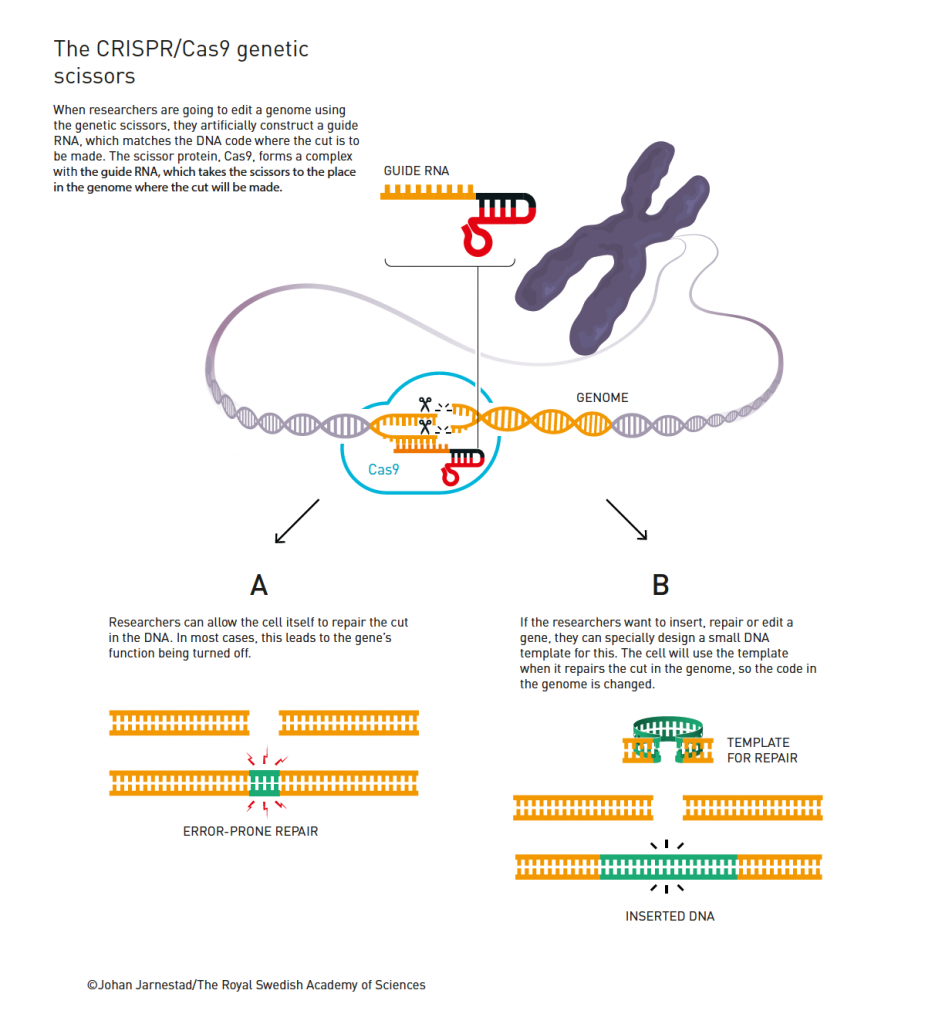 CRISPR: принцип метода. Credit: Johan Jarnestad/The Royal Swedish Academy of Sciences
CRISPR: принцип метода. Credit: Johan Jarnestad/The Royal Swedish Academy of Sciences
Источник
Genetic scissors: a tool for rewriting the code of life. Press release: The Nobel Prize in Chemistry 2020


 Меню
Меню





 Все темы
Все темы



 0
0












