Айнур Рагимова: «Мозг работает как оркестр»
В очередной лекции блока «Мозг» научно-популярного проекта «Метафаза» Айнур Рагимова рассказала о нейробиологических основах депрессии. При этом состоянии нарушаются различные системы регуляции нейропластичности, выработки нейротрансмиттеров и метаболизма головного мозга. Для лечения депрессии сейчас применяют не только антидепрессанты, но и неинвазивную транскраниальную магнитную стимуляцию. Однако она может быть устойчивой к лечению.

Айнур Рагимова, кандидат медицинских наук, врач-психиатр Российского центра неврологии и нейронаук, научный сотрудник Центра нейроэкономики и когнитивных исследований Института когнитивных наук ВШЭ, выступила с лекцией «Нейробиологические основы депрессии».
Депрессия — это не мода
Сегодня депрессия — третье по распространенности заболевание в мире. Для нее характерны снижение настроения, мотивации, обратимое снижение некоторых аспектов когнитивных способностей, моторная заторможенность. Депрессия может быть коморбидна со многими другими состояниями и заболеваниями. И если раньше в психиатрии внимание уделялось преимущественно большому депрессивному эпизоду, то сейчас специалисты говорят об аффективном спектре. Он включает в себя как единичные, так и рекуррентные депрессивные эпизоды, биполярное аффективное расстройство, перинатальную депрессию, а также депрессию, вызванную соматическим заболеванием — например, болезнями щитовидной железы. Именно поэтому при жалобах на слабость, апатию, нарушение концентрации психиатры могут сначала направить пациента на анализы крови, чтобы проверить общее функционирование организма.
Депрессия — это не только болезнь современности. Упоминания депрессии встречались еще с античности, когда ее причиной считался избыток черной желчи. В Средневековье депрессия («уныние») относилась к числу смертных грехов и считалась испытанием веры, а в эпоху Возрождения связанная с депрессией меланхолия начала ассоциироваться с гениальностью. Люди XVII–XVIII века, прежде всего аристократия, стали более склонными к открытому проявлению и обсуждению эмоций, но тогда депрессивные тенденции скорее воспринимались как эстетическое явление. В XIX веке они вновь стали ассоциироваться с гениями, с мрачными мыслящими людьми. В то же время неприкрытое проявление эмоций могло восприниматься как признак выходцев из неблагополучных кругов.
Именно в XIX веке начал развиваться психиатрический подход к лечению депрессии, в частности, психоанализ. Болезни настроения стали воспринимать как состояния, которое можно лечить, а не просто романтизировать их. Врачи начали систематизировать информацию, записывать медицинские наблюдения. С XX века соматические и аффективные расстройства стали изучать системно, исследователи начали доказывать, что такие расстройства имеют нейробиологическую основу. Возникают методы диагностики заболеваний, нейровизуализации, фармакологического лечения.
В XXI веке внимание к депрессии усилилось; все чаще среди аффективных жалоб упоминается феномен выгорания (burn out).
Распространенность депрессии и факторы риска
На психическое здоровье человека влияют разные факторы: как социальные (например, взаимоотношения с окружением), так и биологические, в том числе генетика. В классической клинической систематике депрессию принято делить на эндогенную и экзогенную. Экзогенная депрессия возникает в ответ на стрессовое событие, но со временем она может переходить в эндогенную даже при прохождении стресса. Мозг работает как оркестр, и нарушение его стройной, согласованной работы, вызванное различными причинами, приводит к появлению заболевания.
Для людей, склонных к депрессии, характерны определенные личностные черты: тревожность, перфекционизм, импульсивность, избегание социальных контактов и чувствительность к отвержению. Эти личностные черты могут указывать на определенные нейробиологические факторы, на которые влияют генетика и эпигенетика. Например, импульсивность может быть вызвана особенностями регуляции дофаминергической системы.
По данным ВОЗ, на 2023 год уровень заболеваемости депрессией в мире составляет 3,8% — это около 280 млн человек. Среди взрослых заболеваемость достигает 5%, причем депрессия встречается чаще у женщин. В России распространенность депрессии составляет 3–5%. Айнур Рагимова отметила, что статистические данные сильно варьируются в зависимости от того, учитывают ли опросники субъективные или объективные критерии, проводится ли исследование на дому или в больнице, онлайн или очно, учитываются ли медицинские записи. По этой причине статистические данные о распространенности депрессии в той или иной стране могут не вполне точно характеризовать реальную ситуацию, всегда нужно учитывать особенности сбора информации и диагностики в этой стране.
Как и отмечалось ранее, риск депрессии повышается при соматических заболеваниях. Например, депрессия есть у 20–45% пациентов с сопутствующими сердечно-сосудистыми болезнями, у 20–30% диабетиков, причем заболеваемость депрессией выше при неконтролируемом диабете. В последнем случае важен не только сам факт наличия болезни, но также измененный метаболизм глюкозы, который может влиять на работу астроцитов в мозге. С другой стороны, у людей с нарушениями настроения повышен риск развития инсулинорезистентности.
Не только сами заболевания, но и препараты, которые назначаются для их лечения, могут повышать риск развития депрессии. В число таких препаратов входят бета-блокаторы, некоторые препараты для похудения (например, римонабант и таранабант были запрещены к использованию из-за побочного влияния на психику), интерферон альфа, кортикостероиды, изотретиноин (ретиноид первого поколения), некоторые противоопухолевые препараты.
Риск депрессии повышается с возрастом. Депрессия встречается у 11,9% женщин и у 9,7% мужчин пожилого возраста. При диагностике депрессии врачи должны рассматривать ее не как изолированное событие, а в комплексе с соматическими заболеваниями. Например, депрессия — важный прогностический фактор при нейродегенеративных заболеваниях, поэтому психиатры могут советовать пожилым людям с депрессией обращаться также к неврологам и нейропсихологам.
Снизить риск развития депрессии можно за счет повышения уровня физической активности. Исследования показали, что аэробные нагрузки снижают риск депрессии на 11,5%.
Нейропсихологические признаки депрессии
Для депрессии характерно не только снижение настроения, но и ангедония (утрата способности получать удовольствие), снижение мотивации. При ангедонии у человека может утратиться способность радоваться чему-то хорошему в моменте, способность предвкушать хорошее. Это связано с нарушением дофаминергической регуляции: снижается реакция на положительные стимулы, в то время как реактивность на негативные стимулы, напротив, возрастает.

Определенную роль в развитии депрессии играют зеркальные нейроны. Эти нейроны активируются, когда человек наблюдает за движениями других людей. На ЭЭГ активацию зеркальных нейронов можно увидеть по повышению десинхронизации мю-ритма при наблюдении движений или эмоций. У пациентов с депрессией зеркальные нейроны более активны при распознавании именно негативных эмоций, а в выполнение социальных задач дополнительно вовлекаются лобные и зрительные доли. Считается, что зеркальные нейроны также способствуют эмпатии: когда они активируются, человек «примеряет на себя» действия или эмоции другого. Соответственно, при депрессии человек может «заражаться» негативными эмоциями, что усугубляет снижение настроения.
В целом для депрессии характерна глобальная психомоторная заторможенность. Это нарушение происходит на уровне моторного воображения. Оно позволяет человеку представить выполнение движения и может быть визуальным (от первого или третьего лица), кинестетическим или сенсорным. В моторное воображение вовлечены разные участки мозга, прежде всего моторная кора. У пациентов с депрессией снижается точность воображения движений, уменьшается скорость не только реального движения, но и воображаемого. Также скорости реального и воображаемого движения рассинхронизуются.
Как возникает депрессия
Существует несколько теорий развития депрессии. Наиболее популярная теория — моноаминовая. При передаче сигналов между нейронами электрическая активность служит сигналом для высвобождения химических веществ — нейромедиаторов. Высвобождаясь в синаптическую щель из одного нейрона, они связываются с рецепторами на поверхности другого. После передачи сигнала нейромедиаторы утилизируются, исчезая из синаптической щели. Однако в ней остается некоторое количество нейромедиаторов, которые захватываются назад в нейрон для повторного использования.
В 50-х годах было обнаружено, что противотуберкулезный препарат ипрониазид вызывает у пациентов чувство эйфории. Этот препарат — ингибитор моноаминоксидазы, фермента, который «перерабатывает» нейромедиаторы (в этом случае — серотонин, дофамин, норадреналин) при их обратном захвате в синапс. В результате при действии ипрониазида нейромедиаторы накапливаются в синаптической щели. Многие распространенные в настоящее время антидепрессанты относятся к селективным ингибиторам обратного захвата серотонина (СИОЗС).
Эти наблюдения и легли в основу моноаминовой теории, согласно которой недостаток определенных моноаминов, таких как серотонин или дофамин, приводит к появлению депрессии. Однако сейчас моноаминовая теория ставится под сомнение. Ассоциация между явлениями не позволяет сделать вывод о наличии причинно-следственной связи между ними: недостаток моноаминов может быть и следствием депрессии или одной из возможных ее черт. Так, не у всех пациентов низкий уровень серотонина, и не всем пациентам помогают СИОЗС. Кроме того, эффект от приема антидепрессантов не возникает сразу: требуется две-четыре недели. Ремиссии депрессии могут происходить даже без медикаментозной терапии, спонтанно или на фоне психотерапии.
Следующая теория состоит в том, что при депрессии нарушается гипоталамо-гипофизарно-надпочечниковая ось (ГГН) — нейроэндокринная система, координирующая реакции на стресс. В процессе работы этой оси из гипоталамуса выделяется кортикотропин-рилизинг гормон (КРГ), который стимулирует гипофиз, и он вырабатывает аденокортикотропные гормоны. В результате кора надпочечников производит глюкокортикоиды, в том числе кортизол, часто называемый «гормоном стресса». При длительном стрессе чувствительность к кортизолу снижается, поэтому он вырабатывается более активно. Ресурсы организма истощаются, и возникает депрессия, а также соматические расстройства. Действительно, у людей с длительной депрессией повышается уровень рецепторов к КРГ.
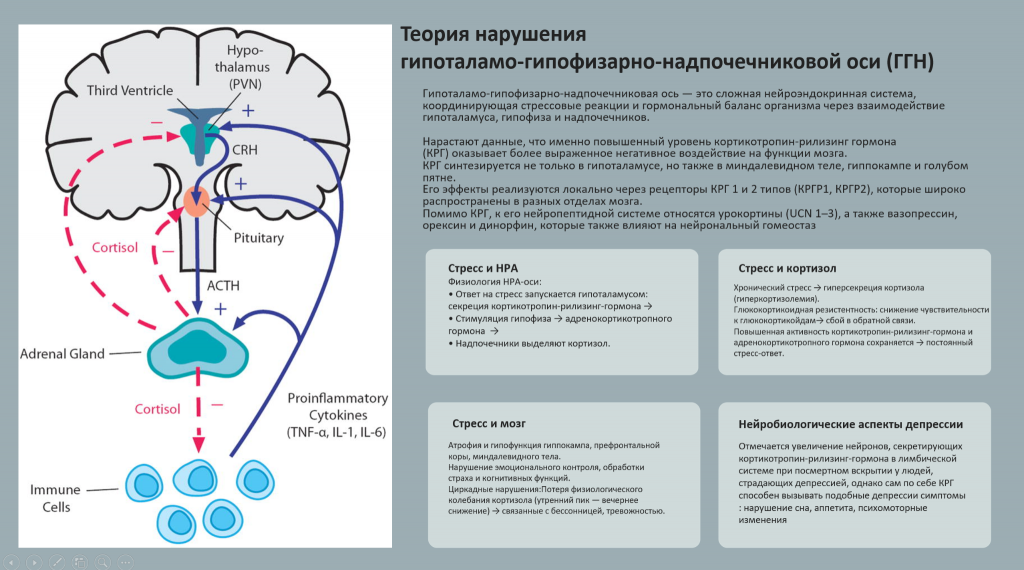
Однако по уровню кортизола трудно установить депрессию. Во-первых, он варьируется для каждого человека. Во-вторых, он может меняться в течение дня, в зависимости от менструального цикла, времени сна и бодрствования, приема лекарств и сопутствующих заболеваний. Даже сама процедура забора крови для анализов может вызывать стресс и, соответственно, повысить уровень кортизола. Разовая сдача анализов на кортизол не отражает суточный ритм его секреции.
Согласно еще одной теории, на развитие депрессии может влиять микробиота кишечника. Считается, что бактерии ЖКТ могут вырабатывать метаболиты, способствующие возникновению воспаления, которое распространяется от кишечника через энтеральную нервную систему и блуждающий нерв в мозг. Эксперименты на мышах показали, что если кишечную микробиоту от мыши с депрессией пересадить другой мыши, то у нее тоже разовьется депрессия. А в кишечной микробиоте пациентов с депрессией чаще встречаются условно-патогенные и провоспалительные штаммы бактерий, но снижается количество противовоспалительных таксонов.
О причинах возникновения депрессии также можно сделать выводы, обратив внимание на те нейрональные системы, работа которых нарушена у пациентов с этим заболеванием. Однако любые данные, полученные с помощью нейровизуализации, гетерогенны, ведь все люди разные, а у некоторых из них могут быть коморбидные заболевания, о которых они даже не знают.
При депрессии аномально активны латеральная лобная и височная кора, мозжечок: при отрицательных эмоциях эти области мозга не активируются, а после лечения антидепрессантами их уровень активности восстанавливается. Противоположные изменения наблюдались в вентромедиальных лобных областях и полосатом теле. Могут уменьшаться в объемах вентромедиальная префронтальная кора, левая передняя часть поясной извилины и орбитофронтальная кора. Кроме того, у пациентов с депрессией снижается плотность глиальных клеток в дорсальной, орбитальной и префронтальной коре, в миндалевидном теле.
Астроциты и депрессия
Еще одна теория возникновения депрессии связана с астроцитами. Астроциты — это клетки глии, которые механически поддерживают и питают нейроны. Также астроциты способствуют формированию синапсов между нейронами и могут регулировать их активность, в частности, экспрессируя рецепторы серотонина и норадреналина. Например, антидепрессанты флуоксетин и сертралин нацелены на серотониновый рецептор 5-HT2B, который экспрессируется на астроцитах.
Кроме того, астроциты способны захватывать из синаптической щели возбуждающий нейромедиатор — глутамат. В больших концентрациях он вреден и вызывает эксайтотоксичность. Поглощая глутамат, астроциты перерабатывают его в глутамин и передают нейронам для повторного использования. При депрессии же этот глутамат-глутаминовый цикл нарушен, в результате глутамат накапливается в синаптической щели и нарушается нейропластичность.
Кроме того, астроциты могут влиять на синаптическую пластичность мозга за счет выработки BDNF (нейтротрофический фактор мозга, стимулирующий развитие нейронов) или D-серина. D-серин — это глиотрансмиттер, который является коагонистом NMDA рецепторов глутамата. Соответственно, его дефицит ассоциирован с депрессивными симптомами, а в крови и в ликворе пациентов с депрессией уровень D-серина снижен. При дефиците BDNF также наблюдается снижение пластичности головного мозга.
Еще одна важная функция астроцитов — энергетическая. Они накапливают глюкозу, которую перерабатывают в ходе гликолиза до лактата для выработки энергии. Лактат впоследствии передается в нейроны и подпитывает их энергетический метаболизм. При инсулинорезистентности или расстройствах пищевого поведения (например, при компульсивном переедании) нарушается и этот процесс, и проницаемость гематоэнцефалического барьера (ГЭБ), и накопление глюкозы астроцитами. Измененный метаболизм может влиять на активность нейронов и синтез нейромедиаторов.
Так называемые реактивные астроциты участвуют в формировании воспалительного ответа. Они выделяют провоспалительные цитокины, активно «сотрудничают» с микроглией и способствуют апоптозу нейронов. В физиологических условиях реактивные астроциты принимают участие в синаптическом прунинге — процессе, при котором избыточные аксоны нейронов «обрезаются», чтобы повысить общую эффективность нейронных сетей. Что важно, депрессия сопровождается хроническим нейровоспалением, а активность реактивных астроцитов может вызывать лекарственно-резистентную депрессию.
Генетика депрессии
Депрессия считается полигенным заболеванием, то есть в повышение риска ее развития вносит вклад множество генов, эффект каждого из которых сам по себе мал. На данный момент изучено более 170 локусов риска и предложено более 200 генов-кандидатов. К наиболее обсуждаемым генам относятся SLC6A4 (транспортер серотонина, участвует в его обратном захвате), TPH2 (фермент биосинтеза серотонина), COMT (фермент, участвующий в катаболизме дофамина и норадреналина), BDNF, FKBP5 (белки, участвующие в ответе на стресс и обеспечивающие нейропластичность). Как упоминалось ранее, на развитие депрессии влияют и средовые факторы: например, известно, что у носителей короткого аллеля SLC6A4 риск развития депрессии выше при хроническом стрессе, но не в благоприятной обстановке.
Считается, что наследуемость большого депрессивного расстройства составляет около 25%. Результаты исследований GWAS, в свою очередь, показывают, что многие ассоциированные с депрессией гены ассоциированы также с другими психологическими чертами и расстройствами, например, с невротизмом.
Когда депрессия не поддается лечению
До 20% пациентов с депрессией (если диагноз был установлен правильно) могут не реагировать на первые два курса лечения. Такое состояние называется резистентной депрессией. У пациентов с резистентной депрессией чаще встречаются коморбидные заболевания, в том числе тревожные расстройства, или депрессивное расстройство скрывает за собой биполярное расстройство. Пациенты с резистентной депрессией как минимум в два раза чаще подвергаются госпитализации и потребляют в 1,4–3 раза больше психотропных препаратов. В США медицинские расходы таких пациентов в шесть раз выше, чем у тех, у кого есть эффект от лечения, а общие затраты, связанные с депрессией, выше в 19 раз.
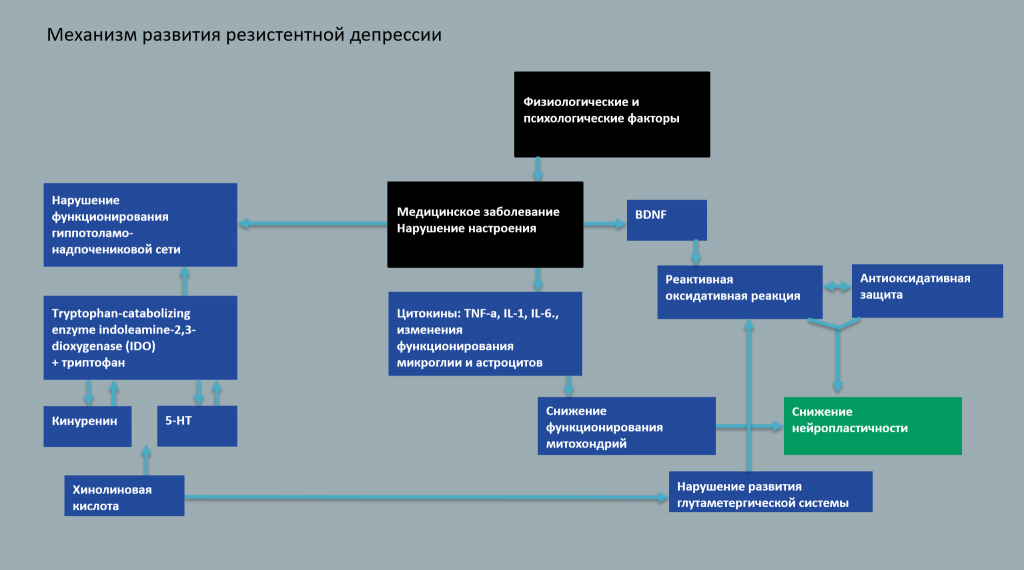
Развитию резистентной депрессии способствуют все ранее упомянутые механизмы. Даже если до этого болезнь сопровождалась нарушениями только со стороны одной системы, при резистентной депрессии эти нарушения усугубляются, накладываясь друг на друга.
Лечение депрессии — не только антидепрессанты и психотерапия?
Первая линия лечения депрессии — назначение СИОЗС. Самый нейтральный препарат этой группы — эсциталопрам, который обладает высокой селективностью и меньшим количеством побочных эффектов, чем другие. Другие СИОЗС имеют разнообразную специфику действия.

Также можно применять транскраниальную магнитную стимуляцию (ТМС). Этот неинвазивный метод был одобрен FDA для лечения большого депрессивного эпизода в 2008 году. Чаще всего применяется ТМС левой дорсолатеральной префронтальной коры.
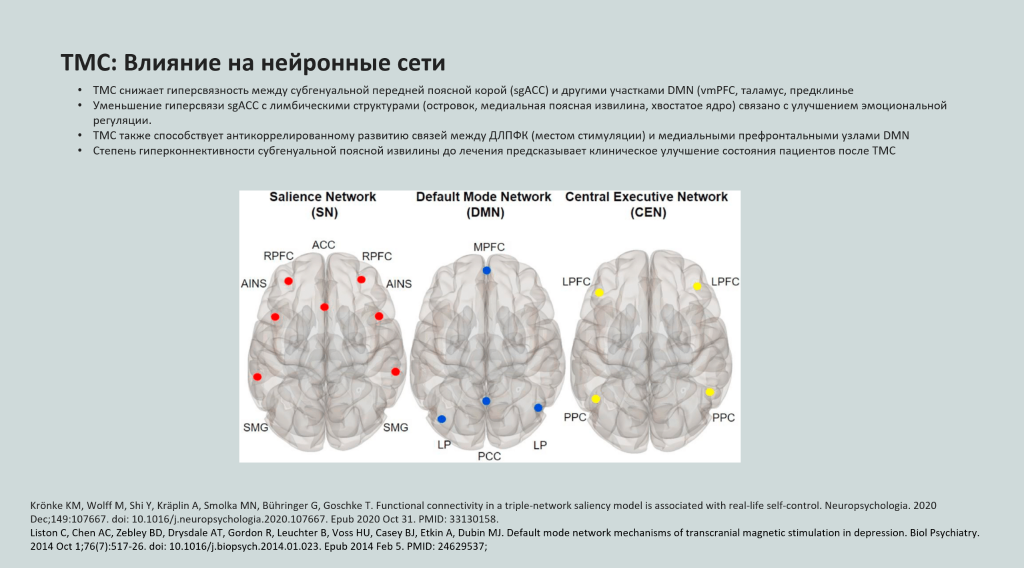
Считается, что ТМС повышает доступность серотонинергических и дофаминергических рецепторов, увеличивает выработку BDNF и позволяет перестроить активность нейрональных сетей, повысив активность гипофункциональных отделов мозга или снизив гиперконнективность между теми или иными структурами. Интересно, что реактивность на ТМС тоже различается у разных пациентов. Например, у пациентов с распространенным однонуклеотидным полиморфизмом Val66Met в гене BDNF реакция на ТМС снижена или вовсе отсутствует.
Другие лекции блока «Мозг»
Максим Карагяур об инструментах для изучения мозга человека
Юлия Шпилюкова: «Будет ли наше старение физиологическим или патологическим — в наших руках»


 Меню
Меню





 Все темы
Все темы




 0
0











