Юлия Шпилюкова: «Будет ли наше старение физиологическим или патологическим — в наших руках»
В продолжение блока лекций «Мозг» научно-просветительского лектория «Метафаза» Юлия Шпилюкова рассказала о болезни Альцгеймера, методах ее диагностики и лечения с позиции врача. Сейчас для диагностики этой болезни активно внедряются различные биомаркеры, а в мире начинает применяться антиамилоидная терапия, хотя предстоит еще долгий поиск комбинированных подходов к лечению.

Юлия Шпилюкова (к.м.н., руководитель Центра когнитивного здоровья, научный сотрудник, врач-невролог ФГБНУ «Российский центр неврологии и нейронаук») продолжила блок лектория «Метафаза», посвященный мозгу, с лекцией «Болезнь Альцгеймера: новая парадигма диагностики и терапии».
Деменция и когнитивная хрупкость
В настоящее время существует глобальный тренд к старению населения. По прогнозам ВОЗ, к 2030 году каждый шестой человек в мире будет в возрасте старше 60 лет, а к 2050 году доля пожилого населения удвоится. В результате этого все чаще встречаются возраст-ассоциированные заболевания, такие как деменция. Самой частой причиной деменции среди людей всех возрастов является болезнь Альцгеймера (БА). Риск ее развития увеличивается с возрастом. Кроме того, по официальной статистике, БА — седьмая по значимости причина смерти в мире и основная причина расходов на здравоохранение. Проблема деменции существует и в России: по данным на 2025 год, около четверти населения составляют люди старше трудоспособного возраста. При этом от БА страдают около двух миллионов человек, хотя людей, официально получивших такой диагноз, меньше.
Важно понимать, что любая деменция — это не нормальный вариант старения. При развитии патологического варианта старения основными стадиями когнитивных нарушений являются умеренное когнитивное расстройство (УКР), когда когнитивные нарушения не мешают повседневной активности человека, и стадия деменции, когда такие нарушения более выражены и значимо нарушают повседневную активность человека. Между нормальным старением и патологическим лежит состояние так называемой «хрупкости», когда организм человека становится более уязвимым к различным стрессам и патологическим изменениям. Если состояние хрупкости не скорректировать, оно может привести к развитию полноценной деменции.

Почему возникает болезнь Альцгеймера?
БА — это хроническое прогрессирующее нейродегенеративное заболевание. Как и другие болезни этой группы, БА характеризуется довольно длинным продромальным периодом, который может длиться до 20 лет. В этот период в мозге накапливаются нерастворимые агрегаты белков, которые нарушают функции клеток мозга и провоцируют атрофию его участков. Интересно, что большая часть случаев БА — спорадические, т.е. они не вызваны наследственными мутациями, а точная причина возникновения болезни может остаться неизвестной.
Развитие БА — комплексный процесс. Патогенез БА связан с формированием агрегатов бета-амилоида и нейрофибриллярных клубков из гиперфосфорилированного белка тау. Значительный вклад в развитие болезни также вносит нейровоспаление. Считается, что накопление агрегатов бета-амилоида происходит во время продромального периода и предшествует другим элементам патогенеза, причем наличие этих агрегатов не во всех случаях приводит к развитию БА. Нейровоспаление же «включается» уже в ответ на возникновение в мозге патологических агрегатов бета-амилоида и тау, причем эти белки прекращают выполнять свои физиологические функции.
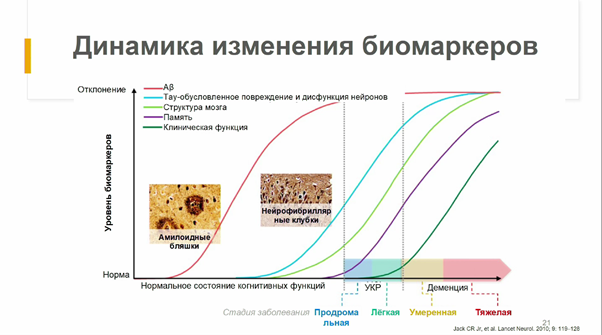
Проследить за развитием БА можно и в пространстве. Известно, что обычно БА сначала поражает гиппокамп, затем распространяется на лимбическую систему и затрагивает всю кору головного мозга. На основе информации о том, в каких участках мозга локализуются агрегаты патологических белков, посмертно определяются стадии заболевания, причем обычно на начальных стадиях — когда агрегаты охватывают только гиппокамп — болезнь не имеет симптомов.
Диагностика болезни Альцгеймера
Для постановки диагноза врачам необходимо обращаться как к клиническим, так и к биологическим критериям. Они должны принимать в учет не только клиническую картину, но и результаты анализа биомаркеров. В мире анализ биомаркеров для диагностики БА используется уже более 15 лет, однако такие тесты все еще не вошли в регулярную клиническую практику в России.
Многие привыкли считать, что один из главных симптомов БА — это потеря эпизодической памяти. На самом же деле это лишь один из нескольких клинических фенотипов болезни, который встречается довольно часто. Помимо нарушений памяти у пациентов также возникают проблемы с речью и зрением, реже — с поведением и движениями.
Для выявления нарушений врачи используют различные нейропсихологические тесты. Например, пациентов могут попросить запомнить информацию и воспроизвести ее через некоторое время, срисовать многоугольник или куб, а также нарисовать циферблат часов и указать на нем определенное время. Часто по мере прогрессирования болезни пациенты начинают все хуже справляться с такими заданиями. Чтобы обнаружить характерные нарушения речи (афазию), пациентов могут попросить выполнить специализированные тесты, например, описать картинку. Характерными для БА нарушениями речи являются запинки при разговоре и затруднения с подбором слов. Двигательные нарушения могут включать так называемую апраксию — сложности с выполнением целенаправленных движений, которые проявляются при осмотре трудностями с копированием жестов или трудностями воспроизведения определенных сложных движений с воображаемым предметом: например, если пациента с БА попросить показать, как он будет расчесываться, он начнет гладить себя по голове ладонью, не показав, что использует для этого инструмент — расческу.

После определения клинической картины врачи приступают к более углубленному обследованию пациента. Сначала они исключают другие возможные диагнозы, приводящие к наблюдаемой клинической картине. Пациентов направляют на сдачу анализов и обследования, позволяющие выявить структурные изменения в головном мозге, — магнитно-резонансную томографию (МРТ) или компьютерную томографию (КТ) головного мозга. Характерные структурные признаки позволяют врачам сделать первичный вывод о наличии како-либо нейродегенеративного заболевания, в том числе БА. При этом врачи предпочитают делать именно структурную МРТ, а не КТ, так как такой метод более информативен, хотя и не позволяет специфически поставить диагноз БА. Есть много других нейродегенеративных заболеваний, похожих на БА клинически и по данным МРТ, например, энцефалопатия позднего возраста с белком TDP-43 и преимущественным поражением лимбических структур (от англ. LATE – Limbic-Predominant Age-Related TDP-43 Encephalopathy), которая была описана сравнительно недавно, в 2019 году. В отличие от БА, LATE вызывается агрегатами белка TDP-43 и чаще всего возникает у очень пожилых пациентов: возраст дебюта обычно составляет 80 лет и старше. Еще одна проблема структурных методов — МРТ или КТ — заключается в том, что на самых ранних стадиях нейродегенеративных заболеваний эти методы могут вовсе не выявить структурных изменений.
Поэтому на следующем этапе диагностики врачи обращаются к биомаркерам, которые могут подтвердить (или исключить) диагноз БА. Существует несколько способов их определения. Первый из них заключается в измерении уровней ключевых маркеров БА бета-амилоида 1–42 и фосфорилированного тау 181 в ликворе (спинномозговой жидкости), которую получают с помощью люмбальной пункции. Так, у пациентов с БА уровень бета-амилоида 1–42 снижен относительно установленных пороговых значений, так как большая часть этого белка концентрируется в бляшках в мозге. А уровень фосфорилированного тау 181 у пациентов с БА повышен в ликворе относительно пороговых значений. Уровень содержания белков в ликворе можно определять с помощью различных методов, например, иммуноферментного анализа (ИФА, ELISA), иммунохемилюминесцентного анализа (ИХЛА), масс-спектрометрии или технологии SiMoA (массив одиночных молекул). Из них самым перспективным является SiMoA — этот метод позволяет определять даже низкие концентрации белков, благодаря чему может стать возможной диагностика БА по крови.
Второй возможный метод оценки биомаркеров БА — использование позитронной эмиссионной томографии (ПЭТ) со специфическими лигандами к агрегатам ассоциированных с БА белков, что позволяет визуализировать степень их распространения. Для этой процедуры пациенту внутривенно вводят лиганд, способный связываться с амилоидными бляшками или тау-белком, благодаря чему можно оценить не только наличие, но и количество, распространенность таких агрегатов в мозге. Оба этих метода довольно специфичны и чувствительны, однако ПЭТ — более дорогой метод; кроме того, в России он пока что не применяется.
На основе данных анализа биомаркеров врачи могут сделать вывод о том, насколько вероятен диагноз БА. Так, например, если по результатам тестов выявляются только признаки амилоидопатии без таупатия, рекомендуется через время повторно провести анализы на тау-белок (или использовать альтернативный способ диагностики). В случае нетипичного клинического фенотипа диагноз БА не может быть поставлен с высокой долей уверенности даже при выявлении измененных биомаркеров, ввиду отсутствия в клинической практике биомаркеров всех других нейродегенеративных заболеваний.
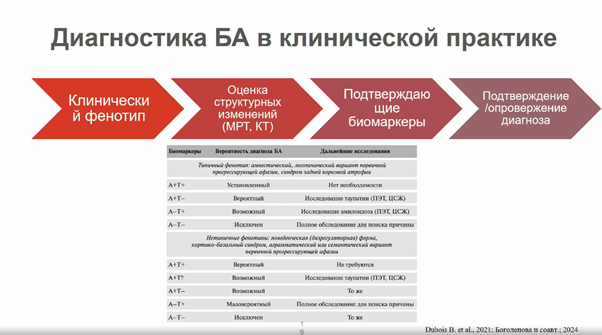
Подтвердить диагноз биомаркерами важно еще и для того, чтобы назначить пациенту подходящее лечение. При этом важно поставить диагноз как можно раньше, желательно — до проявления клинических симптомов, когда патологический процесс уже запущен. В связи с этим исследователи обсуждают многие другие биомаркеры, которые могут быть определены даже на бессимптомной стадии и указывать на ту или иную форму БА, тяжесть протекания болезни и т.д.
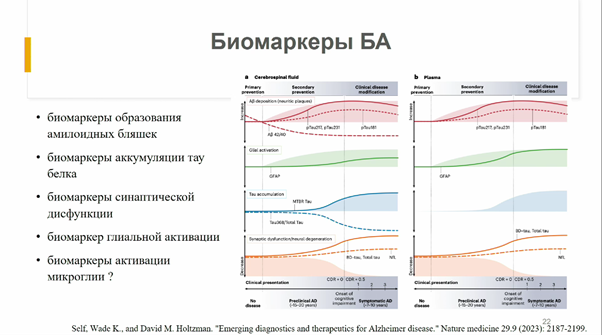
Умеренные когнитивные нарушения — предвестник деменции?
Обычно деменции предшествует стадия умеренного когнитивного расстройства (УКР): у пациента или его близких возникают жалобы на забывчивость, хотя при этом он справляется с бытом и профессиональными навыками. На стадии деменции пациент нуждается в более высоком уровне поддержки. УКР необязательно «прогрессирует» в деменцию: нарушения могут сохраниться на том же уровне или, наоборот, при коррекции всех факторов риска «вернуться» назад в траекторию нормального старения.
К факторам риска развития УКР относятся возраст, пол (по некоторым данным, у женщин встречаются чаще из-за гормональных изменений), отягощенный семейный анамнез (риск выше, если в семье были случаи деменции), а также носительство аллеля e4 гена APOE. Эти факторы считаются немодифицируемыми. Модифицируемыми факторами риска, в свою очередь, являются хронические заболевания, прием лекарственных препаратов (особенно в случае, если пациент принимает несколько препаратов одновременно), тревожно-депрессивное расстройство, метаболические (дефицит B12, фолата) и инфекционные причины (сифилис), нарушения сна, нормотензивная гидроцефалия.
По биомаркерам БА возможно с большей степенью вероятности предсказать конверсию УКР в деменцию. По данным исследований, почти у 60% пациентов, у которых выявлены положительные изменения биомаркеров БА, в течение трех лет развивается деменция, в то время как у пациентов с не измененными биомаркерами этот показатель составляет всего 4%. По данным другого исследования, даже у пациентов, у которых получены отрицательные результаты оценки биомаркеров, риск развития деменции повышается на 10–15% в год; в ряде случаев пациент может оставаться стабильным (УКР сохраняется на протяжении длительного времени), либо наблюдаются улучшения когнитивных функций. К факторам риска конверсии УКР в деменцию относятся нарушения памяти, пожилой возраст, сахарный диабет, низкий уровень образования, перенесенный инсульт и носительство аллеля e4 гена APOE. Возврат к норме или непрогрессирование УКР более вероятны, если не преобладают нарушения памяти (а отмечаются когнитивные нарушения других модальностей), пациенты имеют более высокий когнитивный резерв и уровень образования.
Какие же точки вмешательства при УКР? Врачи должны обращать внимание на потенциально обратимые причины и предлагать способы лечения текущих заболеваний, корректировать сосудистые факторы риска и т.д. Также пациентам с УКР необходима коррекция образа жизни: когнитивный тренинг, физическая активность, социализация. На данный момент нет одобренных лекарств, которые могли бы применяться для профилактики конверсии УКР в деменцию. Тем не менее, в некоторых странах пациентам с УКР и подтвержденной БА по биомаркерам может быть назначена антиамилоидная терапия, которая, замедляя течение заболевания, может отсрочить наступление стадии деменции.
Болезнь Альцгеймера неизлечима?
При установленном диагнозе БА применяют две группы препаратов — ингибиторы ацетилхолинэстеразы (донепезил, галантамин, ривастигмин) и антагонисты NMDA-рецепторов глутамата (мемантин). Первая группа препаратов применяется на стадиях начальной и умеренной деменции, вторая — на стадии умеренной и выраженной деменции. Для лечения тревоги и депрессии применяются антидепрессанты — селективные ингибиторы обратного захвата серотонина (СИОЗС), а для коррекции нарушений поведения и психотических расстройств — антипсихотики. Вся вышеперечисленная терапия корректирует симптомы, но, к сожалению, не может остановить прогрессирование заболевания.
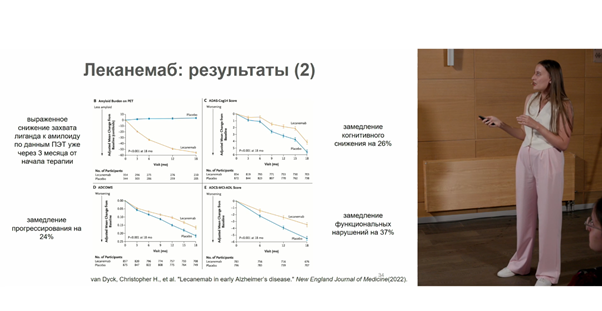
Несколько лет назад в мире начали появляться инновационные препараты патогенетического лечения БА, так называемая антиамилоидная терапия. Данные препараты представляют собой антитела, которые либо препятствуют образованию бляшек, либо способствуют их растворению. Одним из первых одобренных препаратов стал леканемаб, который был одобрен в США в конце 2023 года. В клинических испытаниях леканемаба 3 фазы приняли участие 1795 пациентов с ранней стадией БА (УКР или легкая деменция), у которых была подтвержденная амилоидная патология. Пациентов делили на группу плацебо и группу леканемаба; они получали терапию внутривенно каждые 2 недели в течение 18 месяцев. Прогресс пациентов оценивали по различным шкалам (CDR-SB, ADAS-Cog14 и т.д.). В результате лечения леканемабом у пациентов на 27% замедлялось прогрессирование деменции при оценке по шкале CDR-SB: у них улучшились память, координация в пространстве, коммуникация, хобби, самообслуживание в быту и т.д. Наблюдались улучшения и по другим шкалам, а по данным ПЭТ уже через 3 месяца от начала терапии снижался захват лиганда к бета-амилоиду.
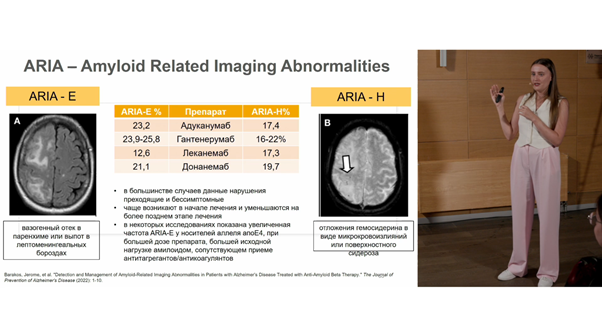
Применение антител для амилоидной терапии связано с некоторыми нежелательными нарушениями, которые могут протекать как бессимптомно, так и с симптомами. Эти нарушения выявляются по данным нейровизуализации (МРТ), объединены аббревиатурой ARIA (Amyloid Related Imaging Abnormalities — связанные с амилоидом нарушения при визуализации) и могут проявляться в виде отека или кровоизлияний в головном мозге. ARIA чаще всего возникают в начале лечения, но могут проявляться и на более поздних этапах. Риск возникновения ARIA может быть повышен у носителей аллеля e4 гена APOE, у пациентов, получавших большую дозу препарата или имевших большую исходную нагрузку амилоида, а также при одновременном приеме с антикоагулянтами.
Продолжаются поиски других лекарственных препаратов для лечения БА. На 1 января 2025 года были зарегистрированы 182 клинических исследования для 132 препаратов, из них 31 препарат находился на 3 фазе испытаний. Три четверти препаратов направлены на различные этапы патогенетического процесса БА; мишенями трети препаратов являются рецепторы нейротрансмиттеров, четверти — амилоид. Многие препараты также направлены на метаболизм, нейрогенез, воспаление и т.д.
При ведении пациентов с БА также назначают немедикаментозное лечение. Оно состоит в коррекции образа жизни: пациентам рекомендуют регулярно заниматься физической активностью, когнитивным тренингом, улучшать качество сна, поддерживать социальные контакты и здоровое сбалансированное питание, отказаться от вредных привычек. Вместе с тем необходимо контролировать сопутствующие заболевания и прием препаратов, корректировать проблемы со зрением или слухом, а также обеспечивать соблюдение гигиенических процедур и безопасности как дома, так и на улице. В том числе поэтому пациентам рекомендуют жить не в одиночестве. Поддержку пациентов и их близких в России занимается фонд Альцрус.
Каковы же меры профилактики БА на досимптомной стадии? Существуют исследования, показывающие, что коррекция ряда факторов риска может снизить риски деменции практически наполовину. К числу этих факторов риска относятся низкий уровень образования, потеря слуха, высокий уровень ЛПНП в крови, депрессия, травмы головного мозга, отсутствие физической активности, диабет, курение, артериальная гипертензия, ожирение, злоупотребление алкоголем, социальная изоляция, загрязнение воздуха и утрата зрения. Следовательно, во многом люди в силах сами снизить риски деменции и обеспечить себе физиологическое старение.
Эксперты сходятся на том, что текущая антиамилоидная терапия — это лишь начало пути иммунотерапии при БА. В будущем, вероятнее всего, будет применяться комбинированный подход, при котором таргетными мишениями будут и амилоид, и тау, и нейровоспаление. Такая терапия будет подбираться индивидуально в зависимости от клинической картины и результатов биомаркерной оценки конкретного пациента. Чтобы реализовать такой подход, необходимо и дальше развивать диагностику и внедрять в практику различные биомаркеры, в том числе для определения других протеинопатий, вызванных, к примеру, альфа-синуклеином или TDP-43. Кроме того, необходимо подготовить инфраструктуру: создавать клинические центры и готовить новых специалистов. На базе Российского центра неврологии и нейронаук в Центре когнитивного здоровья занимаются диагностикой и ведением пациентов с БА и другими когнитивными нарушениями, а также внедряют инновационные методы диагностики и лечения БА, в рамках чего в настоящее время осуществляется в том числе проект «Стоп, Альцгеймер!», реализуемый фондом ФРОНТМЕД вместе с Российским центром неврологии и нейронаук.
Другие лекции блока «Мозг»
Максим Карагяур об инструментах для изучения мозга человека
Айнур Рагимова: «Мозг работает как оркестр»


 Меню
Меню





 Все темы
Все темы




 0
0











