МД-2025. Массовое параллельное секвенирование: успехи и ожидания
Связь между биобанкированием репродуктивных клеток военнослужащих и лечением бесплодия, инструменты китайских ученых для анализа РНК отдельных ядер клеток в подходах пространственной транскриптомики или поиска сайтов сплайсинга в данных РНК-секвенирования с длинными ридами, новые приборы и реагенты и многое другое — на секции «Новейшие разработки в области массового параллельного секвенирования (NGS)» конференции «Молекулярная диагностика 2025».

С докладом «Стратегическое планирование геномных исследований и биобанкирование: настоящее и перспективы» выступил Руслан Глушаков (Научно-исследовательский отдел Военно-медицинской академии имени С.М. Кирова). Он напомнил об основных достижениях медико-биологических наук за последние сто лет, таких как расшифровка генома человека и инструменты для его редактирования, развитие регенеративной медицины и вспомогательных репродуктивных технологий, создание гибридом и получение моноклональных антител, формирование современных представлений о микробиоме. Впереди у нас, на пороге шестого технологического уклада, — конвергенция нано-, био-, информационных и когнитивных технологий (NBIC), получение объективной картины мира с помощью больших данных и ИТ («мир без гипотез»), промышленное получение термоядерной энергии.
Важной частью мира будущего будет работа с омиксными данными, а в их накоплении важную роль играет биобанкирование.
Существуют запросы на работу с биобанками, как от государства и общества, так и от специалистов в различных областях. Легко видеть, что эти запросы пересекаются, и возможно формирование консорциумов для решения сразу нескольких задач. Например, вопросы генетической идентификации граждан можно совместить с расширением базы доноров и длительным хранением репродуктивного материала.
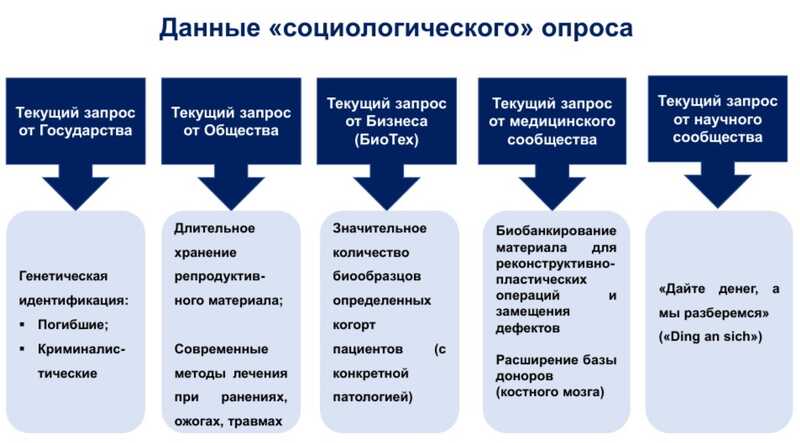
В статье 55 № 323-ФЗ «Об основах охраны здоровья граждан в РФ» указано, что «граждане имеют право на криоконсервацию и хранение своих половых клеток, тканей репродуктивных органов и эмбрионов за счет личных средств и иных средств, предусмотренных законодательством РФ». Но при этом ни Минздрав, ни Минобороны не имеют материальной базы для организации криобанков репродуктивного материала призывников, курсантов военных вузов или мобилизованных, подчеркнул докладчик. Для этого целесообразно создавать биобанки в каждом субъекте РФ.
Руслан Глушаков рассказал о том, как этот вопрос решается «у геополитического противника или партнера». Криохранилища или клиники репродуктивной медицины получают аккредитацию у минобороны США, после чего часть расходов по забору и криоконсервации спермы военнослужащих берет на себя Пентагон. Через некоторое время военнослужащий может начать оплачивать дальнейшее хранение, либо биоматериал станет собственностью организации. А в Израиле существует практика оплаты посмортального зачатия в случае гибели единственного сына-военнослужащего: государство оплачивает все этапы ВРТ, включая суррогатное материнство.
Биобанкированный материал военнослужащих представляет значительный научный интерес, например, с точки зрения исследования бесплодия среди молодых условно здоровых мужчин.
Докладчик также поделился собственным опытом боевой хирургической патологии. Биобанкирование тканей может способствовать клиническому применению децеллюляризированных кожных лоскутов, кадаверных или аутологичных (последнее может быть применено, например, при борьбе с анаэробной инфекцией подкожной жировой клетчатки). То же относится и к децеллюлиризированной костной ткани.
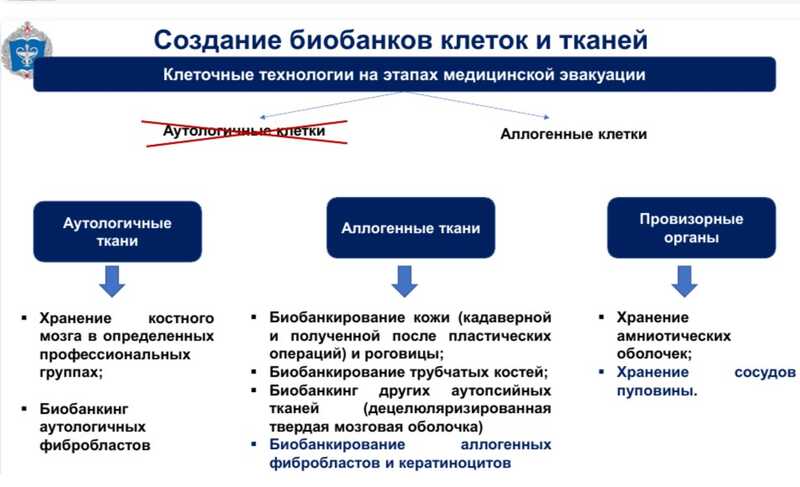
Существует представление о том, что банки персонифицированных клеточных культур военнослужащих могут помочь как в лечении самих доноров клеток, так и в лечении других людей. Но использование аутологичных клеток не слишком реально организовать в настоящее время, подходы, основанный на аллогенных клетках, представляются более перспективными.
В США медико-биологическими исследованиями под патронажем Пентагона занимается DARPA (Defense Advanced Research Projects Agency), включая «прикладную вирусологию», нейронауки и омиксные технологии. В частности, проводится массовое биобанкирование биоматериалов военнослужащих и ветеранов, включая носителей антител к особо опасным антропозоонозам, не болевших этими заболеваниями. Исследуются генные корреляты реакции на боль (цель — создание анальгетиков, в том числе основанных на выключении «генов боли»).
Также согласно открытым источникам, создаются запасы клеточного материала (стволовые клетки, фибробласты, кератиноциты) для терапии в случае массового поступления пострадавших, резервы костного мозга для лечения радиационных поражений. Есть данные об исследовании биоматериала онкопациентов после лучевой терапии с целью изучения генетических факторов радиочувствительности.
Чэньси Тянь (Chenxi Tian) из Китайского национального центра биоинформации (CNCB) Пекинского института геномики представила слушателям метод Stamp-seq, разработанный в коллаборации с компанией SeekGene. Stamp-seq дополняет подходы пространственной транскриптомики баркодированием единичных ядер клеток. С его помощью докладчица с коллегами нашли признаки ответа на иммунотерапию при немелкоклеточном раке легкого (НМРЛ).
При всей революционной роли иммунотерапии в онкологии, она неэффективна у многих пациентов из-за влияния опухолевого микроокружения. Его изучение затруднено тем, что существующие подходы не позволяют исследовать окружающие опухоль клетки «индивидуально», с получением отдельных данных для каждой.
Эту проблему решает метод Stamp-seq, который включает маркировку единичных ядер клеток расщепляемыми баркодами. Использование существующих на рынке чипов и мультиплексное баркодирование снижает цену исследования. В итоге мультиомиксное секвенирование позволяет получить данные для отдельных клеток, включая последовательности В-клеточных рецепторов и статусы метилирования, и интегрировать эти данные с положением клеток на срезе. Среди нерешенных проблем метода докладчица упомянула потерю клеток и невозможность исследовать транскриптом цитоплазмы.
Авторы валидировали метод на образцах ткани головного мозга мышей, причем смогли надежно охарактеризовать более 30 000 клеток на срезе. Затем они проанализировали методом Stamp-seq хирургически удаленные образцы НМРЛ от пациентов, получавших иммунотерапию, и выявили в них различные клеточные сообщества, связанные с ответом на лечение. Например, образцы пациентов, для которых иммунотерапия была эффективной, были обогащены третичными лимфоидными структурами и специализированными нишами плазматических клеток. На основе полученных данных авторы нашли маркеры, с высокой точностью предсказывающие ответ на иммунотерапию и лучшую выживаемость пациентов, — комбинацию IGHG1+ плазматических клеток и антигенпрезентирующих фибробластов, ассоциированных с опухолью (apCAF)
Александр Кузнецов (ИНМЭ РАН; ООО «Полупроводниковые генетические технологии) рассказал о разработке, создании и внедрении первого отечественного полупроводникового секвенатора IONIX.
Прибор помещается в чемоданчике, его масса не превышает 60 кг. Он отличается прочностью и надежностью, низкой стоимостью эксплуатации, не требует частого сервисного обслуживания, поэтому идеально подходит для мобильных лабораторий и анализа в полевых условиях. Обширная сеть небольших лабораторий, снабженных такими приборами, может стать альтернативой сверхпроизводительным центрам секвенирования и помочь охватить услугами по секвенированию все население страны, отметил докладчик.

IONIX — полностью российский продукт: в РФ разработан как сам прибор, так и ПО, микроэлектронные чипы и реагенты. В верхней части прибора находится блок электроники, в средней части — чипы, внизу вспомогательные реагенты.
Принцип действия прибора — регистрация изменения рН во время присоединения нуклеотида ионно-чувствительным полевым транзистором (ISFET).
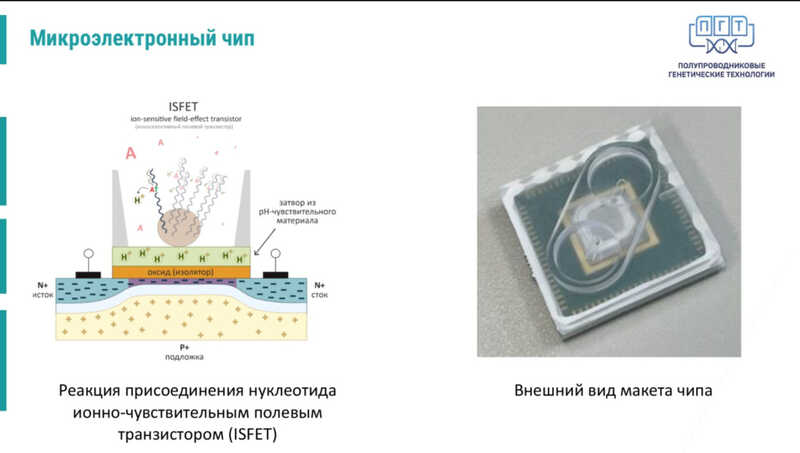
Прибор использует собственный алгоритм для определения нуклеотида, и он, по словам Александра Кузнецова, лучше, чем у IonTorrent. «Пришлось осваивать новые направления: высокоскоростная электроника, проект сложного инженерного софта», — добавил он.
Точность секвенирования прибора, по предварительным оценкам, превышает 97%, длина одноконцевого прочтения — 100–309, количество каналов считывания — от 50 до 11 300, количество прочтений за запуск — от 0,4 до 5,5 млн п.н. Время секвенирования составляет 3,5–7 часов.
Отвечая на вопросы, Александр Кузнецов заметил, что проблемы с чтением гомополимеров, о которой часто говорят применительно к полупроводниковому секвенированию, у их разработки нет. Соведущий секции Егор Прохорчук добавил, что реагенты для прибора разрабатывались в РНИМУ им. Н.И. Пирогова, а финансирование разработки было получено от частного инвестора.
Затем Юань Гао (Yuan Gao) из Китайского национального центра биоинформации (CNCB) Пекинского института геномики рассказал о методе ESPRESSO для обнаружения и количественной оценки изоформ транскриптов с помощью секвенирования РНК длинных прочтений.
Эукариотическая РНК в процессе созревания подвергается сплайсингу — вырезанию интронов и лигированию экзонов. Широко распространен альтернативный сплайсинг — за счет удаления/неудаления различных участков из одной пре-мРНК образуются разные зрелые РНК. Однако события альтернативного сплайсинга сложно идентифицировать, картируя на референсный геном короткие риды РНК, которые не могут захватить двух экзонов.
ESPRESSO (Error Statistics PRomoted Evaluator of Splice Site Options) — вычислительный инструмент, который способен определять изоформы транскриптов, в том числе ранее не описанные, используя только данные РНК-секвенирования с длинными прочтениями. Известно, что секвенирование длинных ридов (например, нанопоровое) подвержено ошибкам, но авторы подхода смогли решить эту проблему.
Разработчики ESPRESSO исходили из двух очевидных предпосылок. Во-первых, сайты сплайсинга, выравнивание вокруг которых при картировании ридов на референсный геном будет абсолютно точным, гораздо реже окажутся ошибочными, чем сайты с чем сайты с неидеальным выравниванием. Во-вторых, обнаружение сайтов сплайсинга можно улучшить, используя информацию из нескольких длинных ридов.
ESPRESSO состоит из трех этапов.Сначала длинные риды РНК-секвенирования выравниваются по референсному геному, и обнаруживаются предполагаемые сайты сплайсинга. Затем для каждого длинного рида РНК-секвенирования ESPRESSO рассматривает все высокодостоверные сайты сплайсинга в соответствующем гене и определяет их оптимальный набор. И наконец, результаты сопоставляются с каталогом транскриптов (являются ли обнаруженные сайты известными, новыми или не полностью совпадающими с известными), восстанавливаются последовательности изоформ транскриптов.
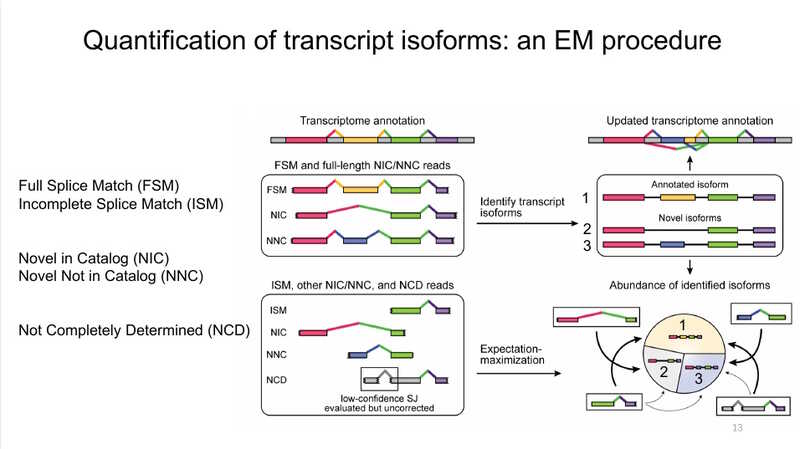
ESPRESSO повышает точность определения контрольных образцов — Spike-In RNA Variants (SIRV), отметил докладчик.
В качестве примера исследователи проанализировали транскрипты гена CD44 в клеточных линиях рака простаты PC3E и GS689 и обнаружили десятки новых изоформ. Переключение изоформ этого гена играет важную роль в эпителиально-мезенхимальном переходе. Кроме того, они составили с помощью ESPRESSO каталог изоформ транскриптов из 30 тканей человека, представляющих различные анатомические области.
В конце доклада Юань Гао упомянул еще один инструмент для идентификации и количественного определения транскриптов на основе данных РНК-секвенирования с длинными прочтениями, представленный на github — BroCOLI (Bron-Kerbosch calibrator of Long-read Isoform). По его словам, это решение поддерживает как приложения для анализа суммарной РНК, так и для пространственной транскриптомики и транскриптомики единичных клеток, отличается быстротой, низким потреблением памяти и высокой производительностью.
Павел Бобрик (Республиканский научно-практический центр детской онкологии, гематологии и иммунологии, Беларусь) выступил с докладом «Третичная биоинформатическая обработка данных высокопроизводительного секвенирования в диагностике первичных иммунодефицитов».
Первичные иммунные дефициты (ПИД) — широкая группа заболеваний, связанных с нарушением различных звеньев иммунитета и вызванных разнообразными генетическими факторами.
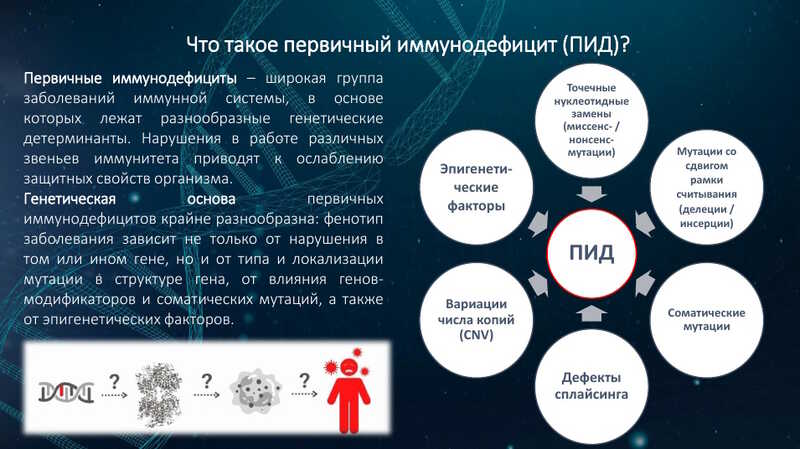

Диагноз подтверждается высокопроизводительным секвенированием. Это может быть как секвенирование панели генов (обычно от 10 до 500), так и секвенирование экзома (всех кодирующих последовательностей) или полногеномное секвенирование. Последний вариант пока еще недоступен для многих пациентов, в то же время полноэкзомное секвенирование доступно и при этом клинически эффективно.
Результатом биоинформатической обработки данных секвенирования является приоритизация обнаруженных генетических вариантов с использованием различных баз данных и предикторов патогенности.

Проблемы биоинформатической обработки — это прежде всего избыточность информации в файлах, полученных при аннотации генетических вариантов. Объем слишком велик для ручного процессинга. Анализ на сторонних онлайн-платформах, в свою очередь, дорого стоит и не гарантирует сохранности данных — от утечки не застрахован никто. Популярная платформа BaseSpace Variant Interpreter с 6 января 2025 года недоступна, но есть другие интересные решения — Franklin (Qiagen), а также OakVar, отметил докладчик.
Еще одна проблема — отсутствие единой, «универсальной» базы данных для аннотации. Интересный универсальный ресурс — dbNSFP, однако использовать только его не представляется возможным, в частности, из-за отсутствия аннотации для делеций и инсерций, интронных замен и синонимичных вариантов. Его может дополнить использование инструмента для аннотации Annovar.
Российские решения для массового параллельного секвенирования ДНК представил Яков Алексеев (ООО «Синтол»).
Существует отечественный набор реагентов для подготовки библиотек SyntEra: стоимость подготовки одного образца — 3000 р., общее время подготовки геномных библиотек — 1 час, а трудозатраты оператора — около 15 мин. Клиентская база включает уже более 50 организаций по всей России. Сравнение с набором NEB показало, что у SyntEra-DNA меньше средняя длина фрагмента между адаптерными последовательностями, при этом качество прочтений высокое для обоих способов пробоподготовки. Благодаря иммобилизации фермента на магнитных шариках размер фрагментов не зависит от количества внесенной ДНК.
Российский прибор для массового параллельного секевенирования «Нанофор СПС», о котором рассказывали два года назад на МД-2023, поступил в продажу.

При использовании американских реагентов качества данных не хуже, чем у MiSeq. Запуск на химии «Синтол» продемонстрировал стабильную работу с 75SE. У компании «Синтол» есть демолаборатория, где можно поработать на разных приборах и оценить их возможности.
Кроме того, «Синтол» предлагает набор для метагеномного секвенирования и метабаркодинга MetaGen-16sRNA. Набор позволяет оценивать состав микробиома почвы или раневых тканей. Сборка малых геномов и аннотация функций проходит успешно.
На «Нанофор СПС» также можно проводить таргетное секвенирование для выявления различных типов патогенных мутаций (как делеций и инсерций, так и SNV).
На сегодняшний день в РФ инсталлировано 15 приборов «Нанофор СПС». Также начата разработка «Нанофора СПС 2.», по характеристикам сходного с NextSeq 550 (Illumina) или DNBSEQ-G50 (BGI, Китай).
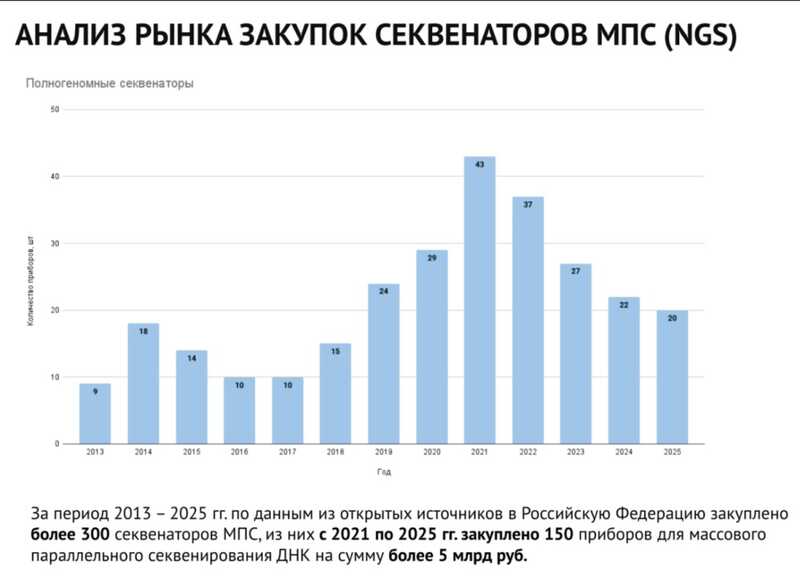
В заключение докладчик рассказал об инженерных курсах Университета «Сириус», где готовят специалистов, способных обслуживать приборы для молекулярно-генетических исследований. Яков Игоревич — один из преподавателей этих курсов.
Темой доклада Николая Кулемина (ФНКЦ ФХМ им Ю.М.Лопухина ФМБА России) были скрытые технологические особенности NGS, которые стоит учитывать при анализе данных.
Приборы для NGS из стран Запада, доступные в России, — это прежде всего Illumina (активно применяются приборы, использующие двухцветную химию, — NovaSeq 6000, NextSeq 2000; приборы на четырехцветной химии — HiSeq1500/2500/4000, NextSeq 500 — выводятся из употребления). Самые массовые на рынке — китайские приборы DNBSEQ (MGI), которые используют для получения ДНК-наношариков (аналогов кластера в технологии Illumina) репликацию катящегося кольца: DNBSEQ G400 и DNBSEQ T7. Выходят на российский рынок секвенаторы компании Sesana (Genemind, Геноскан), аналогичные приборам Illumina.
Также на рынке представлены тесты для анализа ДНК, ориентированные на решение разных задач.
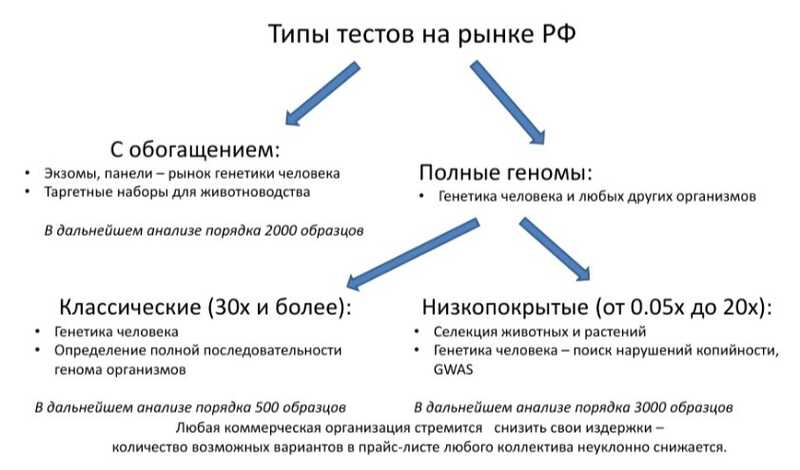
Докладчик и его коллеги занимаются медицинской генетикой, где особенно важно понимать, что необнаружение патогенной мутации врачи и пациенты воспринимают как ее отсутствие и в соответствии с этим принимают дальнейшие решения. Поэтому при секвенировании с обогащением необходимо прочтение всех позиций матрицы с покрытием не менее 20х и отклонением не более 1%. Не нужно ориентироваться на среднее покрытие — необходимо оценивать процент позиций с 20х и более. Важно также знать особенности конкретного набора.
Что касается секвенирования полных геномов, не на всех приборах можно получить покрытие 30х для генома человека без разделения на дорожки или баркоды. Это возможно на Illumina NovaSeq 6000, Illumina Х, DNBSEQ T7 и DNBSEQ T20. На других приборах необходимая глубина покрытия достигается путем суммирования технических повторов (fastq-файлов, полученных секвенированием одной библиотеки на одной дорожке одного прибора с одним баркодом). При этом не следует «разбивать» данные на технические повторы с покрытием менее 7х.
При более низком покрытии (например, при решении агротехнических задач) также крайне важно сохранение его равномерности, контроль среднемедианного покрытия и доли ошибки в конкретной задачи.
«Будьте внимательны к сиквенсам! Ваши итоговые выводы в эксперименте всегда основываются на корректной работе оборудования», — подчеркнул Николай Кулемин.
Назар Самаров-Бестужев (ООО «Альбиоген») рассказал о линейке приборов китайской компании Salus Biomed — Saluseq Nimbo, Pro и Evo, отличающихся в первую очередь производительностью, а также о QNome-3841, первом коммерческом китайском нанопоровом секвенаторе от QiTan Tech. (Подробнее на PCR.NEWS.)

Докладчик отметил, что приборы для нанопорового секвенирования полностью производятся в QiTan, с собственными патентами на все разработки, так что патентные споры и вторичные санкции компании не угрожают. QiTan предлагает комплексное решение для нанопорового секвенирования, включающее приготовление библиотек и анализ данных. Более производительный прибор — QPursue (6 тысяч пор на ячейку, длина прочтений — от 100 п.н. до 1 Мб, производительность портативного варианта до 60 Гб, точность при покрытии 1х — Q20). В 2026 году ожидается выпуск нового прибора QPinnacle2 (16 тысяч пор на ячейку, производительность до 800 Гб за запуск).
В завершение секции Анастасия Букреева (ООО «Эмджиай Тех Рус») рассказала о программном обеспечении MGI TECH для автоматического процессинга данных таргетного секвенирования.
ATOPlex — платформа MGI для таргетного секвенирования — имеет широкий спектр применения, не только в медицине, но и в фундаментальных исследованиях, сельском хозяйстве, криминалистике, а также в сервисах direct-to consumer. На сайте производителя можно бесплатно выполнить дизайн праймеров. Панелями ATOPlex пользуются по всему миру; создано более 100 кастомных панелей под самые разные задачи. ПО для анализа данных, ATOPlex MultiPCR Explorer, широко применяется для исследования опухолевых генов, идентификации патогенов и других задач. Докладчица рассказала о хранении данных и системе автоматизации ZLIMS, а также об анализе данных.
Информация о докладчиках
Глушаков Руслан Иванович, д.м.н., доцент, Научно-исследовательский отдел Военно-медицинской академии им. С.М. Кирова
Chenxi Tian, Dr., China National Center for Bioinformation; Beijing Institute of Genomics, Chinese Academy of Sciences
Кузнецов Александр Евгеньевич, д.т.н., ИНМЭ РАН; ООО «Полупроводниковые генетические технологии»
Yuan Gao, Dr., China National Center for Bioinformation; Beijing Institute of Genomics, Chinese Academy of Sciences
Бобрик Павел Юрьевич, Республиканский научно-практический центр детской онкологии, гематологии и иммунологии, Минский р-н, д. Боровляны, Беларусь
Алексеев Яков Игоревич, директор по науке ООО «Синтол»
Кулемин Николай Александрович, н.с. лаборатории молекулярной генетики человека, ФГБУ ФНКЦ физико-химической медицины имени академика Ю.М. Лопухина ФМБА
Самаров-Бестужев Назар Игоревич, ООО «Альбиоген»
Букреева Анастасия Сергеевна . ООО «Эмджиай Тех Рус» (MGI TECH)


 Меню
Меню





 Все темы
Все темы



 0
0












