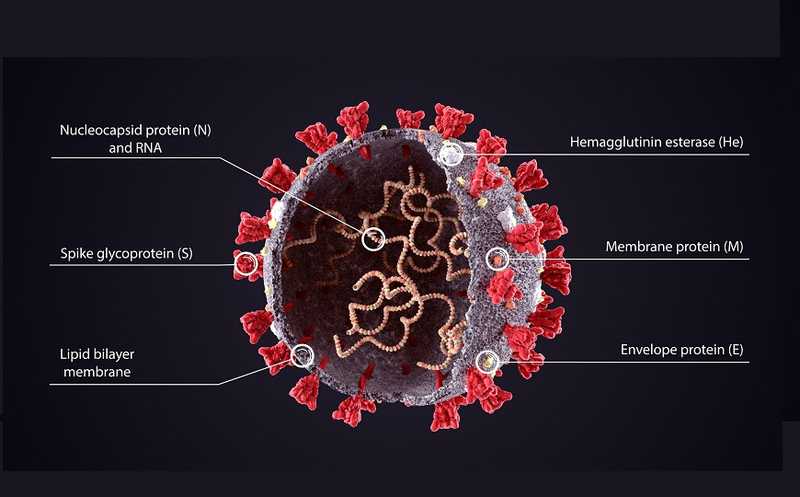
В России разрешили менять штаммы зарегистрированных вакцин от COVID-19
Moderna покупает OriCiro Genomics, «Медскан» выкупила лаборатории KDL, зарегистрирован отечественный кожный тест на Т-клеточный иммунитет к COVID-19. Об этом и многом другом в рубрике «Бизнес-среда».
Отставки/назначения
Исполнительный директор фармкомпании Novavax уходит в отставку
Стэнли Эрк, исполнительный директор компании Novavax, с 23 января 2023 года уходит в отставку. Его сменит экс-глава компании Harmony Biosciences Джон Джейкобс.
«Мой опыт работы в Novavax, особенно управление компанией во время глобального реагирования на пандемию, стал кульминацией моей 40-летней карьеры руководителя в сфере биотехнологий», — прокомментировал свой уход Стэнли Эрк, который в следующие 15 месяцев будет занимать должность советника в компании.
Эрк руководил Novavax последние 12 лет. Его основной задачей с 2019 года было вывести фармкомпанию в лидеры по производству вакцин от новой коронавирусной инфекции.
Novavax разработал вакцину NVX-CoV2373 (Covovax), которая содержит рекомбинантные наночастицы с полноразмерным S-белком SARS-CoV-2и адъювант Matrix-M. Это первая белковая вакцина, показавшая высокую эффективность. Она была одобрена в Евросоюзе и Великобритании, а в 2022 году и на территории США, где спрос на нее оказался не слишком большим.
Инвестиции
Chiesi Farmaceutici покупает Amryt Pharma за $1,48 млрд
Итальянская компания Chiesi Farmaceutici купит ирландского разработчика препаратов для терапии редких заболеваний Amryt Pharma за $1,48 млрд. Поскольку советы директоров обеих компаний уже одобрили слияние, сделка может быть закрыта в первой половине 2023 года.
Выручка Amryt за первые девять месяцев 2022 года составила $188,8 млн, а прогноз на год — $260–270 млн. Самый продаваемый препарат компании — Myalepta для лечения липодистрофии, — принес в третьем квартале 2022 года $37,9 млн.
«Портфолио Amryt, а также их опыт помогут нам в нашей миссии по обеспечению лекарствами пациентов, независимо от того, насколько редкие их заболевания», — заявил генеральный директор Chiesi Group Марко Веккья.
Moderna покупает OriCiro Genomics за $85 млн
Американская биотехнологическая компания — разработчик препаратов на основе мРНК Moderna купила компанию OriCiro Genomics, которая имеет в своем активе технологии бесклеточного синтеза и амплификации ДНК для применения в генной и клеточной терапиях, а также в синтетической биологии. Сумма сделки оценивается в $85 млн.
«С этим приобретением мы получим лучшие в своем классе инструменты для бесклеточного синтеза ДНК и амплификации плазмидной ДНК, ключевого строительного блока в производстве мРНК. Технология OriCiro стратегически дополнит наш производственный опыт и ускорит наши исследования и разработки», — заявил главный исполнительный директор Moderna Стефан Бансель.
Приобретение OriCiro укладывается в стратегию Moderna по развитию мРНК-препаратов. Предыдущее крупное вложение американской компании в этой области — создание предприятия по разработке и производству мРНК-вакцин в Великобритании в конце 2022 года. Этот завод также предназначен для расширения производства вакцин компании против новой коронавирусной инфекции.
«Медскан» купила сеть лабораторий KDL
Группа компаний «Медскан» закрыла сделку по покупке сети лабораторий KDL, выкупив актив у фонда прямых инвестиций UFG Private Equity. Сумма могла составить более 15 млрд рублей.
В результате сделки компания «Диагностика» (основное юридическое лицо KDL) перешла в собственность одной из дочерних компаний группы «Медскан». Как пояснил «Ведомостям» представитель фонда UFG Private Equity, продажа была обусловлена тем, что стандартный срок работы фонда с активом составляет 10–12 лет, поэтому поиск потенциального покупателя начался еще в 2021 году.
Фонд приобрел сеть лабораторий KDL в 2012 году. Тогда совместно с CapMan Russia и Европейским банком реконструкции и развития у основателей Александра Девяткова и Владимира Полякова была выкуплена 75%-ная доля сети.
Сеть KDL насчитывает 13 региональных лабораторий и более 350 медицинских офисов по всей России. Трафик пациентов компании за 2022 год должен составить около 2,5 млн пациентов. Чистая прибыль компании в 2021 году достигла 2,2 млрд рублей, а совокупный долг — 1,98 млрд рублей.
Сеть медицинских компаний «Медскан» была создана в 2014 году. На текущий момент в ее составе 58 медицинских центров: диагностические, многопрофильные клиники, госпитали с хирургическим стационаром и онкоцентры. Также в составе группы находится филиал израильской клиники Хадасса.
MSD и Kelun-Biotech займутся разработкой онкопрепаратов за $9,3 млрд
Компания MSD и китайская Kelun-Biotech достигли соглашения о совместной разработке препарата от рака. Общая сумма сделки может достичь $9,3 млрд. Сотрудничество предполагает получение компанией MSD эксклюзивных лицензий на исследования, разработку, производство и коммерциализацию семи конъюгатов «антитело-лекарство» (ADC).
«Прогресс в технологиях ADC приводит к появлению нового поколения кандидатов, предназначенных для более точного нацеливания и доставки мощных противоопухолевых агентов к опухоли», — прокомментировал сделку президент исследовательских лабораторий MSD Дин Ли.
Компания MSD, по условиям соглашения, будет иметь эксклюзивные возможности на получение дополнительных лицензий для ADC-кандидатов. При этом владелец лицензий — Kelun-Biotech оставляет за собой право проводить исследования, разрабатывать, производить и коммерциализировать препараты на территории материкового Китая, Гонконга и Макао.
Kelun-Biotech получит авансовый платеж в размере $175 млн, в дальнейшем будет иметь право на получение платежей за разработку, регулирование и продажи ADC-препаратов на общую сумму до $9,3 млрд, а также многоуровневые роялти с чистых продаж. Сообщается, что MSD также намерена инвестировать в акционерный капитал Kelun-Biotech.
Регуляторика
В России разрешено менять штаммы зарегистрированных вакцин от COVID-19
Правительство РФ приняло поправки к постановлению № 441, которые позволят изменять состав отечественных вакцин против коронавирусной инфекции. Это было сделано для борьбы с новыми вариантами SARS-CoV-2, ускользающие от иммунного ответа за счет множественных мутаций в S-белке.
Внести изменения в правительственное постановление предложило ФМБА, а Минздрав оформил поправки. В постановление № 441 добавлен пункт 17(1.1)—17(1.10), который поясняет порядок внесения изменений в регистрационное удостоверение, касающихся изменений состава штаммов вакцин.
Для этого заявитель должен будет предоставить результаты доклинических исследований защитной эффективности и безопасности, а также оценки реактогенности и иммуногенности вакцины с участием не менее 50 добровольцев. Срок одобрения изменений в регистрационном удостоверении составит 16–38 дней.
Также на год продлен срок действия РУ, выданных по ускоренной процедуре для препаратов, применяемых в условиях чрезвычайной ситуации или борьбы с опасными заболеваниями — в их числе лекарства от коронавирусной инфекции. Выданные по такой схеме РУ будут действовать до 1 января 2024 года.
Двенадцать групп рецептурных лекарств будут исключены из перечня для онлайн-торговли
Правительство России утвердило критерии формирования перечня рецептурных лекарственных препаратов для проведения эксперимента по дистанционной торговле, который будет запущен на территории столицы и двух областей страны.
Соответствующее постановление № 2465 от 28.12.2022 подписал премьер-министр Михаил Мишустин. Из эксперимента исключены 12 групп лекарств: наркотические средства и их прекурсоры, сильнодействующие вещества, радиофармпрепараты и препараты для иммунобиологии, термолабильные средства с температурой хранения до 15° С, спиртосодержащие препараты с долей этанола более 25% и лекарственные препараты аптечного изготовления.
Также в перечень исключенных из эксперимента лекарств вошли анаболические и антипсихотические средства, анксиолитики, снотворные и седативные средства, препараты, применяемые для прерывания беременности, препараты, подлежащие предметно-количественному учету (ПКУ) и содержащие запрещенные к обороту ядовитые вещества.
Исключения будут действовать на протяжении всего эксперимента — с 1 марта 2023 года по 1 марта 2026 года.
Роспотребнадзор предложил зарегистрировать кожный тест на иммунитет к COVID-19
НИИ эпидемиологии и микробиологии Пастера (Роспотребнадзор) подал заявку в Минздрав на регистрацию препарата «КоронаДерм-PS» для выявления клеточного иммунитета к возбудителю COVID-19.
Препарат представляет собой раствор для внутрикожного введения объемом 0,2 мл, содержащий рекомбинантный аллерген из иммуногенных участков белков коронавируса. Положительный тест означает, что у человека имеется клеточный иммунитет. Отрицательный указывает на то, что ему нужно вакцинироваться либо ревакцинироваться.
Препарат прошел фазы 1-2 КИ с участием 460 добровольцев. После его регистрации у пациентов появится возможность проверить Т-клеточный иммунитет к COVID-19 в поликлиниках. Этот вид иммунитета способен обеспечить легкое протекание болезни при заражении вариантом коронавируса, ускользающим от антител (как, например, новые субварианты омикрона XBB). В настоящее время проверить клеточный иммунитет к возбудителю коронавирусной инфекции можно только в специализированных лабораториях, и стоимость анализа относительно высока (около 10 тысяч рублей).
Международная регуляторика
FDA по ускоренной схеме одобрило препарат Лекемби для лечения болезни Альцгеймера
Несмотря на сомнения, связанные с безопасностью, Управление по контролю продуктов и лекарств США (FDA) по ускоренной схеме одобрило препарат Лекемби (МНН — леканемаб, lecanemab-irmb) для лечения болезни Альцгеймера. Препарат разработан компаниями Biogen и Eisai R&D Management.
Лекемби — это гуманизированное моноклональное антитело, нацеленное на растворимую форму бета-амилоида. В фазе 3 КИ через 18 месяцев после начала терапии когнитивные функции участников снизились в группе, принимавшей препарат, в среднем на 1,21 балла по шкале CDR-SB и на 1,66 балла в группе плацебо. У пациентов первой группы, по данным ПЭТ, существенно уменьшилось отложения амилоида в головном мозге. В исследовании приняли участие 1795 человек в возрасте от 50 до 90 лет с ранней болезнью Альцгеймера.
Применение Лекемби вызвало инфузионные реакции у 26,4% участников, аномалии визуализации, связанные с амилоидом, включая отек или появление выпота, — у 12,6%.
Препарат может быть назначен людям с умеренными нарушениями когнитивных функций либо деменцией в легкой степени, связанными с болезнью Альцгеймера. Получающим лечение рекомендовано пройти три МРТ в первые полгода после начала терапии.
FDA одобрило первый ингибитор капсида для терапии ВИЧ
Кроме того, в США одобрен препарат ленакапавир (Sunlenca) от Gilead Sciences, ранее разрешенный в Евросоюзе и Канаде. Он предназначен для взрослых с ВИЧ-инфекцией и множественной лекарственной устойчивостью.
Это препарат нового класса — капсидный ингибитор, нарушающий структуру белковой оболочки вируса. Его можно принимать перорально или в виде подкожной инъекции. После инициирующей дозы раз в шесть месяцев вводят поддерживающие дозы в комбинации с другими противовирусными средствами. Помимо эффективности против лекарственно-устойчивого ВИЧ-1, редкое применение — еще одно преимущество нового препарата.
Безопасность и эффективность ленакапавира подтверждены в клиническом исследовании при участии 72 пациентов с устойчивостью к различным классам антиретровирусных препаратов. В течение двух недель после начала лечения уровень вируса в крови снизился у 87,5% участников, которые получали ленакапавир, и лишь у 16,7% пациентов из группы плацебо.
Через полгода после начала терапии у 81% пациентов, которые получали ленакапавир в сочетании с другими антиретровирусными средствами, выявили супрессию РНК ВИЧ. Через год после начала КИ супрессия сохранялась у 83% участников.


 Меню
Меню





 Все темы
Все темы




 0
0