МД-2025. Настоящее и будущее молекулярной диагностики. Часть 1
Что происходит с охватом вакцинацией в России, какие переносимые комарами инфекции угрожают европейцам и какой этап в развитии молекулярной диагностики последует за NGS — вот лишь некоторые темы, которые обсуждались на пленарном заседании конференции «Молекулярная диагностика 2025».

Участников конференции «Молекулярная диагностика 2025» приветствовали чл.-корр. РАН Вероника Скворцова, руководитель ФМБА России, и Андрей Плутницкий, зам.министра здравоохранения Российской Федерации.
Как отметил чл.-корр. РАН Андрей Иванов, Президент Ассоциации специалистов и организаций лабораторной службы «Федерация лабораторной медицины», тематика каждого из докладов пленарного заседания в дальнейшем была раскрыта на секциях конференции. Перспективы развития молекулярной диагностики и ее применение в борьбе с инфекционными заболеваниями были в числе ключевых тем.
С первым докладом, посвященным инфекционным заболеваниям в современном мире, традиционно выступил Владимир Чуланов (НМИЦ фтизиопульмонологии и инфекционных заболеваний Минздрава России).
По данным ВОЗ, ежегодно в мире отмечается 2 млрд случаев инфекционных болезней, и они остаются одной из ведущих причин смертности. На эволюцию и распространение инфекционных заболеваний в мире влияет ряд факторов: появление новых, ранее неизвестных патогенов, изменение климата, миграция населения и рост его численности (если в 1920-е годы Землю населяло 2 млрд человек, то сегодня 8 млрд.), расширение ареала обитания людей, которое сопровождается встречами с новыми патогенами, а также развитие новых технологий (здесь примером служат инфекции, связанные с оказанием медицинской помощи).
Бремя инфекционных заболеваний в РФ в 2024 году — 36,1 млн, все еще больше, чем в допандемийном 2019-м.

В основном это острые респираторные вирусные инфекции (87%, не включая COVID-19, вклад которого составил лишь около 3%). В последние два года возросла заболеваемость по ряду нозологий, включая корь, краснуху (здесь впечатляющий рост в 85 раз незначителен в абсолютных цифрах, тем не менее это печально, так как речь идет о вакциноуправляемой инфекции). В 1,7 раз выросло число случаев внебольничной пневмонии, а также завозных вирусных инфекций, таких как лихорадка денге и лихорадка Западного Нила.
В 2025 году, если исключить респираторные инфекции, 37,7% приходится на расшифрованные кишечные инфекции, 9% — на социально значимые заболевания. В несколько раз выросло число случаев менингококковой инфекции, тенденцию к росту демонстрируют геморрагическая лихорадка с почечным синдромом (ГЛПС), клещевой боррелиоз, краснуха, грипп. Отмечены завозные случаи брюшного типа, холеры. Среди инфекций, связанных с медицинской помощью, — вирусные гепатиты В и С (суммарно более 170 случаев в Бурятии, Камчатском крае, Курской области). Крупные вспышки кишечных инфекций происходили в Самаре (гепатит А), Дагестане, Якутии и других регионах. В Москве отмечено более 900 случаев менингококковой инфекции.
Заболеваемость и смертность от COVID-19 ожидаемо упала. Патогенность коронавируса SARS-CoV-2 снижается, и сейчас это обычная сезонная инфекция, отметил Владимир Петрович. Заболеваемость COVID-19 снижается во всем мире (хотя следует понимать, что «снижение» может быть результатом прекращения тестирования; в странах Европы или в Бразилии, где тестирование продолжается, число случаев остается заметным). Сохраняются риски, связанные с вариантами вируса, вызывающими интерес (JN.1) и находящимися под наблюдением (XFG, или «стратус», NB.1.8.1 и др.) или новыми, еще неизвестными вариантами. Докладчик напомнил, что ущерб от COVID-19 был громадным — к началу 2025 года более 7778 млн случаев заболевания и как минимум 7 млн случаев зарегистрированных летальных исходов; реальное же количество смертей могло превысить 20 млн.
Владимир Чуланов коснулся других чрезвычайных ситуаций в области общественного здравоохранения, имеющих международное значение (PHEIC). С тех пор, как это понятие было введено ВОЗ, PHEIC объявляли восемь раз, включая птичий грипп H1N1 в 2009 году, вспышку полиомиелита в2024-м, лихорадку Эбола в 2014-м и 2019-м, лихорадку Зика в 2016-м, и, наконец, COVID-19 и две последующие вспышки оспы обезьян (мпокс).
Сейчас в перечень приоритетных патогенов, опубликованный ВОЗ в июле 2024 года, входят 32 патогена, из них 27 — вирусы. Документ ВОЗ об изучении новых и появляющихся патогенов включает 89 заболеваний, из них 59 вирусной этиологии.
В качестве примера недавних эпидсобытий докладчик рассказал о вспышке лихорадки Марбург в Руанде в 2024 году (на конец октября были зафиксированы 66 случаев заболевания и 15 с летальным исходом: два подозрительных случая в Германии не подтвердились).
Лихорадка Эбола убила еще больше людей, и в 2025 году в труднодоступной сельской местности ДРК снова произошла вспышка, уже шестнадцатая с 1976 года, которая завершилась лишь недавно (64 случая, 45 летальных исходов, таким образом, коэффициент летальности составил 70,3%). Согласно геномным данным, эта вспышка является новым зоонозным событием, не связанным с предыдущими вспышками и передачей от человека к человеку. Более 26 тысяч человек было привито вакциной Эрвебо на основе штамма Заир (rVSVΔG-ZEBOV-GP), 31 пациент получил лечение моноклональными антителами ансувимаб-зикл (Эбанга).
Докладчик также рассказал о вспышках оспы обезьян (мпокс); вторая из них началась в 2024 году и продолжается до сих пор.
«Комариные лихорадки» вместе с комарами-переносчиками распространяются за пределы тропических стран. Вирус лихорадки чикунгунья получил название от слова на языке кимаконде, народа юга Танзании, которое обозначает «стать скрюченным» — лихорадка сопровождается сильными болями в суставах, возможно, вызванными репликацией вируса в артроцитах. С начала 2025 года лихорадка чикунгунья зарегистрирована в 16 странах и территориях; в том числе 768 случаях отмечено во Франции, 370 — в Италии. Крупная вспышка с сотнями заболевших произошла в Китае.
Лихорадка Западного Нила «уже наша», отметил докладчик: в 2024 году в РФ зарегистрировано 426 случаев и 18 летальных исходов. Лихорадка денге — самое распространенное вирусное заболевание, передающееся через укусы комаров; в мире ежегодно регистрируются десятки миллионов случаев и десятки тысяч летальных исходов, и она тоже появляется в Европе (десятки случаев в этом году).
Однако это небольшие цифры по сравнению с гепатитами В и С. Глобальная смертность от них сейчас составляет 16,6 на 100 тысяч человек, тогда как целевой показатель на 2025 год — 10. В РФ отмечается рост заболеваемости хроническим гепатитом С после «спада» во время пандемии (почти 51 тысяча случаев), причем это не новые случаи, у многих пациентов уже развиваются фиброз и цирроз.

Среди первоочередных методов борьбы с гепатитом С — скрининг и расширение доступа к лечению. В настоящее время терапией охвачено менее 9% из состоявших на учете пациентов, однако в последние годы охват превышает число вновь выявленных пациентов. Меры по борьбе с гепатитом включены в нацпроект «Продолжительная и активная жизнь» и в госпрограммы по борьбе с инфекционными заболеваниями.

Проблемой остается снижение охвата вакцинацией от инфекционных заболеваний. Для 2023 года по сравнению со среднемноголетним уровнем 2018— 2020 гг. зафиксировано падение на 11,2% для коклюша, на 5,4% для дифтерии, на 6,4% для столбняка, на 7,9% для полиомиелита, на 21,3% для кори, более чем на 40% для свинки.
При этом национальный календарь прививок сейчас включает иммунизацию против 12 инфекций за счет федерального бюджета и против 16 инфекций за счет регионального. В 2025 году к ним добавляются вакцины против менингококковой, ротавирусной и пневмококковой (для взрослых) инфекции, в 2926 году должна быть включена вакцина против ВПЧ, в 2027-м — против ветряной оспы.
Владимир Чуланов также представил основные положения стратегии борьбы с антимикробной резистентностью в РФ до 2030 года, и подчеркнул, что мониторинг распространения АМР возможен лишь при наличии эффективных диагностическх методов.
В завершение он процитировал генерального директора ВОЗ: говоря о прекращении ЧС, связанной с SARS-CoV-2, Тедрос Аданом Гебреисус сказал, что ковид оставил в нашем мире шрамы, которые «должны служить постоянным напоминанием о возможности появления новых вирусов с разрушительными последствиями».
Доклад Германа Шипулина (ЦСП ФМБА России, Центр постгеномных технологий) назывался «Молекулярная диагностика в XXI веке: камо грядеши?»
Все мы помним имена «отцов основателей» MDx и основные вехи: открытие структуры ДНК, методы гибридизации нуклеиновых кислот (Сол Шпигельман и Эдвин Саузерн), первый получивший широкое применение метод секвенирования ДНК (Фредерик Сэнгер), полимеразная цепная реакция (Кэри Муллис). Вопрос о создателях секвенирования нового поколения (NGS), оно же массовое параллельное или высокопроизводительное секвенирование, уже вызывает затруднения; имена, которые стоит помнить, — сэр Шанкар Баласубраманиан и сэр Дэвид Кленерман, изобретатели секвенирования Solexa (Illumina). Хотя существенный вклад внесли и другие, например, Джонатан Ротберг и Джордж Черч. Конечно, развитие молекулярной диагностики на этом не остановится, но что ожидает нас в будущем?

В 2014 году на очередной конференции «Молекулярная диагностика» обсуждались быстрые темпы роста направления. Предполагалось, что прорыва следует ждать в генетике и онкологии, а не в диагностике инфекционных заболеваний. Однако темпы роста в MDx вернулись к тем, что характерны для лабораторной диагностики в целом.
Рост, тем не менее, продолжается, и к 2032 году прогнозируется объем мирового рынка молекулярной диагностики (не только клинической) — 51 млрд долларов при совокупной среднегодовом темпе роста 10,6%. Рынок клинической диагностики в 2031 году может превысить 10 млрд долларов, а к 2034 году достичь объема в 13,5 млрд. Что касается рынка MDx в РФ, по оценке докладчика он может составлять около 30 млрд рублей.
Пропорциональный вклад в рост вносит диагностика инфекционных болезней. Как показали последние пять лет, их рано сбрасывать со счетов; в 2019 году среди причин смерти в РФ лидировали сердечно-сосудистые и онкологические заболевания, в 2021 году картина резко изменилась. Но два миллиарда случаев инфекционных заболеваний в мире ежегодно, о которых говорил Владимир Чуланов, — это далеко не только COVID-19:
Инфекционных болезней известно более тысячи. В развитых странах в структуре смертности они составляют около четверти, в странах с низким уровнем дохода — до 50%. Если от COVID-19 умерло, по разным оценкам, от 6,9 до 20 млн человек, то от туберкулеза — 1,2 млн только в 2024 году. Туберкулезом заражается 10 млн человек в год, ВИЧ — 40 млн, малярией — более 300 млн. Ужасает статистика смертей от сепсиса и внутрибольничных инфекций, в том числе связанных с антимикробной резистентностью. Как это ни печально, это открывает перспективы для развития MDx.
В нашей стране за последние десять лет произошли существенные изменения. В 2014 году инсталляционная база амплификаторов оценивалась в 5000, рынок переключался на ПЦР и реальном времени и автоматизацию, появлялись закрытые платформы от зарубежных производителей (Cobas, Allinity). Отечественных автоматизированных платформ для MDx тогда не существовало (сейчас есть движение в этом направлении, появились отечественные экстракторы нуклеиновых кислот от нескольких компаний), как и отечественных приборов для сэнгеровского секвенирования и NGS (сейчас существуют инструменты компании «Синтол»). Российских приборов для масс-спектрометрии не было 10 лет назад и нет сейчас. Количество амплификаторов возросло примерно вчетверо.
Появились отечественные тесты на основе секвенирования, тест-системы для молекулярной онкологии и генетических заболеваний (но пока не для фармакогенетики), а также тест-системы для геномной дактилоскопии.
Портфолио тестов у российских производителей шире, чем за рубежом, отметил докладчик. Разнообразие выше, в том числе за счет редких инфекций. Тем не менее нерешенной задачей остается расшифровка инфекционных синдромов — идентификация возбудителей инфекций респираторного тракта, гастроэнтеритов, геморрагических лихорадок, менингитов/энцефалитов, не А–Е гепатитов. Приблизительно в 15–50% случаев возбудитель остается неустановленным. Необходима платформа, которая могла бы поднять эффективность хотя бы до 95%.
В настоящее время типичная платформа, используемая в лаборатории, предназначена для большого количества анализов с помощью небольшого количество тестов. При этом, по оценкам 2011 года, существует не менее 1400 патогенов человека, включая вирусы, бактерии, протистов и гельминтов, и в любой момент может появиться новый, еще неизвестный патоген.
Существуют тест-наборы для выявления десятков патогенов, в том числе отечественные (например, ARVI-screen-short, который выявляет 28 видов вирусов респираторных заболеваний). Но таким образом достичь 100%-ной расшифровки невозможно.
На западе сейчас разрабатывают быстрые супермультиплексные тесты для применения в местах оказания медицинской помощи (BioFire/Biomerieux). Вершина этого направления GenMarkDx (с 2021 года принадлежит Roche). Их панель маркеров сепсиса включает 62 мишени и 10 локусов резистентности. Автоматизированную систему для быстрой детекции 20 мишеней, способную проводить как изотермическую амплификацию, так и ПЦР, разработали и в ЦСП ФМБА.
Но если переходить к большему объему тестирования и большему разнообразию мишеней, придется строить огромные устройства, сравнимые с первыми вычислительными машинами, такими как ENIAC (он был построен в 1946 году, весил 30 тонн и мог выполнять 5000 операций в секунду). Путь, по которому пошла электроника и который вывел ее на новый уровень — смена платформы.
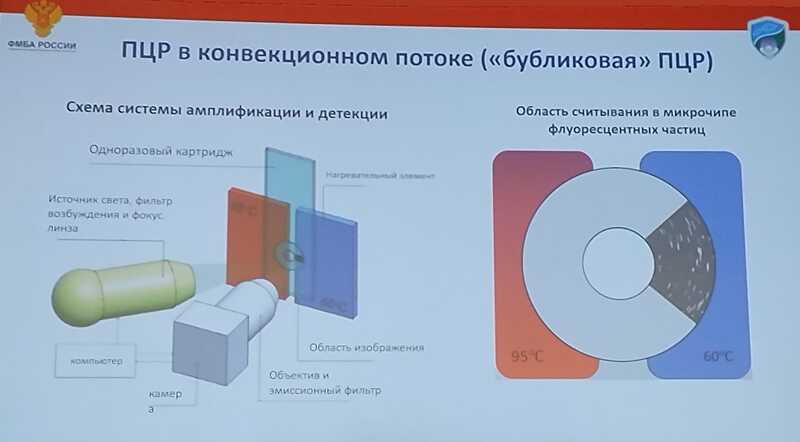
Новой платформой может стать бубликовая, или пончиковая ПЦР (donut PCR, подробнее на PCR.NEWS). Первый автор публикации 2021 года, Дмитрий Ходаков, который в настоящее время работает в ЦСП ФМБА России, рассказал об этой платформе на заключительном пленарном заседании конференции. Не исключено, что «бублик» с циркулирующей реакционной смесью и чипом, способный за минуты детектировать сотни биомаркеров, заменит пробирки в громоздких амплификаторах.

Наконец, для мирового рынка секвенирования тоже прогнозируется устойчивый рост, до 72,2 млрд долларов в 2034 году (эта оценка также включает не только молекулярную диагностику).
На рынке появляются мощные NGS-секвенаторы, хотя не все из них доступны в РФ. Среди новинок последних лет — новые продукты китайской компании MGI CycloneSEQ, интегрирующие нанопоровое секвенирование и технологию DNBSEQ, приборы Oxford Nanopore Technology и Pacific Bioscience для одномолекулярного секвенирования.
Необычностью подхода поразила платформа AXELIOS от компании Roche на основе так называемой технологии sequencing by expansion, или SBX (подробнее на PCR.NEWS). На этой платформе был установлен новый рекорд по секвенированию, попавший в Книгу рекордов Гиннесса, — геном человека за 4 часа.
Существуют отечественные приборы компании «Синтол»: «Нанофор СПС», аналог MySeq (в России их установлено уже не менее 15), ожидается отечественный аналог PacBio Rs II. Компания «Институт инженерной физики» разрабатывает приборы для нанопорового секвенирования.

Если удастся достичь целевого снижения стоимости секвенирование генома человека до 100 долларов, оно станет массово доступным, в том числе найдет новые применения в диагностике.
В случае сепсиса бактериологическая диагностика существенно уступает подходам, основанным на секвенировании. Таргетное NGS дешевле и доступнее метагеномного, но при этом оно выявляет десятки или сотни известных патогенов, а метагеномное — тысячи, в том числе неизвестные.

BGI Genomics уже выпустила панели для расшифровки инфекционных синдромов методом таргетного секвенирования, включающие сотни мишеней. Показано, что, например, при острых респираторных заболеваниях 200–350 патогенов отвечают за 95% случаев, тогда как 20-30 патогенов — за 50–70%.
Геномные исследования играют важную роль в современной онкологии.
Блестящих успехов добилась компания Grail с тестом Gallery, который выявляет около 50 видов рака путем анализа метилома крови. Чувствительность теста на I стадии рака составляет 18,8%, на II стадии — 40,4%, на III стадии — 77%, на IV — 90,1%. Несмотря на то, что на ранних стадиях чувствительность невысокая, даже внедрение такой диагностики, по мнению онкологов, улучшит ситуацию.
В финале докладчик вернулся к загадке первого слайда: следующим этапом развития молекулярной диагностики, станет протеомика. Ее потенциал огромен — в организме синтезируется более 100 тысяч белков (примерно в пять раз больше, чем кодирующих белки генов). Но до недавнего времени их выявлению препятствовала недостаточно высокая чувствительность существующих лабораторных тестов.
Новым направлением детекции белков становится NGP (Next Generation Proteomics), сказал Герман Шипулин. Некоторые примеры достижений в области протеомики плазмы можно увидеть в недавно вышедшей статье. Впечатляют успехи Somalogic, которая использует для детекции ключевых белков плазмы специально разработанные аптамеры (сомамеры), причем удваивает количество детектируемых белков по сравнению с другими платформами.
Среди других перспективных подходов — BioMark IFS Technology компании Standard Biotools (компанию купила Illumina), PEA компании Olink (куплена Thermo Fisher).
Для анализа с помощью протеомных панелей Olink нужен всего 1 мкл крови. Докладчик назвал это «сбывшимися мечтами Элизабет Холмс», печально известной основательницы компании Theranos, которая заявляла об идентификации 200 биомаркеров в 0,5 мкл крови и была арестована за мошенничество. То, что она обещала, в Olink сумели воплотить в жизнь. Еще одно важное преимущество их платформы — воспроизводимость результатов.
В заключение Герман Александрович сослался на статью «Революция в высокопроизводительной протеомике и ИИ», опубликованную в Science в 2024 году. Ее автор — Эрик Тополь из Скриппсовского института, известный специалист в области цифровой медицины. Он упоминает и третью составляющую успеха, помимо методов детекции белка и ИИ — базы данных. Британский биобанк не только собрал огромное количество данных по генотипам и фенотипам человека, но и дает возможность наблюдать участников в динамике.
Важное направление развития протеомики — это определение биологического возраста, оценка риска смерти для индивида. Эрик Тополь упоминает препринт статьи Вадима Гладышева и соавторов об органоспецифических протеомных часах старения, для создания которых использовались данные Британского биобанка и других когорт. В другом подобном исследовании было показано, что для долголетия особенно критично медленное старение мозга и иммунной системы. Знаменитый исландский проект deCODE помог выявить белки — предикторы смерти; наиболее сильным предиктором оказался белок GDF15. Для детекции белков использовалась платформа SOMAscan от Somalogic (подробнее об этой работе на PCR.NEWS). Маркеры повреждения клеток нервной системы, такие как NEFL, могут появляться в крови за годы до симптомов.
Теперь мы знаем, что старение протеома — нелинейный процесс. В работе 2019 года, где анализировались данные почти по 3000 белкам у 4000 людей в возрасте от 18 до 95 лет, было установлено, что в течение жизни человек проходит через три протеомных пика (максимальной экспрессии белков): примерно в 35, 60 и 80 лет, причем последний — самый высокий. Эти три пика формировались разными наборами белков, и два последних были обогащены белками, связанными с болезнью Альцгеймера и сердечно-сосудистыми заболеваниями. Еще одна важная задача — изучение протеома долгожителей.
Таким образом, место на следующей ступени развития молекулярной диагностики по праву должны занять протеомика и Ларри Голд, который в 2000 году основал компанию Somalogic.

Информация о докладчиках
Чуланов Владимир Петрович, д.м.н., профессор, ФГБУ «Национальный медицинский исследовательский центр фтизиопульмонологии и инфекционных заболеваний» Минздрава России, г. Москва
Шипулин Герман Александрович, ФГБУ «Центр стратегического планирования и управления медико-биологическими рисками здоровью» ФМБА России, г.Москва
Продолжение:


 Меню
Меню





 Все темы
Все темы



 0
0










