Вакцины против коронавируса: ответы на очень часто задаваемые вопросы
Когда начнут вакцинировать против коронавируса? Какие вакцины уже на подходе? Какая из них самая хорошая, и почему? Ответы на эти вопросы мы постарались сделать простыми, потому что они возникают у широкого круга читателей. Но они будут интересны и специалистам, поскольку им сейчас постоянно приходится отвечать на те же вопросы.
Для ответов мы использовали информацию о вакцинах, которую PCR.news собирает с февраля, а также обзор, на прошлой неделе опубликованный в Nature. Его автор — Флориан Краммер из Медицинской школы Айкана в Маунт-Синай, специалист по респираторным вирусным инфекциям, руководитель той самой лаборатории, где был разработан один из первых тестов на антитела к коронавирусу. (Подробнее на PCR.news о сотрудничестве Маунт-Синай с российскими учеными.)
Почему до сих пор нет вакцин от других коронавирусов человека?
Потому что известные нам до сих пор коронавирусы человека или почти безвредны, или слишком агрессивны. Против сезонных коронавирусов — двух альфакоронавирусов (NL63, 229E) и двух бетакоронавирусов (HKU1, OC43) разрабатывать вакцину нет необходимости. Во-первых, они вызывают обычную простуду, которая «быстрее пройдет сама». Во-вторых, даже если удастся создать квадривалентную вакцину против всех четырех коронавирусов, она будет предотвращать лишь малую часть всех случаев простуды — большинство их вызывается другими вирусами.
Кстати, предполагается, что все эти четыре вируса имеют зоонозное происхождение, то есть перешли к человеку от животных. Согласно одной из гипотез, OC43 был причиной так называемого русского гриппа 1890 года: как раз в то десятилетие, по данным геномного анализа, этот коронавирус человека отделился от родственных ему бычьих коронавирусов.
Вакцины против возбудителя тяжелого острого респираторного синдрома SARS-CoV-1 в свое время прошли преклинические исследования, две достигли первой фазы клинических испытаний. Но дальше дело не пошло из-за нехватки больных: после 2004 года новых случаев не отмечено, эта болезнь была слишком тяжелой, чтобы распространиться широко. Вакцины против ближневосточного респираторного синдрома MERS активно разрабатываются, и это помогло в создании некоторых вакцин против нового коронавируса. Например, Moderna оказалась среди лидеров гонки, потому что у нее была мРНК вакцина против MERS, прошедшая преклинические исследования. Но MERS известен лишь с 2012 года, а создание вакцины — дело небыстрое.
Какие этапы включает разработка вакцины?
«В мирное время» на создание вакцины может уйти около 15 лет. Несколько лет занимает разработка прототипа, еще несколько — преклинические исследования (на животных), потом около двух лет — на фазу 1 клинических исследований (КИ) с участием десятков людей. В случае положительного результата — столько же на фазу 2, где добровольцев уже сотни. И только затем — рискованная и дорогостоящая фаза 3, а после нее еще процедура лицензирования, которая также может занять год или более.
Сейчас разработка происходит на сверхсветовой скорости. Начальные фазы сокращены за счет использования уже существующих вакцин, модифицированных «под COVID»; КИ той же вакцины mRNA-1273 компании Moderna стартовали в марте 2020 года. Фазу 3 могли начать до окончания совмещенной фазы 1/2, сразу, как только появлялись обнадеживающие промежуточные результаты. И еще до результатов фазы 3 разработчики на свой страх и риск налаживают производство. По сути, время покупают за деньги: если результаты внезапно перестанут обнадеживать, огромные вложения в фазу 3 и производство пропадут.
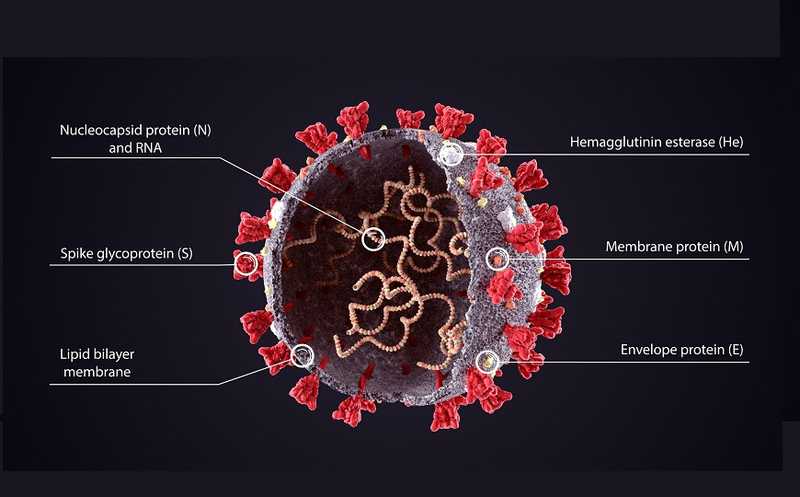
Исследования других коронавирусов и SARS-CoV-2 в первые месяцы пандемии позволили сделать вывод, что хорошая мишень для вакцины — S-белок коронавируса, тот, что образует характерные шипы «короны» и связывается с рецептором человеческой клетки. В самых ранних, еще зимних исследованиях было показано, что антитела к S-белку могут нейтрализовать вирус и что иммунная реакция на SARS-CoV-2 в целом такая же, как и на другие респираторные вирусы. Эксперименты на обезьянах продемонстрировали, что присутствие нейтрализующих антител коррелирует с защитой и что переболевшие животные не заражаются снова. Не так давно это подтвердилось в «естественном эксперименте» на людях, во время вспышки COVID-19 на рыболовном судне. Все эти и другие факты говорили о том, что новый коронавирус с точки зрения иммунологии ничего особенного собой не представляет — это не новый ВИЧ, и вакцину против него сделать можно.
Какие вакцины против коронавируса у нас есть?
Сейчас, на конец сентября, согласно трекеру ВОЗ, 40 вакцин проходят клинические исследования. Десять из них дошли до фазы 3, в том числе две новых за последнюю неделю — Janssen, дочерняя компания Johnson&Johnson, и Novavax (здесь и далее будем называть вакцины по компании-производителю, так как рабочие и коммерческие названия препаратов могут меняться). Это десятки тысяч людей и — наконец-то — проверка не только безопасности, но и эффективности, то есть сравнение доли зараженных в группе вакцинированных и в группе плацебо. Еще 151 вакцина проходит преклинические испытания.
Для создания вакцины против COVID-19 используются как традиционные подходы (инактивированный или ослабленный вирус, рекомбинантные белки, векторные вакцины), так и абсолютно новые, которые в лучшем случае были испытаны на небольшом количестве людей, но до 2020 года не внедрялись в клиническую практику (ДНК и РНК-вакцины). У каждого из подходов есть свои преимущества и недостатки.
Инактивированные вакцины содержат вирус, выращенный в культуре клеток и затем инактивированный химическим веществом. Вводится такая вакцина обычно внутримышечно, с добавлением адъюванта. Технически все просто, однако сложно с точки зрения биобезопасности: выращивать жизнеспособный SARS-CoV-2 разрешено не каждому производителю. Выгода этого подхода в том, что иммунная система «видит» не один белок вируса, а все. Примеры: китайские вакцины Sinovac, Sinopharm, российская — Центра Чумакова, недавно начавшая клинические исследования.
Живые аттенуированные вакцины содержат ослабленную версию вируса, не вызывающую болезнь. Чтобы ослабить вирус, его выращивают в неблагоприятных условиях — при пониженной температуре или в культуре клеток другого вида — либо вводят направленные генетические модификации в его геном. Получение такого вируса требует времени, кроме того, всегда остаются сомнения по поводу его безопасности. Важные плюсы —возможность вводить интраназально и получать иммунный ответ слизистой оболочки (потом разберем, почему это важно), способность вируса реплицироваться в организме. На поздних стадиях КИ таких вакцин пока нет.
Вакцины, содержащие рекомбинантный белок. Это может быть целый S-белок (возможно, с модификациями, повышающими стойкость в организме человека и иммуногенность), или его рецептор-связывающий домен, или же включающие S-белок вирусоподобные частицы. Белок производят в клетках насекомых, млекопитающих, растений или дрожжей, маленький рецептор-связывающий домен можно экспрессировать даже в кишечной палочке. Следовательно, выращивать опасный жизнеспособный вирус для производства вакцины не придется. Но с получением вирусных белков есть свои сложности: полноразмерный белок труднее экспрессировать, а вакцина на основе фрагмента может оказаться бесполезной против штаммов, у которых этот фрагмент изменился в результате мутации, если такие штаммы появятся. Пример вакцины с рекомбинантным белком — Novavax, и как мы увидим далее, характеристики этой вакцины очень хорошие.
Мощно представлены среди финалистов гонки вакцины на основе нереплицирующихся векторов. Ген вирусного белка, как правило, того же S-белка, встраивается в геном безвредного вируса, который, собственно, и называется «вектором». Вирус проникает в клетку и запускает в ней синтез вирусного белка, но размножаться и инфицировать другие клетки он не способен.
У всех на слуху аденовирусы (AdV) 5 и 26, также используются модифицированный поксвирус Анкара, вирусы гриппа и парагриппа, аденоассоциированный вирус и вирус Сендай. Плюсы — жизнеспособный коронавирус тоже не понадобится, производство для многих платформ уже отлажено, известно, что они дают хороший иммунный ответ. Минус в том, что у вакцинированного человека может быть иммунитет к вирусу, использованному в качестве вектора. Аденовирусные инфекции, относящиеся к группе ОРВИ, широко распространены в популяции. Поэтому вакцина AstraZeneca, разработанная в Оксфордском университете, содержит аденовирус шимпанзе, а вакцина ReiThera, которая проходит фазу 1, — аденовирус гориллы: с этими вирусами мало кто из европейцев встречался. Человеческие аденовирусы решили использовать Janssen (AdV26), CanSino (AdV5). Российская вакцина Центра Гамалеи «Спутник V», она же Гам-Ковид-Вак, содержит векторы на основе двух разных аденовирусов: первая доза — Ad5, вторая — Ad26, оба несут ген S-белка.
Вакцины на основе реплицирующихся векторов. Обычно это штаммы вирусов, используемые для вакцинации, например, против кори или гриппа. Плюсы те же, что у живых аттенуированных вирусов: возможность вводить вакцину интраназально, более сильный иммунный ответ за счет размножения вируса.
Чтобы сделать векторную вакцину более контролируемой, вирусный вектор можно инактивировать. Такие инактивированные вирусные векторы не могут размножаться даже в организме человека со сниженным иммунитетом, и дозу антигена будет легко стандартизировать. Вакцины этих двух групп пока в разработке или на ранних стадиях КИ.
ДНК-вакцины — плазмиды (кольцевые молекулы ДНК) со встроенным геном вируса, способным экспрессироваться в человеческих клетках. Хороши тем, что плазмиды можно наработать в кишечной палочке, а также высокой стабильностью — эти моменты сильно упрощают производство и транспортировку. Минус — невысокая иммуногенность известных вариантов. Кроме того, чтобы ДНК-вакцина попала в клетки, мало сделать укол — необходимо провести электропорацию, то есть с помощью электрического поля создать поры в мембране клетки. Таким образом, для введения ДНК-вакцины нужен специальный прибор. Очевидно, что это ограничит их применение в мировом масштабе.
РНК-вакцины — самая новая из платформ, и весьма успешная. Среди лидеров на данный момент две РНК-вакцины, компаний Pfizer и Moderna. Молекулы РНК, кодирующие вирусный белок, обычно в составе липидных наночастиц, вводятся внутримышечно, РНК проникает в клетки и экспрессирует белок вируса. РНК- вакцины может производиться полностью in vitro, для этого не нужны даже культуры клеток. Однако хранить их необходимо в замороженном виде, вариант с лиофилизацией невозможен. Это затрудняет хранение и транспортировку. Кроме того, как врачам, так и производителям, и дистрибьюторам внушает сомнения новизна мРНК-вакцин.
Как определяют, хорошая вакцина или плохая?
Многими способами. Измеряют в сыворотке крови вакцинированного количество антител, специфичных к вирусному белку. Или количество нейтрализующих антител, то есть таких, которые мешают вирусу инфицировать клетки (не всякое антитело к вирусному белку обладает такой способностью). Второй показатель измерить несколько сложнее, но он точнее характеризует эффективность вакцины. Можно также сравнивать титр нейтрализующих антител у вакцинированных и у переболевших, причем желательно, чтобы у вакцинированных он был выше.
Также проверяют, реагируют ли Т-лимфоциты в крови пациента на вирусный белок. После вакцинирования должна появиться популяция Т-клеток, которая при контакте с вирусом начинает размножаться; более полную информацию дает подсчет CD4+ Т-лимфоцитов (Т-хелперов) и CD8+ (Т-киллеров).
Кроме того, важна динамика концентраций антител: как они растут после вакцинации, как долго остаются постоянными и с какой скоростью убывают. Важно понять, насколько отличаются иммунные ответы у молодых и пожилых пациентов. Т
Было бы идеально проверить напрямую, препятствует ли вакцина вирусной инфекции, однако по этическим соображениям такие исследования проводят только на животных. (В Лондоне группа энтузиастов собирается начать исследования на людях, в которых вакцинированных и группу контроля будут целенаправленно заражать коронавирусом, но это будет лишь в следующем году.) Обычно в клинических испытаниях набирают большие группы вакцинированных и плацебо и сравнивают число заразившихся в той и другой.
Наконец, необходимо оценить побочные эффекты и осложнения.
Какая вакцина из тех, которые дошли до фазы 3, лучше?
Забудем о себестоимости, удобстве производства и транспортировки, поговорим только об эффективности и безопасности. Но даже и это — непростой вопрос. Протоколы КИ у каждой вакцины свои: исследователи использовали разные дозы вакцины, группы различного размера, измеряли количество нейтрализующих антител разными способами, и так далее. Наконец, не для всех вакцин доступны полные данные, например, для Гам-Ковид-Вак (пока?) не опубликованы результаты, полученные на животных; о том, что они прошли успешно, известно только из интервью разработчиков.
Вот десять вакцин, достигших фазы 3 КИ.
Три инактивированных, все из Китая: Sinovac, две вакцины от Sinopharm, совместно с Уханьским и Пекинским институтами биопродуктов.
Четыре на основе аденовирусных векторов: Оксфорд/AstraZeneca (аденовирус шимпанзе), CanSino (Ad5), Janssen, дочерняя компания Johnson&Johnson (Ad26), и вакцина НИЦЭМ им. Н.Ф.Гамалеи (Ad26 + Ad5).
Две вакцины на основе мРНК — Moderna/NIAID и BioNTech/Fosun/Pfizer (в фазе 1/2 участвовало два варианта вакцины, BNT162b1 и BNT162b).
И, наконец, одна субъединичная вакцина от компании Novavax, содержащая наночастицы с полноразмерным S-белком коронавируса.
Граждане РФ участвуют в клинических испытаниях трех из них: помимо «Спутника V», это AstraZeneca (сто человек без плацебо-контроля, возобновлено ли КИ после приостановки, вызванной болезнью британской участницы, пока неясно) и китайская вакцина CanSino, уже лицензированная для использования в армии КНР.
Данные по испытаниям на макаках, которых вакцинировали и затем инфицировали SARS-CoV-2, имеются, например, для Sinovac, одной из вакцин Sinopharm, AstraZeneca, Janssen, Moderna, Novavax. Повышением дозы или переходом от однократной схемы введения к двукратной во всех случаях удалось добиться полной защиты нижних дыхательных путей обезьян: вирусная РНК в них не выявлялась. Однако полностью очистить от вируса верхние дыхательные пути не смогла ни одна вакцина, за исключением Janssen и Novavax. Это важный момент: защита легких от вируса спасает от тяжелой формы заболевания, но только отсутствие вируса в верхних респираторных путях гарантирует, что человек и сам не заболеет, и не будет распространять вирус.
В фазе 1/2 клинических исследований всем, по-видимому, удалось получить иммунный ответ, как гуморальный, так и клеточный, опять же варьируя дозы и схему введения. Например, у AstraZeneca большая часть добровольцев получила одну дозу вакцины, и титр антител был довольно низким. После второй дозы он вырос, но ее получили в рамках фазы 1/2 всего десять человек. Результат в итоге оказался приемлемым, но, возможно, из-за завышенных ожиданий по поводу этой вакцины после публикации результатов курс акций AstraZeneca несколько снизился.
Эксперты подчеркивают, что показатели иммуногенности, полученные в различных экспериментах, сложно сравнивать напрямую, и что было бы полезно сравнить разные вакцины в одинаковых условиях и одинаковыми методами. Даже в одном исследовании вакцины AstraZeneca титры нейтрализующих антител, измеренные разными методами, различались почти на порядок.
Тем не менее Флориан Краммер следующим образом оценил характеристики вакцин: по иммуногенности, если оценивать ее по титрам нейтрализующих антител, инактивированная вакцина Sinovac и вакцина AdV5 CanSino будут в нижней части списка, вакцина AstraZeneca и обе мРНК-вакцины — в середине, и, наконец, Novavax с рекомбинантной субъединичной вакциной возглавляет хит-парад. При всех сложностях интерпретации данных по нейтрализующим антителам видно, что вакцина Novavax лидирует с большим отрывом: у других цифры трехзначные, у нее — четырехзначная. Такой результат, по-видимому, достигнут благодаря запатентованному адъюванту Matrix-M: без него титры нейтрализующих антител куда скромнее.
С точки зрения переносимости лучше всех показали себя инактивированные вакцины и рекомбинантная белковая вакцина Novavax, за ними следуют мРНК-вакцины, которые демонстрируют повышенную реактогенность после второй вакцинации, а наибольшее число побочных эффектов дают вакцины с аденовирусными векторами. У инактивированной вакцины Sinovac отличный профиль безопасности, обе дозы дали эффект, сравнимый с плацебо. У AstraZeneca на слабость и усталость жаловалось более 70% участников, на головную боль — более 60%, то есть показатели безопасности были хуже, чем у лицензированной вакцины против менингита, которую использовали для сравнения. А вот Novavax оказывается среди лидеров по обоим показателям.
Вакцина центра Гамалеи по иммуногенности, возможно, опережает CanSino за счет двукратного введения разных векторов (китайская вакцина вводится однократно) и сравнима с ней по побочным эффектам. Детальное сравнение провести сложно ввиду нехватки информации как о нашей вакцине, так и о китайской.
Какие еще проблемы нужно решить?
Чтобы остановить пандемию, потребуется огромное количество доз вакцины. В случае двукратного введения — до 16 миллиардов на все человечество. (Варианты с одной дозой среди лидеров пока рассматривают Janssen и CanSino.) Кроме того, пока неизвестно, насколько длительным окажется иммунитет и как скоро может понадобиться повторная вакцинация. Неясно, удастся ли масштабировать производство новых вакцин. Может возникнуть нехватка не только компонентов вакцины, но и шприцов, и стеклянных ампул.
Все десять рассмотренных вакцин вводятся внутримышечно, и это не очень хорошо. Естественная инфекция индуцирует как появление антител слизистой оболочки (секреторных IgA), так и системный иммунный ответ (IgG в крови). Верхние дыхательные пути в основном защищены секреторными IgA, нижние дыхательные пути — IgG. Вакцины, вводимые внутримышечно, индуцируют главным образом IgG и слабее защищают верхние дыхательные пути, что и было показано в экспериментах на животных. Минус, как уже говорилось, в том, что вакцинированный, хотя не заболеет тяжело, может быть распространителем инфекции. С этой точки зрения были бы предпочтительнее вакцины, которые вводят интраназально — естественным для респираторной инфекции путем.
Плохо изученной остается реакция на вакцину в старших возрастных группах: целенаправленно ее исследовали, по-видимому, только Sinovac и Pfizer. Ожидаемо, у людей старше 55 иммунный ответ слабее. Возможно, им следует выбирать реактогенные вакцины, такие как мРНК или аденовирусные, вызывающие более сильный интерфероновый/антивирусный ответы, предполагает Краммер (то есть кажущийся минус в данном случае будет плюсом). Другой вариант — назначать им более высокие дозы либо повторную иммунизацию. Также пока нет данных про иммунный ответ у детей.
А что с тяжелыми осложнениями?
Многих волнует антителозависимое усиление инфекции, которое может произойти после вакцинации. АЗУИ — редкое явление, когда антитело, связываясь с вирусом, способствует не его уничтожению, а его проникновению в иммунные клетки. Такое случилось с вакциной Sanofi Paster «Денгваксия». против лихорадки денге и привело к катастрофическому падению доверия к вакцинации на Филлипинах.
Пока нет оснований считать, что АЗУИ может иметь место при вакцинации против COVID-19, отмечает Флориан Краммер. Признаки АЗУИ наблюдали для других коронавирусов исключительно в экспериментальных условиях, in vitro и на животных: при исследованиях вакцины против коронавируса кошек, вакцин против SARS-CoV-1 и МЕRS-CoV. Однако даже на животных моделях в настоящее время нет доказательств АЗУИ применительно к вакцинам против SARS-CoV-2. Тем не менее, первостепенное значение имеет мониторинг вакцинированных, особенно после того, как титры начинают снижаться. Если тяжелое осложнение произойдет во время исследований одной из вакцин, это плохо скажется на всех.
Не до конца прояснилась ситуация с «серьезными неврологическими симптомами, соответствующими поперечному миелиту» у участницы КИ вакцины AstraZeneca в Великобритании; неизвестно даже, каков окончательный диагноз. Во многих случаях причину развития поперечного миелита установить не удается (и это значит, что доказать «непричастность» вакцины будет трудно). Но аутоиммунная реакция, вызванная вакциной, теоретически может быть причиной. Наиболее масштабные КИ, в Америке, остановлены, регулирующие органы США призывают провести расследование болезни участницы.
Так когда вакцина поступит на рынок? И какая будет первой?
До ноября, как хотят политики многих стран, — вряд ли. Однако Флориан Краммер допускает, что это может произойти до конца 2020 года. Как следует из опубликованных протоколов КИ Moderna, Pfizer и AstraZeneca, выводы о защитных свойствах вакцины можно сделать после того, как будут инфицированы коронавирусом примерно полторы сотни участников из групп вакцинации и плацебо. Но, например, Moderna планирует делать промежуточные оценки по достижении 35% и 70% от этого числа заболевших, и предполагает, что это может произойти примерно через 5 и 8 месяцев после вакцинации первых участников в июле, а окончательные итоги удастся подвести через 10 месяцев.
Дальше всего пока продвинулись AstraZeneca, Moderna и Pfizer, и, если не случится неожиданностей во время фазы 3, видимо, кто-то из них будет лицензирован первым. (Регистрацию российской вакцины до третьей фазы не считаем.) Однако, возможно, позднее их заменят вакцины, которые покажут аналогичную эффективность, но более приемлемую реактогенность. Кроме того, по ряду причин маловероятно, что небольшое количество вакцин распространится на весь мир. Видимо, вакцины, которые производятся и разрабатываются в Китае, Индии и других странах, будут играть важную роль в удовлетворении глобального спроса.
Источник
Florian Krammer. // SARS-CoV-2 vaccines in development. // Nature, 2020, DOI: 10.1038/s41586-020-2798-3


 Меню
Меню





 Все темы
Все темы




 0
0