Итоги-2025. CRISPR-терапия для Кей-Джея, череп денисовца и антипрививочник во главе минздрава
«Не самый любимый мой год» — так озаглавил свою колонку главный редактор Science Холден Торп. И наш не самый любимый. Меньше, чем в другие годы, было научных новостей, вызывающих восторг, и были новости печальные. Однако важные тренды продолжают развиваться, и хороших новостей в будущем году мы обязательно дождемся.

Успех персонализированной CRISPR-терапии
Персонализированная CRISPR-терапия облегчила симптомы смертельно опасного генетического заболевания. — редкого наследственного дефицита карбамоилфосфатсинтетазы 1 (CPS1) — у маленького ребенка. Это первый описанный в медицинской литературе случай персонализированного применения CRISPR.
CPS1 катализирует первую стадию цикла мочевины, а при нарушении работы этого фермента печень неспособна полностью утилизировать побочные продукты метаболизма азотсодержащих соединений. Из-за этого в организме накапливается аммиак, что приводит к повреждениям мозга и печени, может вызвать кому или смерть. Пациентам показана трансплантация печени, в ожидании которой они вынуждены придерживаться низкобелковой диеты и принимать лекарства, снижающие уровень аммиака. До пересадки доживает лишь около половины младенцев с тяжелым дефицитом CPS1.
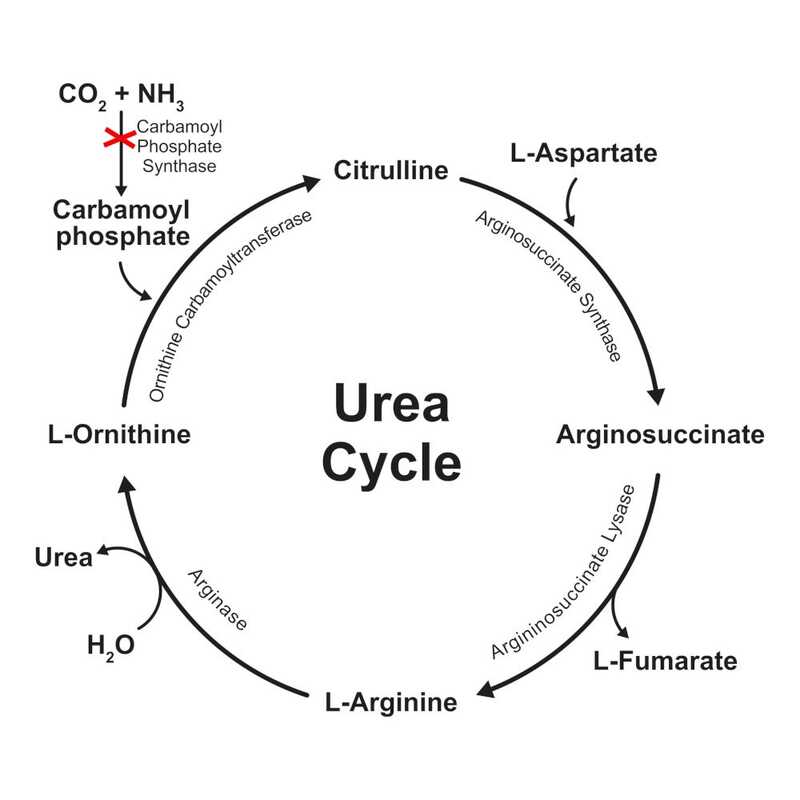
У мальчика по имени Кайл Малдун, которого также называют Кей-Джей (KJ), симптомы заболевания проявились сразу после рождения. Таргетное секвенирование выявило преждевременные стоп-кодоны как в отцовском, так и в материнском аллеле CPS1, приводящие к появлению нефункционального укороченного белка. Ребенок мог получить трансплантат печени через несколько месяцев, но из-за высоких рисков для младенца семье предложили альтернативу — генную терапию.
За первые два месяца жизни пациента исследователи создали редактирующую конструкцию на основе CRISPR-Cas, нацеленную на отцовский вариант. После испытания на клетках пациента и животных моделях было получено одобрение на лечение ребенка. Этот период занял около полугода.
Всего мальчик получил три дозы терапевтической конструкции, первую — самую низкую — на седьмом месяце жизни. Уже после первой дозы появились улучшения, он смог получать больше белка с пищей, а после второй дозы препарата ему снизили дозировку препаратов, связывающих и выводящих аммиак.
Статья, в которой задокументирован этот медицинский случай, была опубликована в The New England Journal of Medicine в мае этого года. На момент публикации ребенку было 10 месяцев, и его состояние продолжало улучшаться. Маленький пациент легко перенес простуду и желудочно-кишечную инфекцию, при том, что дети с дефицитом CPS1 часто умирают от таких инфекций в период ожидания трансплантации.
Среди авторов публикации Дэвид Лю из Института Бродов (под его руководством были созданы первые редакторы оснований). О настоящем излечении говорить пока рано, однако терапия выглядит безопасной и облегчает состояние больного. Врачи надеются, что, возможно, пересадки печени удастся избежать вовсе, а вместо этого мальчик получит дополнительные дозы терапевтического редактора оснований по мере взросления.
Персонализированные вакцины против рака
Терапевтические вакцины против рака, как персонализированные, так и серийные, привлекают много внимания, и мы детально рассмотрели эту тему. Персонализированные вакцины производятся для конкретного пациента и вызывают иммунный ответ именно на неоантигены его опухоли.
В 2024 году была опубликованы результаты фазы 2 КИ вакцины V940 (другие названия — аутоген интисмеран и mRNA-4157) компаний Merck и Moderna. мРНК в составе вакцины кодирует до 34 неоантигенов. У пациентов с хирургически удаленной меланомой, которые получали V940 в комбинации с иммунотерапией, риск рецидива или смерти был меньше на 49% в сравнении с группой, получавшей только иммунотерапию. Ожидаются результаты фазы 3. Персонализированные вакцины под названием V940 проходят КИ и при других диагнозах (например, немелкоклеточный рак легкого
У Онкологического центра Даны—Фарбера (США) есть в разработке пептидные персонализированные вакцины против меланомы и светлоклеточного рака почки (подробнее на PCR.NEWS.)
В этом году разрешены к применению и две российские персонализированные онковакцины: мРНК-вакцина Неоонковак и пептидная вакцина Онкопепт.
Вакцина Неоонковак разработана в Московском научно-исследовательском онкологическом институте им. П.А. Герцена (филиал НМИЦ радиологии), НИЦ эпидемиологии и микробиологии им. Н.Ф. Гамалеи и НМИЦ онкологии им. Н.Н. Блохина. Она предназначена для терапии неоперабельной или метастатической меланомы в комбинации с ингибиторами контрольных точек иммунного ответа. В дальнейшем Неоонковак может применяться также в качестве адъювантной терапии после хирургического лечения взрослых с меланомой кожи IIB–IV стадии.
Пептидную вакцину Онкопепт разработали в ФНКЦ физико-химической медицины им. Ю.М. Лопухина ФМБА России. Вакцина предназначена для лечения метастатического колоректального рака у пациентов, которые получили две и более линий системной противоопухолевой терапии, в монотерапии или в комбинации с ингибиторами PD-1.
Индивидуальные биотехнологические лекарственные препараты (иБТЛП) в России изготавливаются и реализуются в соответствии с постановлением правительства РФ №213 от 24 февраля 2025 года. Согласно этому постановлению, медицинские организации должны получать разрешение на изготовление и применение таких препаратов.
Разработчики подчеркивают, что онковакцины должны применяться в комбинации с другими видами терапии, а решение об их назначении принимается индивидуально в каждом случае.
 text Credit: 123rf.com
text Credit: 123rf.com
Новые рекорды ксенотрансплантации
Многие надеются, что ксенотрансплантация поможет решить проблему нехватки донорских органов. Эта область медицины получила в 2025 году сильный толчок к развитию.
В январе 2025 года был опубликован подробный отчет о состоянии пациента, получившего в 2023 году генетически модифицированное свиное сердце и скончавшегося на 60-й день. Авторы отчета обсуждали вероятные причины неудачи, но в целом были настроены оптимистично.
В апреле 2025 года удалили свиную почку женщине, которая прожила с ней четыре месяца и девять дней. Свинью-донора предоставила компания Revivicor из Блэксбурга, штат Вирджиния (подразделение United Therapeutics). У этих свиней отредактировано 10 генов.
Много месяцев PCR.NEWS следил за судьбой Тима Эндрюса, которому была пересажена почка свиньи от eGenesis с 69 модифицированными генами. Почка функционировала почти девять месяцев, но в октябре все же отказала. Мужчину снова перевели на диализ, и, возможно, ему будет трансплантирован орган от донора-человека. В декабре появилось сообщение, что почка свиньи от китайской компании Clonorgan, пересаженная женщине, тоже была удалена и проработала всего на 10 дней меньше, чем у Тима Эндрюса.
В марте была опубликована статья о пересадке печени генномодифицированной свиньи от Clonorgan — пока что пациенту, перенесшему смерть мозга. Базовые показатели работы печени сохранялись в пределах нормы в течение 10 дней, потом эксперимент прервали. Еще девять дней в организме пациента со смертью мозга функционировало свиное легкое (тоже от Clonorgan).
Китайские исследователи пересаживали печень и живому реципиенту. Это была временная мера, пока не восстановится собственный орган пациента после операции. Однако вскоре орган пришлось удалить, а на 171-й день после операции пациент скончался. У свиньи-донора были модифицированы 10 генов. Специалисты также отслеживали наличие патогенов у свиньи и у реципиента после трансплантации.
Специалисты сходятся во мнении, что свиньям-донорам необходимы дополнительные, еще не определенные генетические модификации для увеличения времени выживания пересаженных органов. Также разрабатывают более безопасные и эффективные препараты для подавления отторжения. А некоторые научные группы испытывают альтернативные стратегии для повышения иммунной толерантности — например, пересадку тимуса свиньи вместе с ее почкой.
 Credit: 123rf.com
Credit: 123rf.com
«Молекулярная диагностика 2025»
Наше главное событие года в молекулярной диагностике и молекулярной медицине — МД 2025. Что бы ни происходило в мире, специалисты работают, общаются и планируют новые проекты.
На открытии конференции говорили о настоящем и будущем MDx: как прошел третий год расширенного неонатального скрининга в РФ, что с инфекционными болезнями в мире, и если секвенирование не высшая и последняя стадия молекулярной диагностики, то что придет за ним?
Несколько секций было посвящено молекулярным методам в онкологии. В чем разница между мутациями в BRCA1 и BRCA2 и что может сегодня жидкостная биопсия? Как на практике обычно выявляют редкие наследственные опухолевые синдромы и где в Москве секвенируют геномы пациентов с этими синдромами? Всегда ли необходимо в этих случаях полногеномное секвенирование? И, как всегда, секция о ВПЧ-ассоциированных онкозаболеваниях — случай, когда диагностика и вакцинация могут особенно много.
Глобальной проблемой остается вирус иммунодефицита человека. На этой секции обсуждали, в частности, как научное сообщество пытается «обогнать» изменчивость вируса, что нужно, чтобы своевременно выявить ВИЧ-инфекцию у младенца и как продвигается разработка новых препаратов против ВИЧ.
Неврологические заболевания тяжело поддаются лечению и диагностике, но тем важнее работы, которые ведутся в этом направлении. Как оптимизировать выявление наследственных атаксий и неклассических форм БАС, какие проблемы помогут решить органоиды из индуцированных плюрипотентных стволовых клеток пациента и не только это — на секции по неврологии.
А еще обсуждались искусственный интеллект, палеогенетика (да, и про скифов было), старение и долголетие и многое другое.
 Фото: Андрей Константинов
Фото: Андрей Константинов
Золифлодацин — перспективный антибиотик против гонореи — одобрен FDA
Последний месяц года принес новость об успехе в борьбе с антибиотикорезистентностью. Антибиотик золифлодацин с уникальным механизмом действия прошел фазу 3 клинических исследований и получил одобрение FDA в качестве однократного перорального препарата для лечения гонореи — одной из самых распространенных инфекций, передаваемых половым путем.
Гонореей ежегодно заражаются свыше 82 млн человек. Для лечения как правило, применяют цефтриаксон и азитромицин, однако Neisseria gonorrhoeae, возбудитель гонореи, все чаще демонстрирует к ним устойчивость. Одобренной вакцины для против гонококка не существует, а нелеченная гонорея может вызывать серьезные проблемы, в ряде случаев распространяясь в системный кровоток, поражая суставы или приводя к бесплодию.
Золифлодацин — ингибитор бактериальной ДНК-гиразы. От других ингибиторов, фторхинолонов, он принципиально отличается мишенью — золифлодацин нацелен на субъединицу GyrB, тогда как фторхинолоны — на GyrA и ParC. Это позволяет обойти резистентность к другим препаратам.
В фазе 3 КИ с почти тысячей участников золифлодацин не уступал по эффективности классической терапии первой линии (сочетанию цефтриаксона и азитромицина), а также был эффективен против резистентных штаммов гонококка. Около 90% пациентов с неосложненной урогенитальной гонореей выздоровели после приема нового препарата.
Важное преимущество золифлодацина состоит в том, что это пероральный препарат для однократного приема — не нужны инъекции или длительные курсы, которые снижают приверженность пациентов лечению. Одобрение FDA — серьезный шаг к внедрению золифлодацина в клиническую практику, которое может не только упростить лечение гонореи, но и снизить риски дальнейшего распространения резистентности, в том числе к такому ключевому антибиотику, как цефтриаксон.
 Credit: 123rf.com
Credit: 123rf.com
Администрация нового президента США реформирует биологию и медицину
Победа Дональда Трампа на выборах негативно повлияла на медико-биологические науки в США, а учитывая их лидирующее положение в этой области — и во всем мире. Президентский указ о выходе из ВОЗ, заморозка помощи иностранным государствам в рамках программ USAID (включая борьбу с ВИЧ и малярией), сокращения штатов в Министерстве здравоохранения и социальных служб США, сокращение грантов NIH, затруднение доступа к сайтам CDC и FDA в ходе борьбы с «незаконной политикой DEI» — то, что произошло уже в первые месяцы года. Многое получило продолжение, например, «сделки» администрации президента с университетами и приостановка gain-of-function исследований вирусов, которые администрация президента считает опасными. С сайта Белого дома удалена страница с ресурсами по COVID-19 и заменена заявлением, что пандемия возникла в результате утечки из лаборатории и модификаций вируса..
Сенат США 13 февраля утвердил на посту главы Министерства здравоохранения и социальных служб Роберта Кеннеди-младшего. Отделениями министерства являются в том числе Центры по контролю и профилактике заболеваний (CDC), Управление по контролю продуктов и лекарств (FDA), Национальные институты здравоохранения (NIH) — крупнейший в мире спонсор биомедицинских исследований. При этом Роберт Кеннеди-младший известен негативным отношением к вакцинации.
В марте министерство здравоохранения обратилось к CDC с просьбой о проведении масштабного исследования, посвященного связи между вакцинами и аутизмом. (Научных подтверждений существования такой связи нет.) Из-за давления главы министерства Питер Маркс, директор Центра оценки и исследований биологических препаратов FDA (CBER), отвечающего в том числе за безопасность и эффективность вакцин, подал заявление об отставке, как и ряд других руководителей. В августе Роберт Кеннеди-младший потребовал у научного журнала отозвать статью об исследовании, не выявившем вред вакцин. Есть и хорошие новости: статья не отозвана.
Также в этом году Управление передовых биомедицинских исследований и разработок (Biomedical Advanced Research and Development Authority, BARDA) минздрава США объявило о прекращении инвестиций в разработку 22 мРНК-вакцин на общую сумму $500 млн. Опять-таки не существует научных подтверждений мнения Роберта Кеннеди-младшего о неэффективности мРНК-вакцин против COVID-19 и гриппа.
Ситуацию с предотвратимыми инфекционными заболеваниями в США невозможно назвать благоприятной. Растет заболеваемость корью и коклюшем. Например, в штате Орегон число случаев коклюша, выявленных в течение года, к середине декабря достигло 1475 — подобных показателей не наблюдалось с 1950-х годов.
 Credit: 123rf.com
Credit: 123rf.com
Генная терапия болезни Гентингтона: большие надежды и разочарования
Болезнь Гентингтона неизлечима, однако ведется разработка генной терапии, которая могла бы замедлить течение болезни или остановить ее развитие. В 2025 году компания uniQure опубликовала первые результаты фазы 1/2 клинических испытаний препарата AMT-130, которые дали надежду пациентам и их семьям. (Подробнее на PCR.NEWS.)
AMT-130 содержит ген, кодирующий микроРНК. Вектором служит модифицированный и безопасный аденоассоциированный вирус, а микроРНК распознает, связывает и снижает уровень белка гентингтина человека, как мутантного, так и нормального. Чтобы избежать побочных реакций, вектор вводят очень медленно, через микрокатетер, в два участка мозга. Эта сложная процедура занимает от 12 до 20 часов, но проводится только один раз и хорошо переносится.
Препарат получили четыре когорты пациентов, и результаты были впечатляющими. Высокие дозы AMT-130 статистически значимо замедляли прогрессирование заболевания на 75% по шкале cUHDRS (снижение на 0,38 от исходного уровня у получивших терапию пациентов по сравнению со снижением на 1,52 у внешних контролей). Препарат также замедлял прогрессирование заболевания на 60% при измерении общего функционального потенциала (Total Functional Capacity, TFC).
Хорошие результаты были показаны и при измерении двигательной и когнитивной функций, включая тест символьно-цифровых модальностей (SDMT), тест Струпа на чтение слов (SWRT) и общую двигательную оценку (TMS). Прогрессирование заболевания замедлилось на 88% по оценке SDMT (p=0,057), на 113% по оценке SWRT (p=0,0021), на 59% по оценке TMS (p=0,1741).
Компания uniQure планировала подать заявление, чтобы получить лицензию на производство биологических препаратов (Biologics Licensing Application) FDA в начале 2026 года. Однако в ноябре 2025 года компания выпустила пресс-релиз, в котором сообщила, что FDA, скорее всего, не примет полученные результаты как основание для выдачи лицензии (результаты встречи, на которой принималось решение, на тот момент еще не сообщили компании). Что же пошло не так?
Согласно пресс-релизу, FDA возражает против использования внешней контрольной группы, хотя uniQure настаивает, что такой протокол клинических испытаний был согласован с управлением. Первоначально AMT-130 сравнивали с плацебо — небольшой группе людей из первой когорты была проведена операция без введения препарата. За ними наблюдали в течение первых 12 месяцев исследования, после чего им предложили возможность получить препарат. Однако из-за прогрессирующего характера болезни Гентингтона и длительности исследований некоторые из этих людей перестали соответствовать критериям включения в исследование. Поэтому было принято решение об использовании внешних контролей из базы Enroll-HD.
Причина решения FDA неясна. Компания uniQure ждет передачи ей результатов встречи, после чего планирует «срочно взаимодействовать с FDA, чтобы найти пути для своевременного ускоренного одобрения AMT-130». Также она собирается обратиться к регуляторным органам Великобритании и других европейских стран.
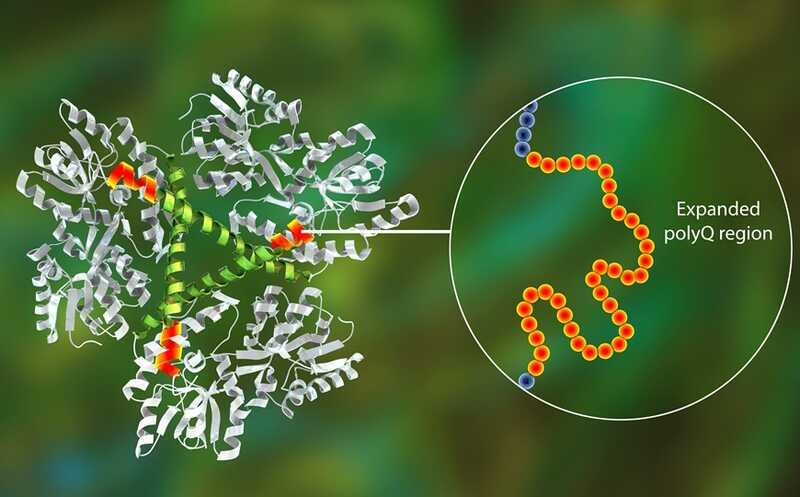 Credit: 123rf.com
Credit: 123rf.com
Банкротство 23andMe
Компания 23andMe, которая одной из первых начала оказывать услуги в области потребительской геномики, объявила о банкротстве в марте 2025 года. Тогда же компания сообщила об аукционе для продажи своих активов, в том числе генетических данных более 15 млн клиентов. Это событие вызвало дискуссии о жизнеспособности бизнес-модели «развлекательной генетики», а клиенты обеспокоились вопросом о безопасности своих данных, звучали призывы удалить свою информацию, пока не поздно.
Причиной банкротства 23andMe был назван слабый спрос на наборы для тестирования. Стоимость акций компании с 2021 года почти непрерывно снижалась. Кроме того, в 2023 году произошла утечка данных 7 млн клиентов, а 23andMe получила судебные иски. Компания также пережила несколько волн сокращений. Самая масштабная оптимизация произошла в ноябре 2024 года — уволили 40% персонала. В 2024 году стоимость акций компании на бирже была ниже $150 млн, тогда как в 2021-м она оценивалась в $6 млрд.
Энн Воджицки, соосновательница компании, писала в соцсетях, что «ушла с поста генерального директора, чтобы иметь возможность претендовать на компанию в качестве независимого участника торгов». Она заявила, что верит в 23andMe, а причиной проблем назвала «развивающуюся бизнес-модель».
В мае сообщалось, что американская фармкомпания Regeneron Pharmaceuticals выкупит 23andMe за $256 млн. Однако Энн Воджицки обратилась в федеральный суд США по делам о банкротстве с просьбой возобновить аукцион по продаже компании. Она утверждала, что нашла финансовую поддержку от компании из списка Fortune 500 с рыночной капитализацией более $400 млрд и $17 млрд наличными.По словам Воджицки, 23andMe и юридические консультанты несправедливо переориентировали аукцион в пользу Regeneron: хотя созданный ею TTAM Research Institute был готов предложить свыше $280 млн: аукцион закрыли раньше времени, не дав TTAM сделать ставку.
Воджицки удалось добиться пересмотра итога торгов. В новом раунде аукцион выиграл TTAM со ставкой в $305 млн. Сделка должна завершиться после одобрения в суде.
В заявлении TTAM оговорено, что новый владелец продолжит политику 23andMe, разрешающую использование анонимизированных данных клиентов для научных и биомедицинских исследований в академических университетах и других некоммерческих организациях, и по-прежнему будет «отклонять пожертвования от частных лиц или компаний в определенных странах».
 Credit: 123rf.com
Credit: 123rf.com
Геномные языковые модели и не только
Искусственный интеллект (ИИ) и машинное обучение находят все более широкое применение в биологии и медицине. За разработки в этой области было присуждено две Нобелевских премии в прошлом году — по химии и по физике, — однако развитие направления продолжается. Одно из важнейших приложений машинного обучения в исследованиях генома — это большие языковые модели, способные обрабатывать геномный язык и производить вычисления, опираясь на геномный контекст.
Какими же успехами могут похвастаться большие языковые модели в 2025 году применительно к биологии? Обученные на огромных объемах геномного «текста», они способны предсказывать продолжение (следующий нуклеотид) заданного участка или заполнять пропуски в нем, исходя из имеющегося контекста. Обзор инструментов ИИ, позволяющих «расшифровать грамматику генома», был опубликован в Nature, и важное место в нем было отведено именно геномным языковым моделям.
Evo, одна из таких моделей, была обучена на 300 миллиардах нуклеотидов, составляющих геномы различных бактерий, архей и бактериофагов.
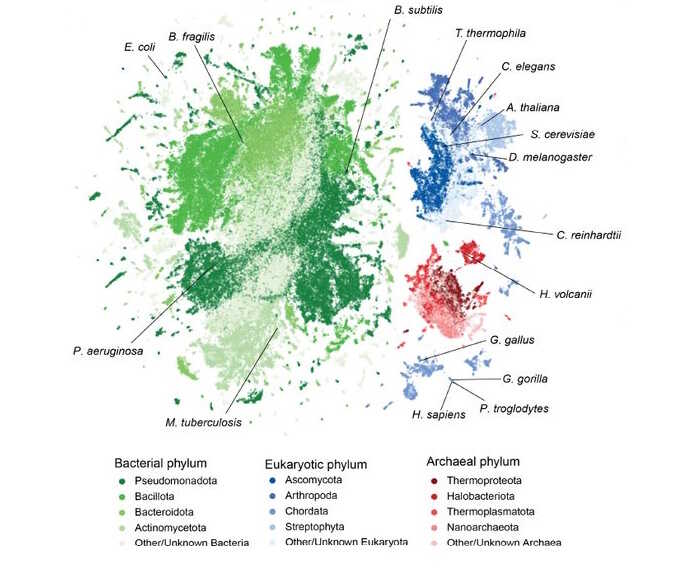 Обучающая выборка для Evo 2, по словам авторов, репрезентативна в контексте всей известной эволюции. Она охватывает широкий ряд таксонов бактерий, архей и эукариот. Credit: bioRxiv (2025). DOI: 10.1101/2025.02.18.638918 | CC BY-ND
Обучающая выборка для Evo 2, по словам авторов, репрезентативна в контексте всей известной эволюции. Она охватывает широкий ряд таксонов бактерий, архей и эукариот. Credit: bioRxiv (2025). DOI: 10.1101/2025.02.18.638918 | CC BY-ND
В 2025 году ее разработчики выпустили следующую версию — Evo 2 — которую обучили также на эукариотических геномах. Авторы утверждают, что таким образом они создали для обучения репрезентативную выборку, которая охватывает всю наблюдаемую эволюцию. Evo 2 надежно идентифицирует границы интронов и экзонов, предсказывает влияние мутаций и генерирует функциональные гены и геномные последовательности с нуля.
А ее первая версия — Evo, обученная на геномах прокариот, — нашла применение в новой концепции семантического проектирования. Она способна создавать функциональные гены de novo, опираясь только на организацию геномов, то есть на их контекст. С помощью Evo были получены системы токсин-антитоксин (как белковые, так и на основе РНК) и анти-CRISPR белки, в том числе не имеющие сходства последовательности с природными белками. Авторы этой работы создали и выложили в открытый доступ базу SynGenome, содержащую 120 гигабаз синтетической ДНК. Некоторые входящие в нее гены также выходили за пределы естественных последовательностей. Таким образом, геномные языковые модели позволяют быстро генерировать стартовые варианты, которые затем можно подвергнуть дальнейшей инженерии.
Ценность геномного контекста для разработки функциональных последовательностей подтвердили еще в одной работе. Создание терапевтических мРНК и мРНК-вакцин требует проектирования не только кодирующей последовательности, но и регуляторных областей, которые обеспечат оптимальную экспрессию. Для решения этой задачи ученые из Китая и США создали генеративную языковую РНК-модель, адаптированную под кодирующие последовательности и 5'-нетранслируемые области (UTR). Разработка получила название GEMORNA — generative model for RNA.
Модель, предназначенная для проектирования мРНК de novo, генерирует полноразмерную мРНК, содержащую как кодирующие участки, так и нетранслируемые области (5'-UTR и 3'-UTR). Как и Evo, она была обучена на природных кодирующих последовательностях, однако оказалась способна генерировать и принципиально отличные мРНК.
С помощью GEMORNA ее авторы сгенерировали мРНК эритропоэтина (линейную и кольцевую) и химерный антигенный рецептор к CD19, а также получили мРНК-вакцину от COVID-19. Сгенерированные последовательности обеспечивали высокую и стабильную экспрессию целевых генов в клеточных культурах и в организме мышей, превосходя коммерчески доступные аналоги.
Получение половых клеток человека из соматических — подход к лечению бесплодия
От бесплодия страдают миллионы людей в мире, и многие случаи вызваны дефицитом функциональных гамет — это одна из ведущих причин бесплодия у женщин в возрасте 35 лет и старше. При этом снижается и вероятность успеха экстракорпорального оплодотворения (ЭКО). Для лечения бесплодия в таком случае нужны гаплоидные ооциты, и ученые из Орегонского университета здравоохранения и науки под руководством Шухрата Миталипова получили их из человеческих соматических клеток.
Соматические клетки диплоидные, и чтобы получить их них гаплоидные гаметы, необходимо уменьшить их плоидность, подобно тому, как это естественным образом происходит при мейозе. Авторы исследования предложили экспериментальный процесс деления, сочетающий в себе черты как митоза, так и мейоза — он получил название «митомейоз». Идея заключается в том, чтобы вызвать преждевременное деление соматической клетки еще до удвоения ее генома. Ранее исследователи опробовали технологию на мышах; после оплодотворения полученного ооцита и его имплантации самкам-реципиентам у них рождалось нормальное способное к размножению потомство.
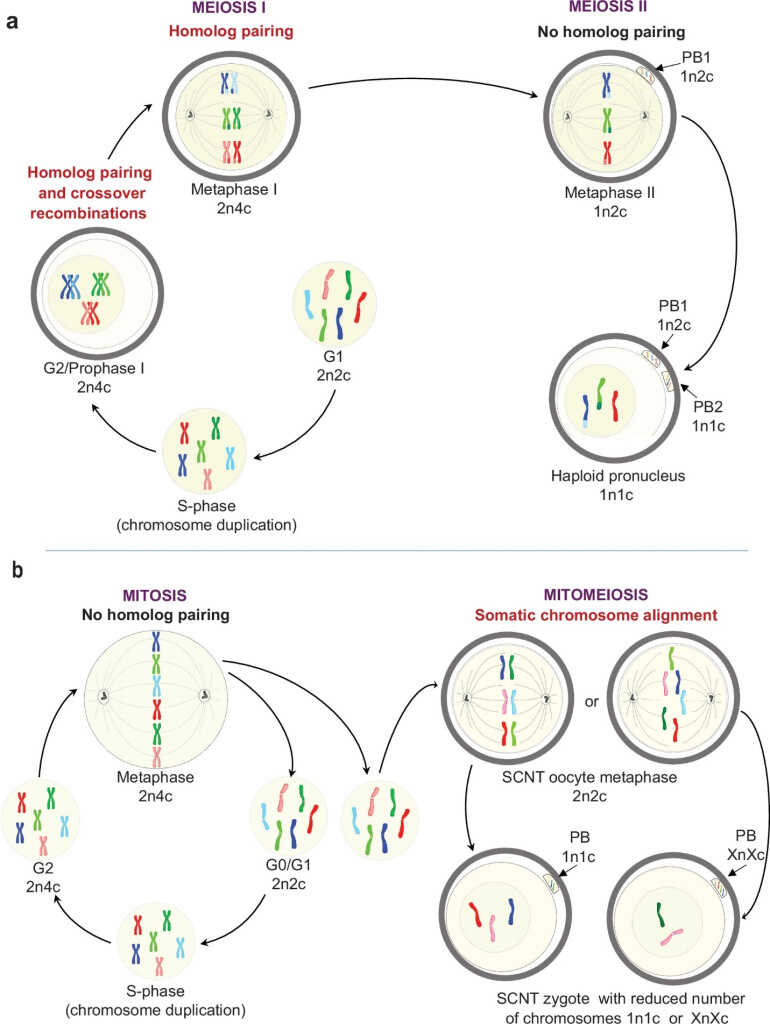 Естественный мейоз, митоз и митомейоз. PB — полярные тельца, в которых направляются «лишние» хромосомы в ходе оогенеза, чтобы получить гаплоидный пронуклеус ооцита; *n — число наборов хромосом, *c — число копий генома в клетке. Как и мейоз, митомейоз приводит к редукции плоидности (2n —> 1n). Однако к полюсам веретена деления расходятся не сестринские хроматиды, а гомологичные хромосомы соматической клетки. При этом возможны сбои и появление клеток с аномальным количеством хромосом. Credit: Nature Communications (2025). DOI:
10.1038/s41467-025-63454-7 |
CC BY-NC-ND 4.0
Естественный мейоз, митоз и митомейоз. PB — полярные тельца, в которых направляются «лишние» хромосомы в ходе оогенеза, чтобы получить гаплоидный пронуклеус ооцита; *n — число наборов хромосом, *c — число копий генома в клетке. Как и мейоз, митомейоз приводит к редукции плоидности (2n —> 1n). Однако к полюсам веретена деления расходятся не сестринские хроматиды, а гомологичные хромосомы соматической клетки. При этом возможны сбои и появление клеток с аномальным количеством хромосом. Credit: Nature Communications (2025). DOI:
10.1038/s41467-025-63454-7 |
CC BY-NC-ND 4.0
Теперь методику адаптировали для ооцитов человека. В энуклеированные, то есть лишенные ядра ооциты здоровых добровольцев, полученные стандартным применяемым в клинике путем, переносили ядра соматических клеток (фибробластов). Эта технология позволяет получать функциональные, хотя и диплоидные ооциты (somatic cell nuclear transfer, SCNT).
В норме первичные ооциты претерпевают задержку клеточного цикла в MII перед овуляцией и возвращаются к делению после оплодотворения. Однако в диплоидных ооцитах активация нарушается, и завершения мейоза после оплодотворения не происходит.
Остановка мейоза в ооцитах поддерживается высокой активностью двух известных регуляторов клеточного цикла — циклинзависимой протеинкиназы 1 (Cdk1) и циклина B. Исследователи протестировали различные режимы инактивации этих регуляторов и подобрали оптимальный, который включал повышенный уровень Ca2+ в среде, электропорацию и обработку росковитином — ингибитором Cdk1. Таким образом обработали 82 оплодотворенных ооцита, полученных переносом ядра. Большинство клеток стало проходить дальнейшие деления, и около 9% достигли стадии бластоцисты к шестому дню эксперимента.
Расхождение гомологичных хромосом происходило случайным образом и без кроссинговера, причем паттерны сегрегации хромосом между пронуклеусом и полярным тельцем варьировали. Однако в среднем в зиготе сохранялось 23 пары хромосом, что подтверждает возможность гаплоидизации соматических клеток с помощью митомейоза.
Нейроны отдают раковым клеткам митохондрии
Раковые клетки «отнимают» силы у своих здоровых соседей. В 2025 году исследователи из США открыли один из механизмов того, как они это делают. Нейроны передают раковым клеткам свои митохондрии, что способствует метастазированию.
То, что нервы способствуют росту опухоли, не новость. Еще в 2017 году было показано, что опухоли простаты уменьшались у мышей, если перерезать нервы, идущие к этой железе, или воздействовать на них ботоксом. Инъекции ботокса в предстательную железу у людей с опухолями в этом органе также увеличивали скорость гибели раковых клеток. T-клетки тоже иногда обмениваются митохондриями с раковыми клетками, но для нейронов этот процесс был показан впервые.
Исследователи наблюдали, как между клетками рака молочной железы и нейронами формировались «мостики», по которым меченные красителем митохондрии перемещались к раковым клеткам. Опухолевые клетки без митохондрий приобретали способность делиться, если культивировать их с нейронами.
Нейроны и раковые клетки модифицировали таким образом, что опухолевые клетки становились зелеными, получив митохондрии от нейронов. Если поместить такие клетки в тело мыши и дать развиться метастазам, то можно видеть, что только 5% раковых клеток в первичной опухоли получали митохондрии. Однако в метастазах в легких этот показатель достигал 27%, а в мозге — 46%. В образцах рака простаты, полученных от пациентов, митохондрий было больше в тех клетках, которые находились ближе к нервам.
Вполне возможно, это исследование не только улучшит наше понимание процессов, происходящих при опухолеобразовании, но и откроет новые пути к терапии рака.
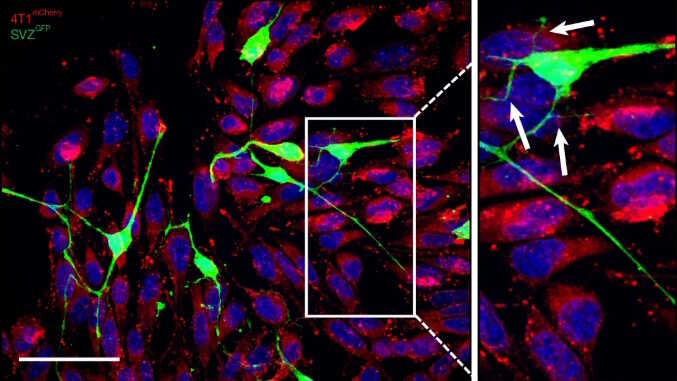 Конфокальная микрофотография. Белые стрелки указывают на установление контактов между нейронами и раковыми клетками. Credit: Gregory Hoover, et al. Nature, DOI:
10.1038/s41586-025-09176-8 |
CC 4.0
Конфокальная микрофотография. Белые стрелки указывают на установление контактов между нейронами и раковыми клетками. Credit: Gregory Hoover, et al. Nature, DOI:
10.1038/s41586-025-09176-8 |
CC 4.0
«Человек-дракон» из Харбина — денисовец
В отличие от неандертальцев, денисовцы были идентифицированы как отдельный таксон внутри рода Homo не по особенностям скелета, а по анализу ДНК или белков из костных останков. Эти останки — зубы, фаланги пальцев, фрагмент черепа, челюсти и т.п. — были слишком фрагментарными, чтобы по ним реконструировать внешность. В то же время многие останки плейцстоценовых Homo, из которых пока не выделена ДНК, могут принадлежать как неандертальцам, так и денисовцам (или еще какому-то их родственнику, пока неизвестному?). В 2025 году китайские ученые исследовали митохондриальную ДНК (мтДНК) и протеом образцов черепа древнего человека из Харбина. Первый автор обеих статей — палеогенетик Цяомэй Фу из пекинского Института палеонтологии позвоночных и палеоантропологии.
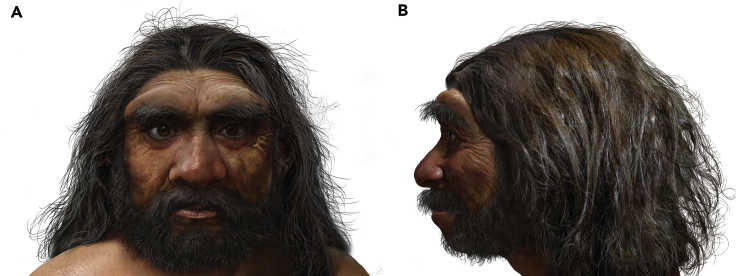
Череп был найден в 1933 году в провинции Хэйлунцзян при строительстве моста через реку Сунгари. Тогда это была территория империи Маньчжоу-Го. Находка оказалась у подрядчика строительства, и он решил скрыть ее от японской администрации. Позднее он не сообщал о находке и правительству Китайской Народной Республики, так как опасался обвинений в том, что работал на японцев, и раскрыл тайну только перед смертью. В 2018 году череп попал в руки ученых. Древнего человека назвали Homo longi, потому что провинцию Хэйлунцзян также называют Лунцзян (Longjiang) — «Река дракона», отсюда «человек-дракон». Авторы статьи 2021 года сделали вывод, что череп непохож на неандертальский, а единственный сохранившийся зуб сходен с денисовскими.
Выделить ДНК из зуба и каменистой части височной кости черепа не удалось. В итоге мтДНК была получена из зубного камня. Как сказала Цяомэй Фу в интервью National Geographic, митохондриальный геном «содержит 27 генетических вариантов, которые найдены только у семи известных индивидов-денисовцев. Ни один из них не мог появиться из-за контаминации ДНК современного человека». Филогенетический анализ подтвердил, что последовательность кластеризуется с денисовскими, причем наиболее сходной она была с самыми старыми образцами из Денисовской пещеры (187–217 тысяч лет назад; возраст харбинского индивида — более 146 тысяч лет).
Теперь у нас есть портрет денисовца, реконструированный по черепу. Интересно, что когда ученые из Еврейского университета в Иерусалиме воссоздали «цифровых денисовцев» на основе данных о метилировании их ДНК, человек из Харбина оказался очень похожим на них. Возможно, теперь будет проще находить новых денисовцев.


 Меню
Меню





 Все темы
Все темы
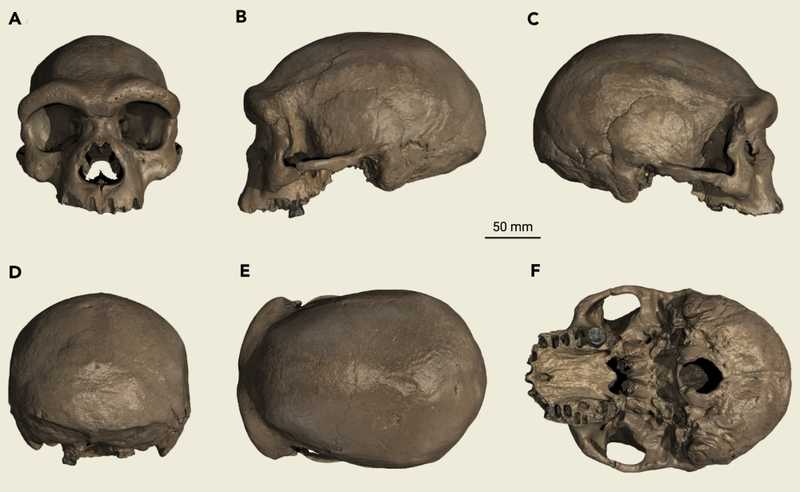 Credit: Innovation (Camb). 2021. DOI:
Credit: Innovation (Camb). 2021. DOI:




 0
0










